よむ、つかう、まなぶ。
資料4 新たに定期接種に位置づけられるワクチンに係る副反応疑い報告基準について[1.2MB] (10 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/newpage_00106.html |
| 出典情報 | 厚生科学審議会・薬事審議会(合同開催) 予防接種・ワクチン分科会副反応検討部会(第102回 7/29)医薬品等安全対策部会安全対策調査会(令和6年度第4回 7/29)(合同開催)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
第61回厚生科学審議会予防接種・ワクチン分科会
予
防
接
種
基
本
方
針
部
会
2024(令和6)年7月18日
資料
1
(改)
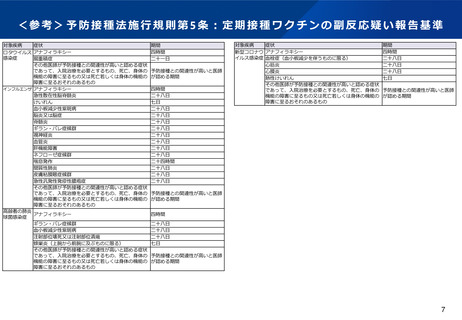
定期接種の対象者、接種方法及び用いるワクチン等について(小括)
まとめ
【PCV20の薬事上の規定】
• 薬事承認されたPCV20の接種対象者及び接種方法については、薬事上、PCV15と比較して大きな違いはない。
【小児肺炎球菌ワクチンの現行の予防接種法上の規定】
• 予防接種法施行令における、接種対象者の規定に係る部分については、PCV13およびPCV15とPCV20に薬事上
の差異はない。
• さらに、事務運用の詳細を「予防接種実施要領(健康局長通知)」として整理し、その中で標準的な接種時期を
示している。
【ワクチン小委員会での議論】
• PCV20はPCV13及びPCV15と比較して有効性の向上が期待でき、安全性に差がないと考えられる。
また、接種に係る費用が増加しない見込みであることが企業から示された。
【その他】
• 製造販売業者より、PCV20の発売と同時に、PCV13の供給を停止する意向が示されている。
第61回基本方針部会(令和6年7月18日)の検討結果
• 現行のPCV20の規定や小委員会での議論を踏まえ、PCV20を定期接種に用いるワクチンに位置づける。その際、
薬事上の承認内容に合わせて関係規定を見直す。
• PCV20はPCV13及びPCV15と比較して有効性の向上が期待でき、安全性に差がないと考えられる。ただし、現場の
運用上、PCV20に速やかに移行できない場合でも、肺炎球菌ワクチンの接種を確実に行う観点から、当面の間は
PCV15も使用できることとする。
• PCV13については、製造販売業者からPCV20の発売と同時に供給を停止する意向が示されているため、供給停止後
にPCV13を定期接種に位置づけるワクチンから除く。
10
予
防
接
種
基
本
方
針
部
会
2024(令和6)年7月18日
資料
1
(改)
定期接種の対象者、接種方法及び用いるワクチン等について(小括)
まとめ
【PCV20の薬事上の規定】
• 薬事承認されたPCV20の接種対象者及び接種方法については、薬事上、PCV15と比較して大きな違いはない。
【小児肺炎球菌ワクチンの現行の予防接種法上の規定】
• 予防接種法施行令における、接種対象者の規定に係る部分については、PCV13およびPCV15とPCV20に薬事上
の差異はない。
• さらに、事務運用の詳細を「予防接種実施要領(健康局長通知)」として整理し、その中で標準的な接種時期を
示している。
【ワクチン小委員会での議論】
• PCV20はPCV13及びPCV15と比較して有効性の向上が期待でき、安全性に差がないと考えられる。
また、接種に係る費用が増加しない見込みであることが企業から示された。
【その他】
• 製造販売業者より、PCV20の発売と同時に、PCV13の供給を停止する意向が示されている。
第61回基本方針部会(令和6年7月18日)の検討結果
• 現行のPCV20の規定や小委員会での議論を踏まえ、PCV20を定期接種に用いるワクチンに位置づける。その際、
薬事上の承認内容に合わせて関係規定を見直す。
• PCV20はPCV13及びPCV15と比較して有効性の向上が期待でき、安全性に差がないと考えられる。ただし、現場の
運用上、PCV20に速やかに移行できない場合でも、肺炎球菌ワクチンの接種を確実に行う観点から、当面の間は
PCV15も使用できることとする。
• PCV13については、製造販売業者からPCV20の発売と同時に供給を停止する意向が示されているため、供給停止後
にPCV13を定期接種に位置づけるワクチンから除く。
10