よむ、つかう、まなぶ。
資料1-2:日本医療機器産業連合会 谷岡委員 提出資料 (14 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_49984.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第39回 1/29)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
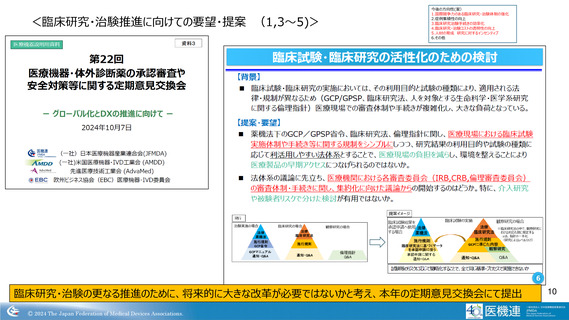
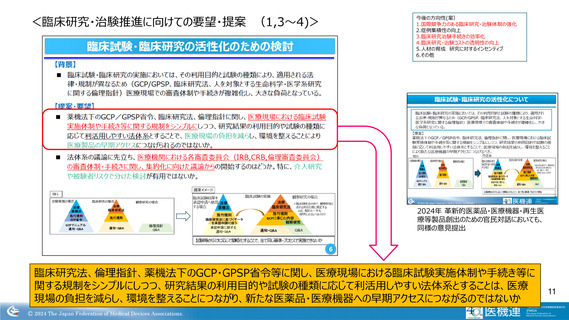
<臨床研究・治験推進に向けての要望・提案 2,その他>
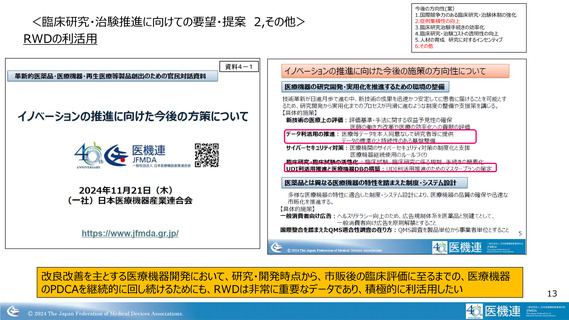
RWDの利活用
2024年 革新的医薬品・医療機器・再生医療等製品創出のための官民対話資料より
医療機器の特定可能な情報が必要
RWDの利活用推進のための規制等の整備推進
・開発段階での医療情報の2次利用の際の困難さへの対応→特別法、ガイドライン、基準等の検討、制定等
(例えば、教師データ収集を含むAI機器開発は医療情報を2次利用した臨床研究とみなされ、個人情報保護法や倫理指針遵守
必要 → 複数の法令調査必須、解釈等非常に難しい状況での対応)
・製品開発、承認申請、市販後調査への利活用のため、医療機器の特定が可能なDBの構築、工夫等
→UDI DB*、保険上の特定コード** 別目的のデータであってもリンク可能で利活用可能な状態へ
*制度部会で検討中
**現在のNDBは機能区分のデータであり、製品特定不可能、要望中
Ⓒ 2024 The Japan Federation of Medical Devices Associations.
14
RWDの利活用
2024年 革新的医薬品・医療機器・再生医療等製品創出のための官民対話資料より
医療機器の特定可能な情報が必要
RWDの利活用推進のための規制等の整備推進
・開発段階での医療情報の2次利用の際の困難さへの対応→特別法、ガイドライン、基準等の検討、制定等
(例えば、教師データ収集を含むAI機器開発は医療情報を2次利用した臨床研究とみなされ、個人情報保護法や倫理指針遵守
必要 → 複数の法令調査必須、解釈等非常に難しい状況での対応)
・製品開発、承認申請、市販後調査への利活用のため、医療機器の特定が可能なDBの構築、工夫等
→UDI DB*、保険上の特定コード** 別目的のデータであってもリンク可能で利活用可能な状態へ
*制度部会で検討中
**現在のNDBは機能区分のデータであり、製品特定不可能、要望中
Ⓒ 2024 The Japan Federation of Medical Devices Associations.
14