よむ、つかう、まなぶ。
資料1-2:日本医療機器産業連合会 谷岡委員 提出資料 (7 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_49984.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第39回 1/29)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
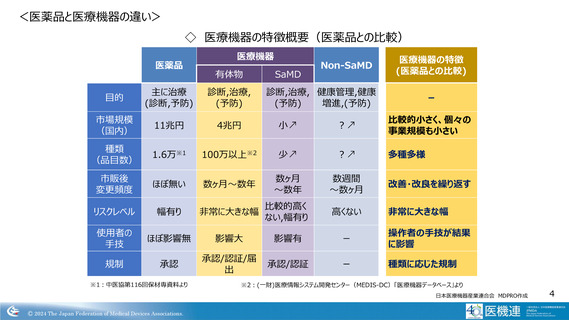
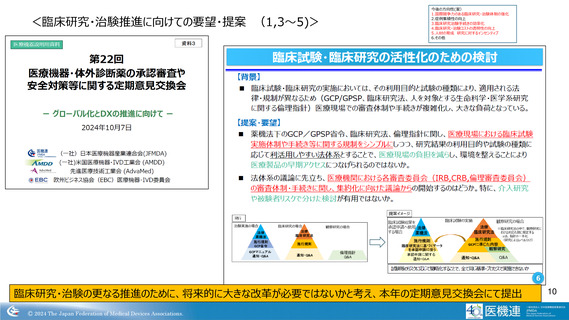
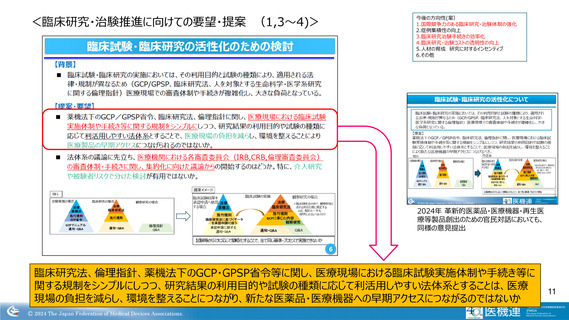
<医療機器治験の現状>
医療機器は、新医療機器やリスクの高いもの、治療用のプログラム等、
治験が必要なものもある。多額の費用を要する治験の実施は、開発費
用を回収できるかが投資基準のひとつであるが、診療報酬上の評価等
も含めた医療機器の価格や事業規模の問題等から新技術開発への投
資が難しい悪循環が発生。
革新的医療機器の開発、導入のためにも治験環境の改善、効率化等
は重要。
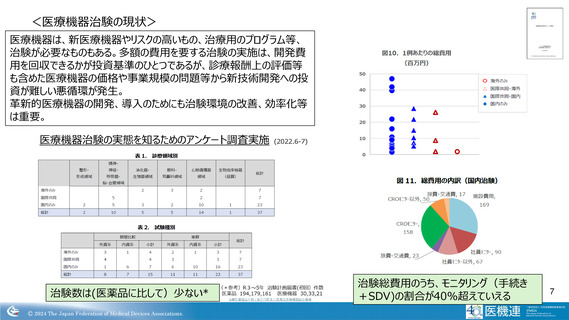
医療機器治験の実態を知るためのアンケート調査実施 (2022.6-7)
治験数は(医薬品に比して)少ない*
Ⓒ 2024 The Japan Federation of Medical Devices Associations.
治験総費用のうち、モニタリング(手続き
+SDV)の割合が40%超えていえる
7
医療機器は、新医療機器やリスクの高いもの、治療用のプログラム等、
治験が必要なものもある。多額の費用を要する治験の実施は、開発費
用を回収できるかが投資基準のひとつであるが、診療報酬上の評価等
も含めた医療機器の価格や事業規模の問題等から新技術開発への投
資が難しい悪循環が発生。
革新的医療機器の開発、導入のためにも治験環境の改善、効率化等
は重要。
医療機器治験の実態を知るためのアンケート調査実施 (2022.6-7)
治験数は(医薬品に比して)少ない*
Ⓒ 2024 The Japan Federation of Medical Devices Associations.
治験総費用のうち、モニタリング(手続き
+SDV)の割合が40%超えていえる
7