よむ、つかう、まなぶ。
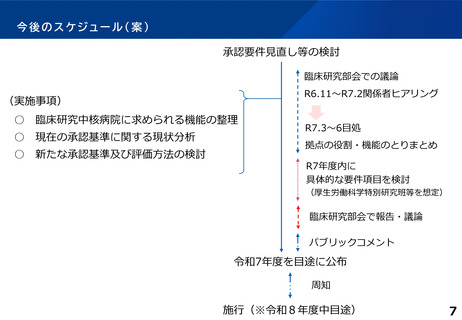
資料2:臨床研究中核病院の承認要件見直しについて (10 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_55079.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第41回 3/19)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
人材育成
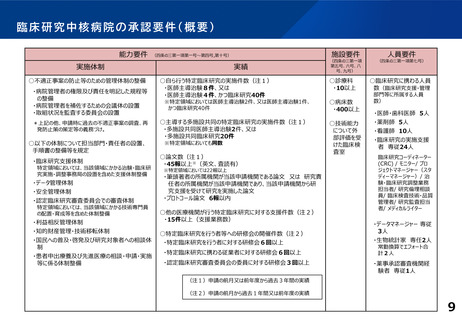
橋渡し研究支援機関認定要件(概要)
機能分類
①
拠点内で
備える
べき機能
体制
要綱第3条第1項第1号及び第2号
組織体制
⚫ 橋渡し研究支援を実施する専門人材を確
保・登用する体制
⚫ 橋渡し研究に対する国民の理解を高めるた
めの啓発・広報活動を実施する体制
⚫ 橋渡し研究支援を実施する専門人材が情
報交換をする体制
⚫ シーズを発掘・評価・選定する体制
⚫ プロジェクトを管理する体制
⚫ 非臨床試験を管理する体制
⚫ 試験物の製造を管理する体制
⚫ First-in-Human(FIH)試験を計画・
実施する体制
⚫ 臨床試験を計画・実施する体制
⚫
他組織や ⚫ 多施設共同研究を計画・実施する体制
研究データの信頼性を確保する体制
他機関と ⚫ 関係法令・指針等を遵守させる体制
⚫ 研究の倫理性・科学性・安全性・利益相
の連携
反を審査・管理する体制
⚫ データセンターを運用する体制
でも可
⚫ モニタリング体制
⚫ 監査体制
⚫ 臨床試験ネットワークを運用する体制
⚫ 起業・技術移転を支援する体制
⚫ 臨床研究について教育・啓発・広報する体
制
②
③
特色
⚫ 細胞培養加工施設を運用する体制
⚫ 製剤製造設備を運用する体制
⚫ 国際共同臨床研究・治験等における規制
当局への対応等、国際水準の支援をする
体制
⚫ その他特色のある支援体制
人員
⚫
⚫
⚫
⚫
⚫
⚫
⚫
拠点長
数値要件
拠点統括
開発企画担当者
シーズ発掘担当者
シーズ評価担当者
プロジェクトマネージャー
拠点間連携担当者・拠点
外支援担当者
⚫ 薬事担当者
⚫ メディカルライター
⚫ 非臨床(安全性・動態)
品質管理担当者
⚫ 試験物品質管理担当者
⚫ 臨床研究コーディネーター
⚫ データマネージャー
⚫ 生物統計家
⚫ 安全性情報担当者
⚫ 情報システム担当者
⚫ モニター
⚫ 監査担当者
⚫ 研究倫理相談員
⚫ 法務担当者
⚫ 起業・資金調達支援者
⚫ 産学連携担当者
⚫ 知的財産管理担当者
⚫ 広報担当者
⚫ 教育担当者
⚫ CMC試験担当者
⚫ 安全性試験担当者
⚫ 国際対応実務担当者
実績
要綱第3条第1項第3号
取組
⚫ 拠点内外のシーズの発掘・育成・実
用化支援
⚫ 実用化を見据えた客観的な評価基
準によるシーズの選定
⚫ シーズの進捗管理
⚫ シーズのステージアップ又は支援中
断・中止の判断を含む評価
⚫ 実用化に向けた開発方針の策定の
支援及び開発戦略の立案
⚫ 企業や異分野の研究者との連携
⚫ 企業とのマッチング及び企業等への導
出の支援
⚫ 異分野シーズのマッチング・融合
⚫ 戦略的な知的財産の取得及び活用
の支援
⚫ 拠点による研究成果の頑健性に対
する科学的評価
⚫ 国際共同臨床研究・治験等におけ
る規制当局への対応等、国際水準
の支援
⚫ シーズの最適化支援
⚫ その他特色のある支援
取組の成果
数値要件
⚫ 臨床試験の届
出件数(直近
5年間)
⚫ 企業等への導
出件数(直近
5年間)
⚫ 製造販売承認・
認証の申請件
数(直近5年
間)
要綱第3条第1項
第4号
取組
⚫ 専門人材の育成
• プロジェクトマネー
ジャー
● 研究者の育成
• 薬事規制
• 知的財産
• 医療技術開発
⚫ 専門人材の育成
• 薬事担当者
• 非臨床(安全性・
動態)品質管理
担当者
• 試験物品質管理
担当者
• 生物統計家
• 知的財産管理担
当者
⚫ その他特色のある
取組
10
橋渡し研究支援機関認定要件(概要)
機能分類
①
拠点内で
備える
べき機能
体制
要綱第3条第1項第1号及び第2号
組織体制
⚫ 橋渡し研究支援を実施する専門人材を確
保・登用する体制
⚫ 橋渡し研究に対する国民の理解を高めるた
めの啓発・広報活動を実施する体制
⚫ 橋渡し研究支援を実施する専門人材が情
報交換をする体制
⚫ シーズを発掘・評価・選定する体制
⚫ プロジェクトを管理する体制
⚫ 非臨床試験を管理する体制
⚫ 試験物の製造を管理する体制
⚫ First-in-Human(FIH)試験を計画・
実施する体制
⚫ 臨床試験を計画・実施する体制
⚫
他組織や ⚫ 多施設共同研究を計画・実施する体制
研究データの信頼性を確保する体制
他機関と ⚫ 関係法令・指針等を遵守させる体制
⚫ 研究の倫理性・科学性・安全性・利益相
の連携
反を審査・管理する体制
⚫ データセンターを運用する体制
でも可
⚫ モニタリング体制
⚫ 監査体制
⚫ 臨床試験ネットワークを運用する体制
⚫ 起業・技術移転を支援する体制
⚫ 臨床研究について教育・啓発・広報する体
制
②
③
特色
⚫ 細胞培養加工施設を運用する体制
⚫ 製剤製造設備を運用する体制
⚫ 国際共同臨床研究・治験等における規制
当局への対応等、国際水準の支援をする
体制
⚫ その他特色のある支援体制
人員
⚫
⚫
⚫
⚫
⚫
⚫
⚫
拠点長
数値要件
拠点統括
開発企画担当者
シーズ発掘担当者
シーズ評価担当者
プロジェクトマネージャー
拠点間連携担当者・拠点
外支援担当者
⚫ 薬事担当者
⚫ メディカルライター
⚫ 非臨床(安全性・動態)
品質管理担当者
⚫ 試験物品質管理担当者
⚫ 臨床研究コーディネーター
⚫ データマネージャー
⚫ 生物統計家
⚫ 安全性情報担当者
⚫ 情報システム担当者
⚫ モニター
⚫ 監査担当者
⚫ 研究倫理相談員
⚫ 法務担当者
⚫ 起業・資金調達支援者
⚫ 産学連携担当者
⚫ 知的財産管理担当者
⚫ 広報担当者
⚫ 教育担当者
⚫ CMC試験担当者
⚫ 安全性試験担当者
⚫ 国際対応実務担当者
実績
要綱第3条第1項第3号
取組
⚫ 拠点内外のシーズの発掘・育成・実
用化支援
⚫ 実用化を見据えた客観的な評価基
準によるシーズの選定
⚫ シーズの進捗管理
⚫ シーズのステージアップ又は支援中
断・中止の判断を含む評価
⚫ 実用化に向けた開発方針の策定の
支援及び開発戦略の立案
⚫ 企業や異分野の研究者との連携
⚫ 企業とのマッチング及び企業等への導
出の支援
⚫ 異分野シーズのマッチング・融合
⚫ 戦略的な知的財産の取得及び活用
の支援
⚫ 拠点による研究成果の頑健性に対
する科学的評価
⚫ 国際共同臨床研究・治験等におけ
る規制当局への対応等、国際水準
の支援
⚫ シーズの最適化支援
⚫ その他特色のある支援
取組の成果
数値要件
⚫ 臨床試験の届
出件数(直近
5年間)
⚫ 企業等への導
出件数(直近
5年間)
⚫ 製造販売承認・
認証の申請件
数(直近5年
間)
要綱第3条第1項
第4号
取組
⚫ 専門人材の育成
• プロジェクトマネー
ジャー
● 研究者の育成
• 薬事規制
• 知的財産
• 医療技術開発
⚫ 専門人材の育成
• 薬事担当者
• 非臨床(安全性・
動態)品質管理
担当者
• 試験物品質管理
担当者
• 生物統計家
• 知的財産管理担
当者
⚫ その他特色のある
取組
10