よむ、つかう、まなぶ。
資料2:臨床研究中核病院の承認要件見直しについて (7 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_55079.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第41回 3/19)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
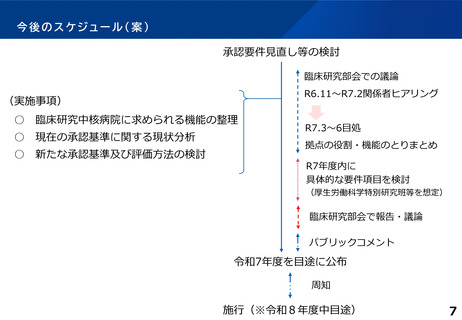
今後のスケジュール(案)
承認要件見直し等の検討
臨床研究部会での議論
R6.11~R7.2関係者ヒアリング
(実施事項)
○
臨床研究中核病院に求められる機能の整理
○ 現在の承認基準に関する現状分析
○
新たな承認基準及び評価方法の検討
R7.3~6目処
拠点の役割・機能のとりまとめ
R7年度内に
具体的な要件項目を検討
(厚生労働科学特別研究班等を想定)
臨床研究部会で報告・議論
パブリックコメント
令和7年度を目途に公布
周知
施行(※令和8年度中目途)
7
承認要件見直し等の検討
臨床研究部会での議論
R6.11~R7.2関係者ヒアリング
(実施事項)
○
臨床研究中核病院に求められる機能の整理
○ 現在の承認基準に関する現状分析
○
新たな承認基準及び評価方法の検討
R7.3~6目処
拠点の役割・機能のとりまとめ
R7年度内に
具体的な要件項目を検討
(厚生労働科学特別研究班等を想定)
臨床研究部会で報告・議論
パブリックコメント
令和7年度を目途に公布
周知
施行(※令和8年度中目途)
7