よむ、つかう、まなぶ。
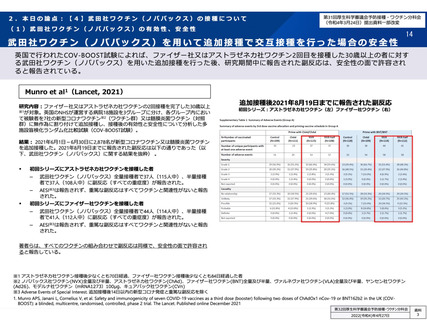
参考資料1-1 新型コロナウイルスワクチン(ノババックス、J&J)接種後の採血制限期間について(令和4年7月22日開催 大隈班会議資料) (9 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_27504.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会血液事業部会安全技術調査会(令和4年度第2回 8/23)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
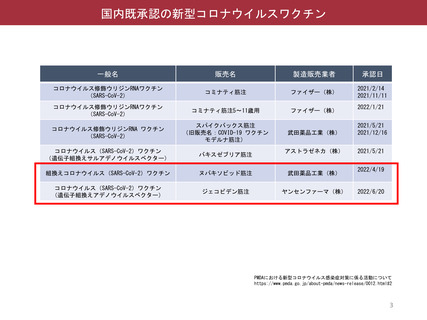
2. 本日の論点: 【4】武田社ワクチン (ノババックス) の接種について (1) 武田社ワクチン (ノババックス) の有効性、安全性
武田社ワクチン (ノババックス) の安全性 第31回厚生科学審議会予防接種・ワクチング和会
(令和4年3月24日) 提出資料一部改変
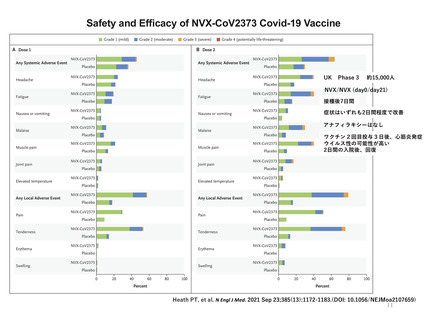
18歳以上について、武田社ワクチン (ノババックス) の初回シリーズ接種後7日までの局所・全身反応は軽度て中等度
で一過性であり、著者らは追跡期間中に安全性の懸念は認められなかったと報告している。
Dunkle LM et al (NEJM, 2022) 接種後7日までに出現した局所・全身副反応
研究内容 : 2020年12月27日-2021年2月18日の間に米国113施設、メキシコ6施 間 半 0
設において、18歳以上を対象に武田社 ワクチン (ノババックス) 2回接種群と "el 削2
プラセボ接種群を2: 1で無作為に割り付け、武田社ワクチン (ノババックス) 2 ok
回接種後の有効性及び安全性を評価したフェーズ本試験。 1 4 しししし
結果 : 26.976名 (ワクチン接種群18,072名、プラセボ和群8.904名) が解析さ 1ド 和
れた (年齢中央値47.0歳) 。 el
接種後日目までの安補性は以下の通りであった。 asP | | | | |UI
局所・全身反応ともに多くは軽度一中等度で、一過性であった。 ES
* プラセボ接種群と比較しワクチン接種群では、局所・全身反応がより多く報 B ymemc
告された。 sl 介[ 人FT
す 局所反応 Musde pen | ee e
ー 多くは軽度中等度で、 持締期間は2日以下であった。 iT
ー 接種部位の圧痛が最も多くみられ、1回目接種52.39%、2回目接種73.4%、 ーー
-持続期間中央値は2日であった。 是 M
* 生身反応 " 抽 市導ああきす 吉語 寺
ー 億怠感、頭痛、筋肉痛、活気不良が多く見られた。 al
ー 重度の全身反応はワクチン接種群 (12.1%) がプラセボ群 (2.1%) より ws| ーー ・
も多かったが、他種のコロナウイルスワクチン※!より少なかった。 間間間aa 『
追跡期間中※2報告されたすべての重症度の副反応%3の発生割合は以下の通りで Se
あっ > Fcver に
。 ワクチン接種群 : 16.3% る 古おああおす5 大
・ プラセボ接種群 : 14.8% aa
※1 モデルナ社ワクチン (Baden LR et al, 2021 を文中引用。)
※2 本研究はクロスオーバー試験であり、1回目接種から3 4か月後に、ワクチン群にはプラセボを、プラセボ群にはワクチンを接種した。副反応は、この3 -4か月後の異なる薬剤の接種まで、もし
くは参加者の研究からの辞退時点まで観察されている。
※3 副反応には局所反応として疲痛、圧痛、紅班、腫且、全身反応として頭痛、供臣感、活気不良、筋肉痛、関節痛、発熱、嘱気・嘱吐を含む。 第32回厚生科学審議会予防接種・ワクチン分科会 | 資料
3
1 Dunkle LM, Kotloff KL, Gay CL et al. Efficacy and Safety of NVX-CoV2373 in Adults in the United States and Mexico. N Engl J Med. 2022:386(6):531-543. 2日
9
武田社ワクチン (ノババックス) の安全性 第31回厚生科学審議会予防接種・ワクチング和会
(令和4年3月24日) 提出資料一部改変
18歳以上について、武田社ワクチン (ノババックス) の初回シリーズ接種後7日までの局所・全身反応は軽度て中等度
で一過性であり、著者らは追跡期間中に安全性の懸念は認められなかったと報告している。
Dunkle LM et al (NEJM, 2022) 接種後7日までに出現した局所・全身副反応
研究内容 : 2020年12月27日-2021年2月18日の間に米国113施設、メキシコ6施 間 半 0
設において、18歳以上を対象に武田社 ワクチン (ノババックス) 2回接種群と "el 削2
プラセボ接種群を2: 1で無作為に割り付け、武田社ワクチン (ノババックス) 2 ok
回接種後の有効性及び安全性を評価したフェーズ本試験。 1 4 しししし
結果 : 26.976名 (ワクチン接種群18,072名、プラセボ和群8.904名) が解析さ 1ド 和
れた (年齢中央値47.0歳) 。 el
接種後日目までの安補性は以下の通りであった。 asP | | | | |UI
局所・全身反応ともに多くは軽度一中等度で、一過性であった。 ES
* プラセボ接種群と比較しワクチン接種群では、局所・全身反応がより多く報 B ymemc
告された。 sl 介[ 人FT
す 局所反応 Musde pen | ee e
ー 多くは軽度中等度で、 持締期間は2日以下であった。 iT
ー 接種部位の圧痛が最も多くみられ、1回目接種52.39%、2回目接種73.4%、 ーー
-持続期間中央値は2日であった。 是 M
* 生身反応 " 抽 市導ああきす 吉語 寺
ー 億怠感、頭痛、筋肉痛、活気不良が多く見られた。 al
ー 重度の全身反応はワクチン接種群 (12.1%) がプラセボ群 (2.1%) より ws| ーー ・
も多かったが、他種のコロナウイルスワクチン※!より少なかった。 間間間aa 『
追跡期間中※2報告されたすべての重症度の副反応%3の発生割合は以下の通りで Se
あっ > Fcver に
。 ワクチン接種群 : 16.3% る 古おああおす5 大
・ プラセボ接種群 : 14.8% aa
※1 モデルナ社ワクチン (Baden LR et al, 2021 を文中引用。)
※2 本研究はクロスオーバー試験であり、1回目接種から3 4か月後に、ワクチン群にはプラセボを、プラセボ群にはワクチンを接種した。副反応は、この3 -4か月後の異なる薬剤の接種まで、もし
くは参加者の研究からの辞退時点まで観察されている。
※3 副反応には局所反応として疲痛、圧痛、紅班、腫且、全身反応として頭痛、供臣感、活気不良、筋肉痛、関節痛、発熱、嘱気・嘱吐を含む。 第32回厚生科学審議会予防接種・ワクチン分科会 | 資料
3
1 Dunkle LM, Kotloff KL, Gay CL et al. Efficacy and Safety of NVX-CoV2373 in Adults in the United States and Mexico. N Engl J Med. 2022:386(6):531-543. 2日
9