よむ、つかう、まなぶ。
【資料2-2】新型コロナウイルス感染症ワクチンの添付文書の改訂について(医薬・生活衛生局からの説明資料) (7 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_30030.html |
| 出典情報 | 医薬品等行政評価・監視委員会(第10回 12/27)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
No.
一般名
関連資料・関連情報等
薬効
分類
改訂内容
改訂理由
直近3年度の国内副作用症例
の集積状況 【転帰死亡症例】
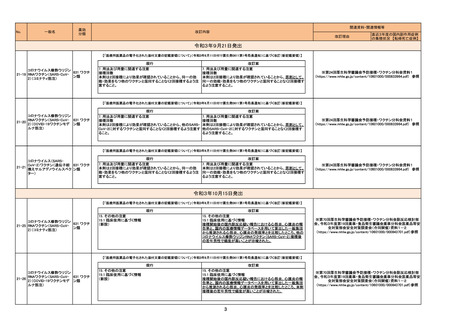
令和4年7月8日発出
【「医療用医薬品の電子化された添付文書の記載要領について」(令和3年6月11日付け薬生発0611第1号局長通知)に基づく改訂(新記載要領)】
現行
組換えコロナウイルス
631 ワクチ
22-24 (SARS-CoV-2)ワクチン(ヌ
ン類
バキソビッド筋注)
改訂案
8. 重要な基本的注意
心筋炎、心膜炎が報告されているため、被接種者又はその保護者
に対しては、心筋炎、心膜炎が疑われる症状(胸痛、動悸、むく
み、呼吸困難、頻呼吸等)が認められた場合には、速やかに医師
の診察を受けるよう事前に知らせること。
8. 重要な基本的注意
(新設)
※第81回厚生科学審議会予防接種・ワクチン分科会副反応検討部
会、令和4年度第6回薬事・食品衛生審議会薬事分科会医薬品等安
全対策部会安全対策調査会(合同開催)資料1-9
(https://www.mhlw.go.jp/stf/shingi2/0000208910_00043.html)参照
令和4年10月19日発出
【「医療用医薬品の電子化された添付文書の記載要領について」(令和3年6月11日付け薬生発0611第1号局長通知)に基づく改訂(新記載要領)】
コロナウイルス修飾ウリジン
RNAワクチン(SARS-CoV-2)
(コミナティRTU筋注(2価:起
源株/オミクロン株BA.1)、コ 631 ワクチ
22-50
ミナティRTU筋注(2価:起源
ン類
株/オミクロン株BA.4-5)、ス
パイクバックス筋注(2価:起
源株/オミクロン株BA.1))
現行
7. 用法及び用量に関連する注意
接種時期
通常、前回のSARS-CoV-2ワクチンの接種から少なくとも5ヵ月経
過した後に接種することができる。
改訂案
7. 用法及び用量に関連する注意
接種時期
通常、前回のSARS-CoV-2ワクチンの接種から少なくとも3ヵ月経
過した後に接種することができる。
令和4年度第11回薬事・食品衛生審議会医薬品第二部会資料
(https://www.mhlw.go.jp/stf/newpage_28695.html)参照
【「医療用医薬品の電子化された添付文書の記載要領について」(令和3年6月11日付け薬生発0611第1号局長通知)に基づく改訂(新記載要領)】
22-51
コロナウイルス修飾ウリジン
RNAワクチン(SARS-CoV- 631 ワクチ
2)(コミナティ筋注(1価:起源
ン類
株))
現行
7. 用法及び用量に関連する注意
追加免疫
接種対象者
12歳以上の者。SARS-CoV-2の流行状況や個々の背景因子等を
踏ま え、ベネフィットとリスクを考慮し、追加免疫の要否を判断す
ること。
改訂案
7. 用法及び用量に関連する注意
追加免疫
接種対象者
過去に初回免疫又は追加免疫としてSARS-CoV-2ワクチンの接種
歴のある12歳以上の者。SARS-CoV-2の流行状況や個々の背景
因子等を踏まえ、ベネフィットとリスクを考慮し、追加免疫の要否を
判断すること。
接種時期
接種時期
通常、本剤2回目の接種から少なくとも5ヵ月経過した後に3回目の 通常、前回のSARS-CoV-2ワクチンの接種から少なくとも3ヵ月経
接種を行うことができる。
過した後に接種することができる。
4回目接種については、ベネフィットとリスクを考慮した上で、高齢 (削除)
者等において、本剤3回目の接種から少なくとも5ヵ月経過した後に
接種を判断することができる。
他のSARS-CoV-2ワクチンを接種した者に追加免疫として本剤を
接種した際の有効性、安全性は確立していない。
本剤以外のSARS-CoV-2ワクチンを接種した者に追加免疫として
本剤を接種した際の有効性及び安全性は確立していない。
7
22-50に同じ
一般名
関連資料・関連情報等
薬効
分類
改訂内容
改訂理由
直近3年度の国内副作用症例
の集積状況 【転帰死亡症例】
令和4年7月8日発出
【「医療用医薬品の電子化された添付文書の記載要領について」(令和3年6月11日付け薬生発0611第1号局長通知)に基づく改訂(新記載要領)】
現行
組換えコロナウイルス
631 ワクチ
22-24 (SARS-CoV-2)ワクチン(ヌ
ン類
バキソビッド筋注)
改訂案
8. 重要な基本的注意
心筋炎、心膜炎が報告されているため、被接種者又はその保護者
に対しては、心筋炎、心膜炎が疑われる症状(胸痛、動悸、むく
み、呼吸困難、頻呼吸等)が認められた場合には、速やかに医師
の診察を受けるよう事前に知らせること。
8. 重要な基本的注意
(新設)
※第81回厚生科学審議会予防接種・ワクチン分科会副反応検討部
会、令和4年度第6回薬事・食品衛生審議会薬事分科会医薬品等安
全対策部会安全対策調査会(合同開催)資料1-9
(https://www.mhlw.go.jp/stf/shingi2/0000208910_00043.html)参照
令和4年10月19日発出
【「医療用医薬品の電子化された添付文書の記載要領について」(令和3年6月11日付け薬生発0611第1号局長通知)に基づく改訂(新記載要領)】
コロナウイルス修飾ウリジン
RNAワクチン(SARS-CoV-2)
(コミナティRTU筋注(2価:起
源株/オミクロン株BA.1)、コ 631 ワクチ
22-50
ミナティRTU筋注(2価:起源
ン類
株/オミクロン株BA.4-5)、ス
パイクバックス筋注(2価:起
源株/オミクロン株BA.1))
現行
7. 用法及び用量に関連する注意
接種時期
通常、前回のSARS-CoV-2ワクチンの接種から少なくとも5ヵ月経
過した後に接種することができる。
改訂案
7. 用法及び用量に関連する注意
接種時期
通常、前回のSARS-CoV-2ワクチンの接種から少なくとも3ヵ月経
過した後に接種することができる。
令和4年度第11回薬事・食品衛生審議会医薬品第二部会資料
(https://www.mhlw.go.jp/stf/newpage_28695.html)参照
【「医療用医薬品の電子化された添付文書の記載要領について」(令和3年6月11日付け薬生発0611第1号局長通知)に基づく改訂(新記載要領)】
22-51
コロナウイルス修飾ウリジン
RNAワクチン(SARS-CoV- 631 ワクチ
2)(コミナティ筋注(1価:起源
ン類
株))
現行
7. 用法及び用量に関連する注意
追加免疫
接種対象者
12歳以上の者。SARS-CoV-2の流行状況や個々の背景因子等を
踏ま え、ベネフィットとリスクを考慮し、追加免疫の要否を判断す
ること。
改訂案
7. 用法及び用量に関連する注意
追加免疫
接種対象者
過去に初回免疫又は追加免疫としてSARS-CoV-2ワクチンの接種
歴のある12歳以上の者。SARS-CoV-2の流行状況や個々の背景
因子等を踏まえ、ベネフィットとリスクを考慮し、追加免疫の要否を
判断すること。
接種時期
接種時期
通常、本剤2回目の接種から少なくとも5ヵ月経過した後に3回目の 通常、前回のSARS-CoV-2ワクチンの接種から少なくとも3ヵ月経
接種を行うことができる。
過した後に接種することができる。
4回目接種については、ベネフィットとリスクを考慮した上で、高齢 (削除)
者等において、本剤3回目の接種から少なくとも5ヵ月経過した後に
接種を判断することができる。
他のSARS-CoV-2ワクチンを接種した者に追加免疫として本剤を
接種した際の有効性、安全性は確立していない。
本剤以外のSARS-CoV-2ワクチンを接種した者に追加免疫として
本剤を接種した際の有効性及び安全性は確立していない。
7
22-50に同じ