よむ、つかう、まなぶ。
【資料3】我が国の薬事制度に関する海外への情報発信について (5 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_36390.html |
| 出典情報 | 創薬力の強化・安定供給の確保等のための薬事規制のあり方に関する検討会(第5回 11/15)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
▍PMDAの次期中期計画(令和6年度~)の方向性
・PMDAは、厚生労働省が5年毎に作成する中期目標に従って中期計画を作成、独立行政法人評価委員会において毎年実績を評価・公表
されている。
・令和6年度から次期中期計画が始まる予定。
【次期中期計画の方向性】(抜粋)
2.審査等業務
(1) 医薬品審査業務の迅速かつ的確な実施
① 世界最速レベルの審査期間の堅持と効率的で質の高い審査
② Early consideration の発信や最新の科学的知見に基づく臨床評価ガイドラインの策定などイノベーションに的確に
対応した相談及び審査の実施
* Early consideration とは、情報等が十分に収集されていない段階ではある ものの、イノベーションの実用化と革新的な医薬品等の開発促進
の参考情報として、その時点における開発の方向性に係る審査側の考え方を示したもの。
③ 希少疾病用医薬品、小児用医薬品など患者ニーズの高い医薬品の開発の積極的な支援
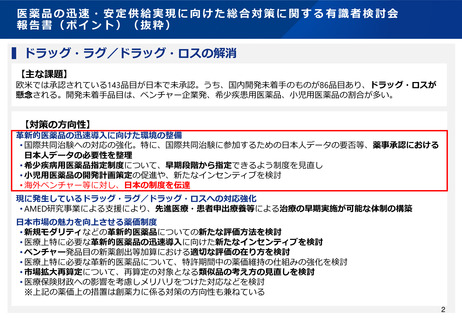
④ 海外開発先行の革新的医薬品について日本での開発・導入に着手しやすくなる環境の整備と情報発信の強化
⑤ パンデミック等に対応できる緊急時相談・審査体制の構築
5.国際化の推進
(3) PMDA の業務内容・実績の世界への発信
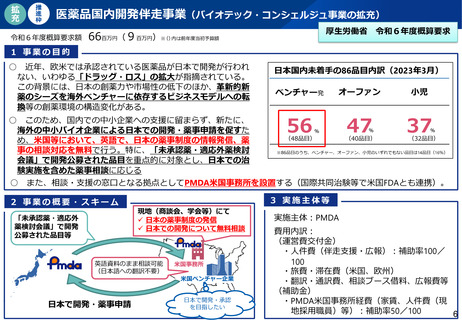
① PMDA 米国拠点の設置等を通じ、海外のベンチャー企業等に対する我が国の薬事制度に関する情報発信を強化
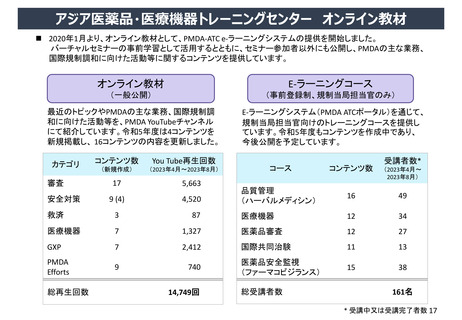
② 審査報告書の英訳版の作成強化、レギュラトリーサイエンスセンター等の活動内容の世界への発信
③ 日本の薬事行政に関する取組等について、実績や経験等に係る積極的・効果的な周知を展開
出典:令和5年度第2回運営評議会資料
5
・PMDAは、厚生労働省が5年毎に作成する中期目標に従って中期計画を作成、独立行政法人評価委員会において毎年実績を評価・公表
されている。
・令和6年度から次期中期計画が始まる予定。
【次期中期計画の方向性】(抜粋)
2.審査等業務
(1) 医薬品審査業務の迅速かつ的確な実施
① 世界最速レベルの審査期間の堅持と効率的で質の高い審査
② Early consideration の発信や最新の科学的知見に基づく臨床評価ガイドラインの策定などイノベーションに的確に
対応した相談及び審査の実施
* Early consideration とは、情報等が十分に収集されていない段階ではある ものの、イノベーションの実用化と革新的な医薬品等の開発促進
の参考情報として、その時点における開発の方向性に係る審査側の考え方を示したもの。
③ 希少疾病用医薬品、小児用医薬品など患者ニーズの高い医薬品の開発の積極的な支援
④ 海外開発先行の革新的医薬品について日本での開発・導入に着手しやすくなる環境の整備と情報発信の強化
⑤ パンデミック等に対応できる緊急時相談・審査体制の構築
5.国際化の推進
(3) PMDA の業務内容・実績の世界への発信
① PMDA 米国拠点の設置等を通じ、海外のベンチャー企業等に対する我が国の薬事制度に関する情報発信を強化
② 審査報告書の英訳版の作成強化、レギュラトリーサイエンスセンター等の活動内容の世界への発信
③ 日本の薬事行政に関する取組等について、実績や経験等に係る積極的・効果的な周知を展開
出典:令和5年度第2回運営評議会資料
5