よむ、つかう、まなぶ。
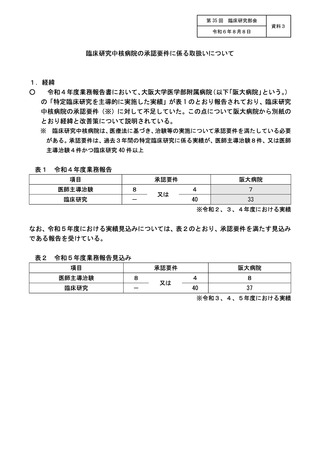
資料3:臨床研究中核病院の承認要件に係る取扱いについて (12 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_42147.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第35回 8/8)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
(別紙)
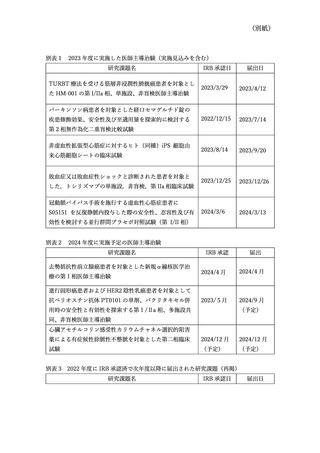
別表1 2023 年度に実施した医師主導治験(実施見込みを含む)
研究課題名
TURBT 療法を受ける筋層非浸潤性膀胱癌患者を対象とし
IRB 承認日
届出日
2023/3/29
2023/4/12
2022/12/15
2023/7/14
2023/8/14
2023/9/20
2023/12/25
2023/12/26
2024/3/6
2024/3/13
た HM-001 の第 I/IIa 相、単施設、非盲検医師主導治験
パーキンソン病患者を対象とした経口セマグルチド錠の
疾患修飾効果、安全性及び至適用量を探索的に検討する
第 2 相無作為化二重盲検比較試験
非虚血性拡張型心筋症に対するヒト(同種)iPS 細胞由
来心筋細胞シートの臨床試験
敗血症又は敗血症性ショックと診断された患者を対象と
した,トシリズマブの単施設,非盲検,第 IIa 相臨床試験
冠動脈バイパス手術を施行する虚血性心筋症患者に
S05151 を反復静脈内投与した際の安全性、忍容性及び有
効性を検討する並行群間プラセボ対照試験(第 I/II 相)
別表2 2024 年度に実施予定の医師主導治験
研究課題名
去勢抵抗性前立腺癌患者を対象とした新規α線核医学治
療の第Ⅰ相医師主導治験
IRB 承認
届出
2024/4 月
2024/4 月
2023/5月
2024/9 月
進行固形癌患者および HER2 陰性乳癌患者を対象として
抗ペリオスチン抗体 PT0101 の単剤、パクリタキセル併
用時の安全性と有効性を探索する第Ⅰ/Ⅱa 相、多施設共
(予定)
同、非盲検医師主導治験
心臓アセチルコリン感受性カリウムチャネル選択的阻害
薬による有症候性徐脈性不整脈を対象とした第二相臨床
2024/12 月
2024/12 月
試験
(予定)
(予定)
別表 3 2022 年度に IRB 承認済で次年度以降に届出された研究課題(再掲)
研究課題名
IRB 承認日
届出日
12
別表1 2023 年度に実施した医師主導治験(実施見込みを含む)
研究課題名
TURBT 療法を受ける筋層非浸潤性膀胱癌患者を対象とし
IRB 承認日
届出日
2023/3/29
2023/4/12
2022/12/15
2023/7/14
2023/8/14
2023/9/20
2023/12/25
2023/12/26
2024/3/6
2024/3/13
た HM-001 の第 I/IIa 相、単施設、非盲検医師主導治験
パーキンソン病患者を対象とした経口セマグルチド錠の
疾患修飾効果、安全性及び至適用量を探索的に検討する
第 2 相無作為化二重盲検比較試験
非虚血性拡張型心筋症に対するヒト(同種)iPS 細胞由
来心筋細胞シートの臨床試験
敗血症又は敗血症性ショックと診断された患者を対象と
した,トシリズマブの単施設,非盲検,第 IIa 相臨床試験
冠動脈バイパス手術を施行する虚血性心筋症患者に
S05151 を反復静脈内投与した際の安全性、忍容性及び有
効性を検討する並行群間プラセボ対照試験(第 I/II 相)
別表2 2024 年度に実施予定の医師主導治験
研究課題名
去勢抵抗性前立腺癌患者を対象とした新規α線核医学治
療の第Ⅰ相医師主導治験
IRB 承認
届出
2024/4 月
2024/4 月
2023/5月
2024/9 月
進行固形癌患者および HER2 陰性乳癌患者を対象として
抗ペリオスチン抗体 PT0101 の単剤、パクリタキセル併
用時の安全性と有効性を探索する第Ⅰ/Ⅱa 相、多施設共
(予定)
同、非盲検医師主導治験
心臓アセチルコリン感受性カリウムチャネル選択的阻害
薬による有症候性徐脈性不整脈を対象とした第二相臨床
2024/12 月
2024/12 月
試験
(予定)
(予定)
別表 3 2022 年度に IRB 承認済で次年度以降に届出された研究課題(再掲)
研究課題名
IRB 承認日
届出日
12