よむ、つかう、まなぶ。
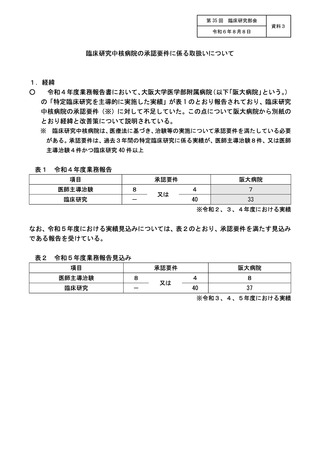
資料3:臨床研究中核病院の承認要件に係る取扱いについて (14 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_42147.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第35回 8/8)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
(別紙)
知財、非臨床の情報提
B440 ビフィズス菌を用い
供・助言、特許出願支
た経口癌ワクチン/尿路上
皮がん
2022/10/31
医薬品
1
【PI が他機関所属のため
トマネジメント
次世代バイオロジクスと
開発戦略助言、薬事(非
しての治療ワクチンの開
【開発者は本学所属であ
OUVC を通じた出資、企
業連携支援、プロジェク
神戸大で実施】
発(P2)
援、GMP 製剤の製造、
臨床、臨床)に関する助
2023/9/1
医薬品
2
言、プロトコル策定の助
言及びレビュー、プロジ
るが専門医のいる機関で
ェクトマネジメント
実施】
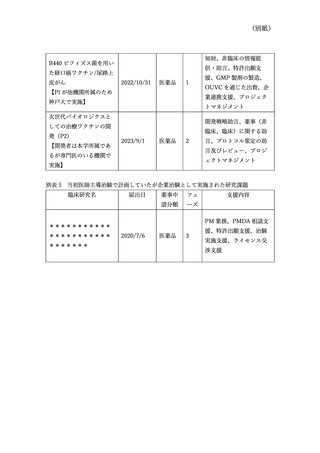
別表 5 当初医師主導治験で計画していたが企業治験として実施された研究課題
臨床研究名
届出日
薬事申
フェ
請分類
ーズ
PM 業務、PMDA 相談支
***********
***********
*******
支援内容
2020/7/6
医薬品
3
援、特許出願支援、治験
実施支援、ライセンス交
渉支援
14
知財、非臨床の情報提
B440 ビフィズス菌を用い
供・助言、特許出願支
た経口癌ワクチン/尿路上
皮がん
2022/10/31
医薬品
1
【PI が他機関所属のため
トマネジメント
次世代バイオロジクスと
開発戦略助言、薬事(非
しての治療ワクチンの開
【開発者は本学所属であ
OUVC を通じた出資、企
業連携支援、プロジェク
神戸大で実施】
発(P2)
援、GMP 製剤の製造、
臨床、臨床)に関する助
2023/9/1
医薬品
2
言、プロトコル策定の助
言及びレビュー、プロジ
るが専門医のいる機関で
ェクトマネジメント
実施】
別表 5 当初医師主導治験で計画していたが企業治験として実施された研究課題
臨床研究名
届出日
薬事申
フェ
請分類
ーズ
PM 業務、PMDA 相談支
***********
***********
*******
支援内容
2020/7/6
医薬品
3
援、特許出願支援、治験
実施支援、ライセンス交
渉支援
14