よむ、つかう、まなぶ。
総-4-1○最適使用推進ガイドラインについて (12 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000212500_00160.html |
| 出典情報 | 中央社会保険医療協議会 総会(第528回 9/14)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
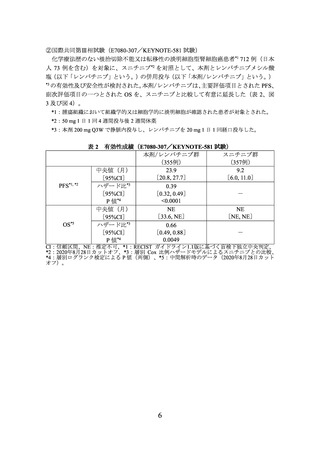
②国際共同第Ⅲ相試験(E7080-307/KEYNOTE-581 試験)
有害事象は本剤/レンバチニブ群 351/352 例(99.7%)及びスニチニブ群 335/340 例
(98.5%)に認められ、治験薬との因果関係が否定できない有害事象は、それぞれ 341/352
例(96.9%)及び 313/340 例(92.1%)に認められた。いずれかの群で発現率が 5%以上
の副作用は下表のとおりであった。
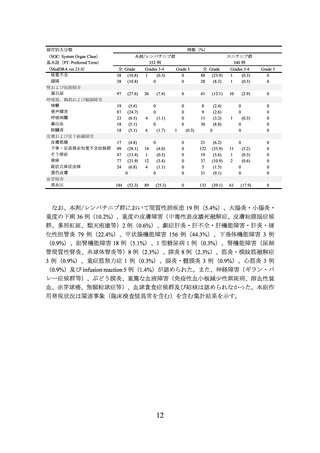
表 5 いずれかの群で発現率が 5%以上の副作用(E7080-307/KEYNOTE-581 試験)
(安全性解析対象集団)
器官別大分類
例数(%)
(SOC: System Organ Class)
基本語(PT: Preferred Term)
(MedDRA ver.23.0)
全副作用
本剤/レンバチニブ群
352 例
全 Grade
341
血液およびリンパ系障害
貧血
20
白血球減少症
4
好中球減少症
8
血小板減少症
13
内分泌障害
甲状腺機能亢進症
22
甲状腺機能低下症
150
胃腸障害
腹痛
39
便秘
24
下痢
192
口内乾燥
28
消化不良
26
胃食道逆流性疾患
8
悪心
94
口内炎
113
嘔吐
56
一般・全身障害および投与部位の状態
無力症
71
疲労
113
末梢性浮腫
17
発熱
16
臨床検査
ALT 増加
34
アミラーゼ増加
53
AST 増加
33
血中クレアチニン増加
23
血中甲状腺刺激ホルモン増加
38
リパーゼ増加
50
好中球数減少
8
血小板数減少
20
体重減少
70
白血球数減少
10
代謝および栄養障害
食欲減退
123
高コレステロール血症
18
高トリグリセリド血症
30
筋骨格系および結合組織障害
関節痛
60
筋肉痛
38
神経系障害
Grades 3-4
(96.9)
252
(5.7)
(1.1)
(2.3)
(3.7)
3
Grade 5
4
Grades 3-4
Grade 5
(92.1)
200
(58.8)
0
(0.3)
(0.3)
0
0
0
0
44
21
42
51
(12.9)
(6.2)
(12.4)
(15.0)
11
7
18
18
(3.2)
(2.1)
(5.3)
(5.3)
0
0
0
0
4
(1.1)
0
0
8
79
(2.4)
(23.2)
(11.1)
(6.8)
(54.5)
(8.0)
(7.4)
(2.3)
(26.7)
(32.1)
(15.9)
4
1
29
(1.1)
(0.3)
(8.2)
6
6
5
(1.7)
(1.7)
(1.4)
0
0
0
0
0
0
0
0
0
12
20
151
10
42
26
94
127
45
(3.5)
(5.9)
(44.4)
(2.9)
(12.4)
(7.6)
(27.6)
(37.4)
(13.2)
(20.2)
(32.1)
(4.8)
(4.5)
16
11
1
(4.5)
(3.1)
(0.3)
0
0
0
0
54
109
17
18
(9.7)
(15.1)
(9.4)
(6.5)
(10.8)
(14.2)
(2.3)
(5.7)
(19.9)
(2.8)
11
26
9
1
0
0
0
34
6
3
21
1
(34.9)
(5.1)
(8.5)
(17.0)
(10.8)
(0.9)
0
1
1
0
0
0
0
(1.1)
全 Grade
313
(6.3)
(42.6)
(71.6)
スニチニブ群
340 例
0
0
1
0
0
(0.3)
0
15
(4.4)
0
0
0
2
7
3
(0.6)
(2.1)
(0.9)
(15.9)
(32.1)
(5.0)
(5.3)
11
13
(3.2)
(3.8)
1
(0.3)
(1.8)
(2.6)
(0.6)
(9.7)
(1.7)
(0.9)
(6.0)
(0.3)
(8.8)
(7.6)
(8.8)
(5.0)
(5.0)
(10.0)
(11.5)
(16.8)
(5.6)
(8.8)
6
9
2
0
0
0
0
0
0
30
26
30
17
17
34
39
57
19
30
12
1
10
(3.4)
(0.3)
(2.8)
0
0
0
84
2
23
(24.7)
(0.6)
(6.8)
4
3
(1.1)
(0.9)
0
0
22
8
(6.5)
(2.4)
0
(3.1)
(7.4)
(2.6)
(0.3)
0
11
1
(0.3)
0
0
0
0
0
0
0
0
0
0
0
0
0
0
6
(1.8)
0
0
0
0
0
0
0
0
0
0
5
1
14
(1.5)
(0.3)
(4.1)
0
0
0
0
0
24
19
18
(7.1)
(5.6)
(5.3)
0
0
0
0
0
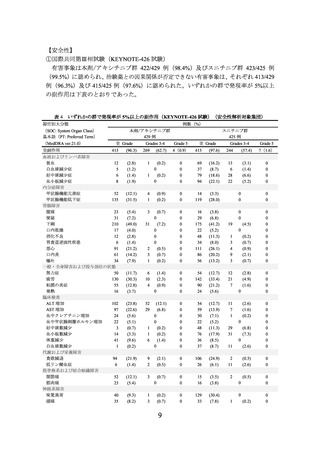
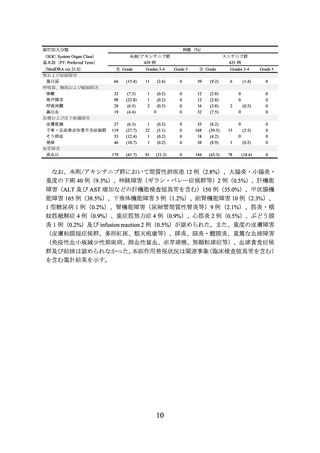
有害事象は本剤/レンバチニブ群 351/352 例(99.7%)及びスニチニブ群 335/340 例
(98.5%)に認められ、治験薬との因果関係が否定できない有害事象は、それぞれ 341/352
例(96.9%)及び 313/340 例(92.1%)に認められた。いずれかの群で発現率が 5%以上
の副作用は下表のとおりであった。
表 5 いずれかの群で発現率が 5%以上の副作用(E7080-307/KEYNOTE-581 試験)
(安全性解析対象集団)
器官別大分類
例数(%)
(SOC: System Organ Class)
基本語(PT: Preferred Term)
(MedDRA ver.23.0)
全副作用
本剤/レンバチニブ群
352 例
全 Grade
341
血液およびリンパ系障害
貧血
20
白血球減少症
4
好中球減少症
8
血小板減少症
13
内分泌障害
甲状腺機能亢進症
22
甲状腺機能低下症
150
胃腸障害
腹痛
39
便秘
24
下痢
192
口内乾燥
28
消化不良
26
胃食道逆流性疾患
8
悪心
94
口内炎
113
嘔吐
56
一般・全身障害および投与部位の状態
無力症
71
疲労
113
末梢性浮腫
17
発熱
16
臨床検査
ALT 増加
34
アミラーゼ増加
53
AST 増加
33
血中クレアチニン増加
23
血中甲状腺刺激ホルモン増加
38
リパーゼ増加
50
好中球数減少
8
血小板数減少
20
体重減少
70
白血球数減少
10
代謝および栄養障害
食欲減退
123
高コレステロール血症
18
高トリグリセリド血症
30
筋骨格系および結合組織障害
関節痛
60
筋肉痛
38
神経系障害
Grades 3-4
(96.9)
252
(5.7)
(1.1)
(2.3)
(3.7)
3
Grade 5
4
Grades 3-4
Grade 5
(92.1)
200
(58.8)
0
(0.3)
(0.3)
0
0
0
0
44
21
42
51
(12.9)
(6.2)
(12.4)
(15.0)
11
7
18
18
(3.2)
(2.1)
(5.3)
(5.3)
0
0
0
0
4
(1.1)
0
0
8
79
(2.4)
(23.2)
(11.1)
(6.8)
(54.5)
(8.0)
(7.4)
(2.3)
(26.7)
(32.1)
(15.9)
4
1
29
(1.1)
(0.3)
(8.2)
6
6
5
(1.7)
(1.7)
(1.4)
0
0
0
0
0
0
0
0
0
12
20
151
10
42
26
94
127
45
(3.5)
(5.9)
(44.4)
(2.9)
(12.4)
(7.6)
(27.6)
(37.4)
(13.2)
(20.2)
(32.1)
(4.8)
(4.5)
16
11
1
(4.5)
(3.1)
(0.3)
0
0
0
0
54
109
17
18
(9.7)
(15.1)
(9.4)
(6.5)
(10.8)
(14.2)
(2.3)
(5.7)
(19.9)
(2.8)
11
26
9
1
0
0
0
34
6
3
21
1
(34.9)
(5.1)
(8.5)
(17.0)
(10.8)
(0.9)
0
1
1
0
0
0
0
(1.1)
全 Grade
313
(6.3)
(42.6)
(71.6)
スニチニブ群
340 例
0
0
1
0
0
(0.3)
0
15
(4.4)
0
0
0
2
7
3
(0.6)
(2.1)
(0.9)
(15.9)
(32.1)
(5.0)
(5.3)
11
13
(3.2)
(3.8)
1
(0.3)
(1.8)
(2.6)
(0.6)
(9.7)
(1.7)
(0.9)
(6.0)
(0.3)
(8.8)
(7.6)
(8.8)
(5.0)
(5.0)
(10.0)
(11.5)
(16.8)
(5.6)
(8.8)
6
9
2
0
0
0
0
0
0
30
26
30
17
17
34
39
57
19
30
12
1
10
(3.4)
(0.3)
(2.8)
0
0
0
84
2
23
(24.7)
(0.6)
(6.8)
4
3
(1.1)
(0.9)
0
0
22
8
(6.5)
(2.4)
0
(3.1)
(7.4)
(2.6)
(0.3)
0
11
1
(0.3)
0
0
0
0
0
0
0
0
0
0
0
0
0
0
6
(1.8)
0
0
0
0
0
0
0
0
0
0
5
1
14
(1.5)
(0.3)
(4.1)
0
0
0
0
0
24
19
18
(7.1)
(5.6)
(5.3)
0
0
0
0
0