よむ、つかう、まなぶ。
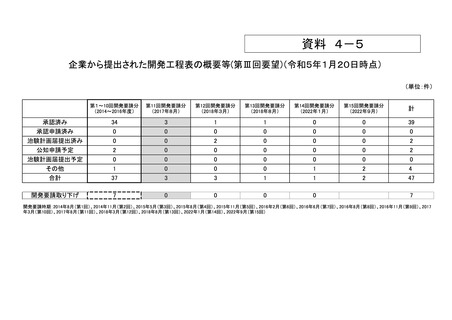
資料4-5 企業から提出された開発工程表の概要等(第III回要望) (8 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00026.html |
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第54回 2/15)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
要望番号
企業名
成分名
販売名
開発内容
承認年月
公知
申請
販売名
開発内容
承認年月
公知
申請
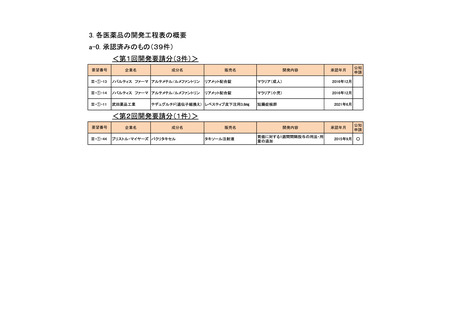
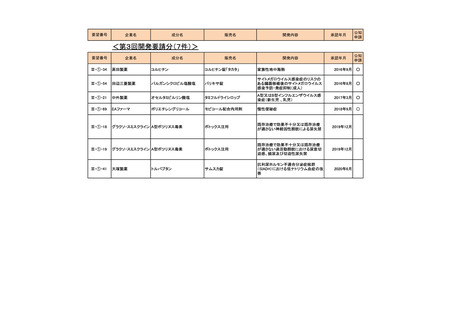
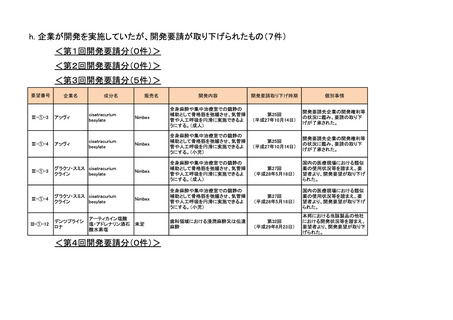
<第6回開発要請分(9件)>
要望番号
企業名
Ⅲ-③-13
CSL ベーリング
乾燥濃縮人 C1-インアクチベー
ベリナートP静注用500
ター
侵襲を伴う処置による遺伝性血管性浮
腫の急性発作の発症抑制
2017年3月
○
Ⅲ-①-74
全薬工業
リツキシマブ(遺伝子組換え)
リツキサン注
慢性特発性血小板減少性紫斑病
2017年6月
○
アセチルコリン塩化物
オビソート注射用
冠攣縮性狭心症が疑われる患者に対
し、診断を確定するために施行する冠
攣縮薬物誘発負荷試験時の冠動脈内
投与
2017年8月
○
オランザピン
ジプレキサ錠、ジプレキサ細
粒、ジプレキサザイディス錠
抗悪性腫瘍剤投与に伴う消化器症状
(悪心、嘔吐)
2017年12月
○
Ⅲ-③-25
共和薬品工業株式会
社
ドブタミン塩酸塩
当該薬剤を投与することにより、心臓の
ドブトレックス注射液
交感神経を刺激し、心筋収縮力を高
ドブトレックスキット点滴静注用 め、潜在的な循環動態異常を顕在化さ
せる
2018年9月
○
Ⅲ-③-10
アスペンジャパン
アザチオプリン
イムラン錠
自己免疫性肝炎
2019年2月
○
Ⅲ-③-10
田辺三菱製薬
アザチオプリン
アザニン錠
自己免疫性肝炎
2019年2月
○
2020年9月
-
Ⅲ-③-24
第一三共
Ⅲ-①-22.1
日本イーライリリー
Ⅲ-①-22.2
成分名
(効能・効果)
てんかん重積状態
Ⅲ-④-3
武田薬品工業
ミダゾラム
ブコラム口腔用液
2.5mg/5mg/7.5mg/10mg
(用法・用量)
ミダゾラムとして、生後3 ヵ月以上1 歳未
満には2.5 mg(生後6 ヵ月以下は医療機
関内での投与に限定)、1 歳以上5 歳未
満には5 mg、5 歳以上10 歳未満には
7.5 mg、10 歳以上18 歳未満には10 mg
を口腔内(歯茎と頬の間)に緩徐に注入
する。なお、必要に応じて、1 回投与量
を半量に分割して口腔内の左右に注入
することもできる。
企業名
成分名
販売名
開発内容
承認年月
公知
申請
販売名
開発内容
承認年月
公知
申請
<第6回開発要請分(9件)>
要望番号
企業名
Ⅲ-③-13
CSL ベーリング
乾燥濃縮人 C1-インアクチベー
ベリナートP静注用500
ター
侵襲を伴う処置による遺伝性血管性浮
腫の急性発作の発症抑制
2017年3月
○
Ⅲ-①-74
全薬工業
リツキシマブ(遺伝子組換え)
リツキサン注
慢性特発性血小板減少性紫斑病
2017年6月
○
アセチルコリン塩化物
オビソート注射用
冠攣縮性狭心症が疑われる患者に対
し、診断を確定するために施行する冠
攣縮薬物誘発負荷試験時の冠動脈内
投与
2017年8月
○
オランザピン
ジプレキサ錠、ジプレキサ細
粒、ジプレキサザイディス錠
抗悪性腫瘍剤投与に伴う消化器症状
(悪心、嘔吐)
2017年12月
○
Ⅲ-③-25
共和薬品工業株式会
社
ドブタミン塩酸塩
当該薬剤を投与することにより、心臓の
ドブトレックス注射液
交感神経を刺激し、心筋収縮力を高
ドブトレックスキット点滴静注用 め、潜在的な循環動態異常を顕在化さ
せる
2018年9月
○
Ⅲ-③-10
アスペンジャパン
アザチオプリン
イムラン錠
自己免疫性肝炎
2019年2月
○
Ⅲ-③-10
田辺三菱製薬
アザチオプリン
アザニン錠
自己免疫性肝炎
2019年2月
○
2020年9月
-
Ⅲ-③-24
第一三共
Ⅲ-①-22.1
日本イーライリリー
Ⅲ-①-22.2
成分名
(効能・効果)
てんかん重積状態
Ⅲ-④-3
武田薬品工業
ミダゾラム
ブコラム口腔用液
2.5mg/5mg/7.5mg/10mg
(用法・用量)
ミダゾラムとして、生後3 ヵ月以上1 歳未
満には2.5 mg(生後6 ヵ月以下は医療機
関内での投与に限定)、1 歳以上5 歳未
満には5 mg、5 歳以上10 歳未満には
7.5 mg、10 歳以上18 歳未満には10 mg
を口腔内(歯茎と頬の間)に緩徐に注入
する。なお、必要に応じて、1 回投与量
を半量に分割して口腔内の左右に注入
することもできる。