よむ、つかう、まなぶ。
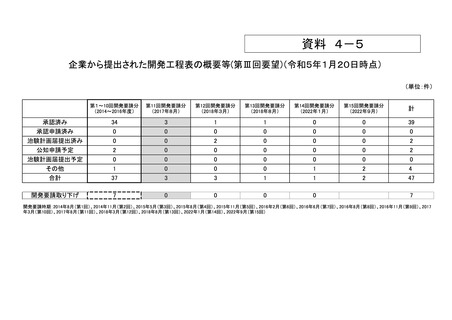
資料4-5 企業から提出された開発工程表の概要等(第III回要望) (9 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00026.html |
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第54回 2/15)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
要望番号
Ⅲ-③-23
企業名
日本歯科薬品
成分名
メピバカイン塩酸塩
販売名
スキャンドネストカートリッジ
3%
開発内容
歯科領域における伝達麻酔
承認年月
2022年12月
公知
申請
○
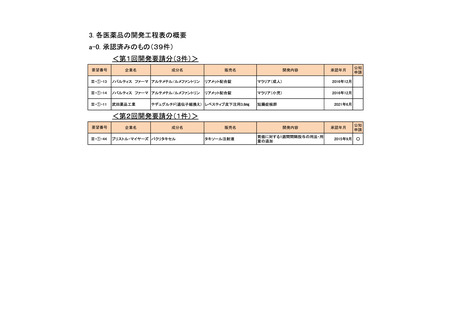
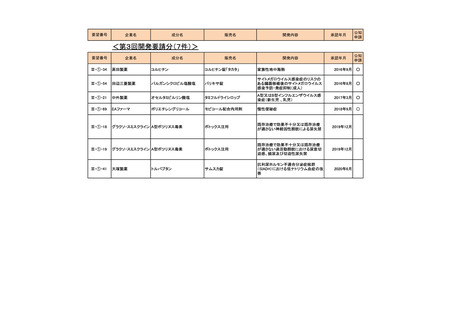
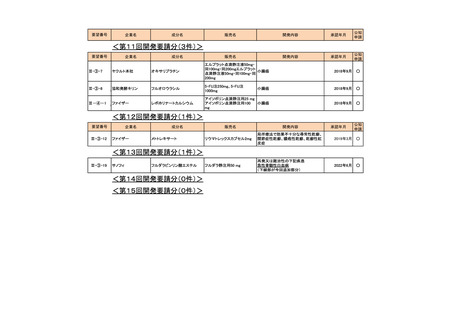
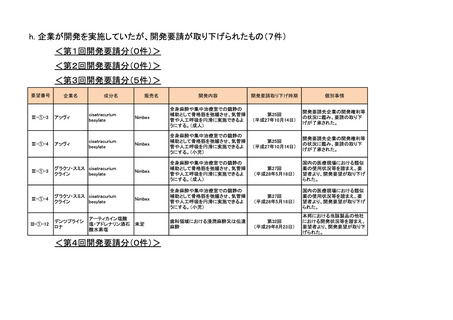
<第7回開発要請分(3件)>
要望番号
企業名
成分名
販売名
開発内容
承認年月
公知
申請
III-③-1.1
III-③-1.2
ヤンセンファーマ
ボルテゾミブ
ベルケイド注射用
原発性マクログロブリン血症/リンパ形
質細胞リンパ腫
2018年3月
○
III-③-11
III-③-26
第一三共
インドシアニングリーン
ジアグノグリーン注射用
血管及び組織の血流評価
2018年7月
○
Ⅲ-①-80
あすか製薬
レボチロキシンナトリウム
チラーヂンS静注液200μg
粘液水腫性昏睡、重症甲状腺機能低下
症
2020年1月
開発内容
承認年月
<第8回開発要請分(1件)>
要望番号
Ⅲ-④-4
企業名
成分名
ギリアド・サイエンシズ ソホスブビル
販売名
ソバルディ錠
次のいずれかのC型慢性肝炎又はC型
代償性肝硬変におけるウイルス血症の
改善
1.セログループ2(ジェノタイプ2)の患者
2. セログループ1(ジェノタイプ1)又はセ
ログループ2(ジェノタイプ2)のいずれに
も該当しない患者
(下線部が今回追加部分)
公知
申請
2017年3月
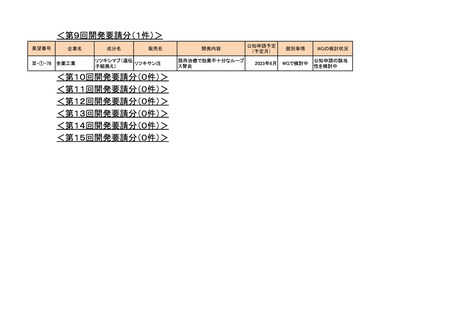
<第9回開発要請分(2件)>
要望番号
III-④-19
企業名
日本メジフィジックス
Ⅲ-①-72
Ⅲ-①-72.2 帝人ファーマ
Ⅲ-①-72.3
成分名
販売名
開発内容
フルデオキシグルコース(18F)
FDGスキャン注
大型血管炎の診断における炎症部位の
可視化
ランレオチド酢酸塩
ソマチュリン皮下注
甲状腺刺激ホルモン産生下垂体腫瘍
<第10回開発要請分(2件)>
承認年月
公知
申請
2018年2月
○
2020年12月
-
Ⅲ-③-23
企業名
日本歯科薬品
成分名
メピバカイン塩酸塩
販売名
スキャンドネストカートリッジ
3%
開発内容
歯科領域における伝達麻酔
承認年月
2022年12月
公知
申請
○
<第7回開発要請分(3件)>
要望番号
企業名
成分名
販売名
開発内容
承認年月
公知
申請
III-③-1.1
III-③-1.2
ヤンセンファーマ
ボルテゾミブ
ベルケイド注射用
原発性マクログロブリン血症/リンパ形
質細胞リンパ腫
2018年3月
○
III-③-11
III-③-26
第一三共
インドシアニングリーン
ジアグノグリーン注射用
血管及び組織の血流評価
2018年7月
○
Ⅲ-①-80
あすか製薬
レボチロキシンナトリウム
チラーヂンS静注液200μg
粘液水腫性昏睡、重症甲状腺機能低下
症
2020年1月
開発内容
承認年月
<第8回開発要請分(1件)>
要望番号
Ⅲ-④-4
企業名
成分名
ギリアド・サイエンシズ ソホスブビル
販売名
ソバルディ錠
次のいずれかのC型慢性肝炎又はC型
代償性肝硬変におけるウイルス血症の
改善
1.セログループ2(ジェノタイプ2)の患者
2. セログループ1(ジェノタイプ1)又はセ
ログループ2(ジェノタイプ2)のいずれに
も該当しない患者
(下線部が今回追加部分)
公知
申請
2017年3月
<第9回開発要請分(2件)>
要望番号
III-④-19
企業名
日本メジフィジックス
Ⅲ-①-72
Ⅲ-①-72.2 帝人ファーマ
Ⅲ-①-72.3
成分名
販売名
開発内容
フルデオキシグルコース(18F)
FDGスキャン注
大型血管炎の診断における炎症部位の
可視化
ランレオチド酢酸塩
ソマチュリン皮下注
甲状腺刺激ホルモン産生下垂体腫瘍
<第10回開発要請分(2件)>
承認年月
公知
申請
2018年2月
○
2020年12月
-