よむ、つかう、まなぶ。
資料1-6 副反応疑い報告の状況について (4 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000208910_00059.html |
| 出典情報 | 第92回厚生科学審議会予防接種・ワクチン分科会副反応検討部会、令和4年度第27回薬事・食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会(合同開催)(3/10)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
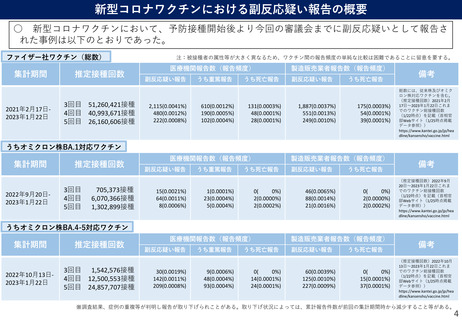
新型コロナワクチンにおける副反応疑い報告の概要
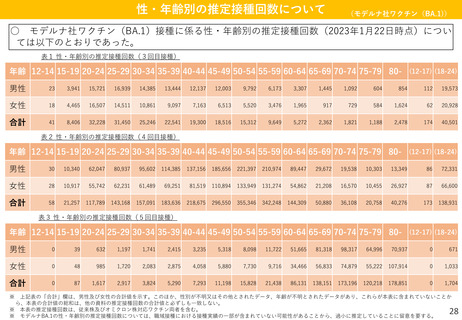
○ 新型コロナワクチンにおいて、予防接種開始後より今回の審議会までに副反応疑いとして報告さ
れた事例は以下のとおりであった。
ファイザー社ワクチン(総数)
集計期間
2021年2月17日2023年1月22日
推定接種回数
3回目 51,260,421接種
4回目 40,993,671接種
5回目 26,160,606接種
注:被接種者の属性等が大きく異なるため、ワクチン間の報告頻度の単純な比較は困難であることに留意を要する。
医療機関報告数(報告頻度)
副反応疑い報告
2,115(0.0041%)
480(0.0012%)
222(0.0008%)
うち重篤報告
610(0.0012%)
190(0.0005%)
102(0.0004%)
うち死亡報告
131(0.0003%)
48(0.0001%)
28(0.0001%)
製造販売業者報告数(報告頻度)
副反応疑い報告
1,887(0.0037%)
551(0.0013%)
249(0.0010%)
うち死亡報告
175(0.0003%)
54(0.0001%)
39(0.0001%)
備考
総数には、従来株及びオミク
ロン株対応ワクチンを含む。
(推定接種回数)2021年2月
17日~2023年1月22日これま
でのワクチン総接種回数
(1/22時点)を記載(首相官
邸Webサイト(1/25時点掲載
データ参照))
https://www.kantei.go.jp/jp/hea
dline/kansensho/vaccine.html
うちオミクロン株BA.1対応ワクチン
集計期間
2022年9月20日2023年1月22日
推定接種回数
3回目
4回目
5回目
705,373接種
6,070,366接種
1,302,899接種
医療機関報告数(報告頻度)
副反応疑い報告
15(0.0021%)
64(0.0011%)
8(0.0006%)
うち重篤報告
1(0.0001%)
23(0.0004%)
5(0.0004%)
うち死亡報告
0(
0%)
2(0.0000%)
2(0.0002%)
製造販売業者報告数(報告頻度)
副反応疑い報告
46(0.0065%)
88(0.0014%)
21(0.0016%)
うち死亡報告
0(
0%)
2(0.0000%)
2(0.0002%)
備考
(推定接種回数)2022年9月
20日~2023年1月22日これま
でのワクチン総接種回数
(1/22時点)を記載(首相官
邸Webサイト(1/25時点掲載
データ参照))
https://www.kantei.go.jp/jp/hea
dline/kansensho/vaccine.html
うちオミクロン株BA.4-5対応ワクチン
集計期間
2022年10月13日2023年1月22日
推定接種回数
3回目 1,542,576接種
4回目 12,500,553接種
5回目 24,857,707接種
医療機関報告数(報告頻度)
副反応疑い報告
30(0.0019%)
142(0.0011%)
209(0.0008%)
うち重篤報告
9(0.0006%)
48(0.0004%)
93(0.0004%)
うち死亡報告
0(
0%)
14(0.0001%)
24(0.0001%)
製造販売業者報告数(報告頻度)
副反応疑い報告
60(0.0039%)
125(0.0010%)
227(0.0009%)
うち死亡報告
0(
0%)
15(0.0001%)
37(0.0001%)
備考
(推定接種回数)2022年10月
13日~2023年1月22日これま
でのワクチン総接種回数
(1/22時点)を記載(首相官
邸Webサイト(1/25時点掲載
データ参照))
https://www.kantei.go.jp/jp/hea
dline/kansensho/vaccine.html
※調査結果、症例の重複等が判明し報告が取り下げられことがある。取り下げ状況によっては、累計報告件数が前回の集計期間時から減少すること等がある。
4
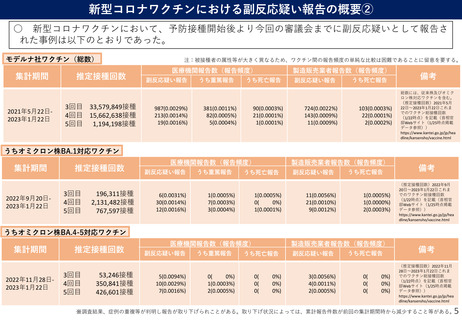
○ 新型コロナワクチンにおいて、予防接種開始後より今回の審議会までに副反応疑いとして報告さ
れた事例は以下のとおりであった。
ファイザー社ワクチン(総数)
集計期間
2021年2月17日2023年1月22日
推定接種回数
3回目 51,260,421接種
4回目 40,993,671接種
5回目 26,160,606接種
注:被接種者の属性等が大きく異なるため、ワクチン間の報告頻度の単純な比較は困難であることに留意を要する。
医療機関報告数(報告頻度)
副反応疑い報告
2,115(0.0041%)
480(0.0012%)
222(0.0008%)
うち重篤報告
610(0.0012%)
190(0.0005%)
102(0.0004%)
うち死亡報告
131(0.0003%)
48(0.0001%)
28(0.0001%)
製造販売業者報告数(報告頻度)
副反応疑い報告
1,887(0.0037%)
551(0.0013%)
249(0.0010%)
うち死亡報告
175(0.0003%)
54(0.0001%)
39(0.0001%)
備考
総数には、従来株及びオミク
ロン株対応ワクチンを含む。
(推定接種回数)2021年2月
17日~2023年1月22日これま
でのワクチン総接種回数
(1/22時点)を記載(首相官
邸Webサイト(1/25時点掲載
データ参照))
https://www.kantei.go.jp/jp/hea
dline/kansensho/vaccine.html
うちオミクロン株BA.1対応ワクチン
集計期間
2022年9月20日2023年1月22日
推定接種回数
3回目
4回目
5回目
705,373接種
6,070,366接種
1,302,899接種
医療機関報告数(報告頻度)
副反応疑い報告
15(0.0021%)
64(0.0011%)
8(0.0006%)
うち重篤報告
1(0.0001%)
23(0.0004%)
5(0.0004%)
うち死亡報告
0(
0%)
2(0.0000%)
2(0.0002%)
製造販売業者報告数(報告頻度)
副反応疑い報告
46(0.0065%)
88(0.0014%)
21(0.0016%)
うち死亡報告
0(
0%)
2(0.0000%)
2(0.0002%)
備考
(推定接種回数)2022年9月
20日~2023年1月22日これま
でのワクチン総接種回数
(1/22時点)を記載(首相官
邸Webサイト(1/25時点掲載
データ参照))
https://www.kantei.go.jp/jp/hea
dline/kansensho/vaccine.html
うちオミクロン株BA.4-5対応ワクチン
集計期間
2022年10月13日2023年1月22日
推定接種回数
3回目 1,542,576接種
4回目 12,500,553接種
5回目 24,857,707接種
医療機関報告数(報告頻度)
副反応疑い報告
30(0.0019%)
142(0.0011%)
209(0.0008%)
うち重篤報告
9(0.0006%)
48(0.0004%)
93(0.0004%)
うち死亡報告
0(
0%)
14(0.0001%)
24(0.0001%)
製造販売業者報告数(報告頻度)
副反応疑い報告
60(0.0039%)
125(0.0010%)
227(0.0009%)
うち死亡報告
0(
0%)
15(0.0001%)
37(0.0001%)
備考
(推定接種回数)2022年10月
13日~2023年1月22日これま
でのワクチン総接種回数
(1/22時点)を記載(首相官
邸Webサイト(1/25時点掲載
データ参照))
https://www.kantei.go.jp/jp/hea
dline/kansensho/vaccine.html
※調査結果、症例の重複等が判明し報告が取り下げられことがある。取り下げ状況によっては、累計報告件数が前回の集計期間時から減少すること等がある。
4