よむ、つかう、まなぶ。
【参考資料6】国際共同治験に参加する場合の日本人第1相試験の必要性について(第2回検討会 資料1) (18 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_35181.html |
| 出典情報 | 創薬力の強化・安定供給の確保等のための薬事規制のあり方に関する検討会(第3回 9/13)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
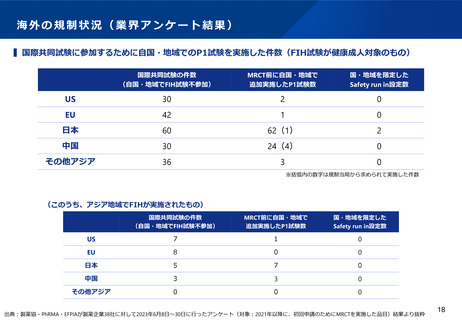
海外の規制状況(業界アンケート結果)
▍国際共同試験に参加するために自国・地域でのP1試験を実施した件数(FIH試験が健康成人対象のもの)
国際共同試験の件数
(自国・地域でFIH試験不参加)
MRCT前に自国・地域で
追加実施したP1試験数
国・地域を限定した
Safety run in設定数
US
30
2
0
EU
42
1
0
日本
60
62(1)
2
中国
30
24(4)
0
その他アジア
36
3
0
※括弧内の数字は規制当局から求められて実施した件数
(このうち、アジア地域でFIHが実施されたもの)
国際共同試験の件数
(自国・地域でFIH試験不参加)
MRCT前に自国・地域で
追加実施したP1試験数
国・地域を限定した
Safety run in設定数
US
7
1
0
EU
8
0
0
日本
5
7
0
中国
3
3
0
その他アジア
0
0
0
出典:製薬協・PhRMA・EFPIAが製薬企業38社に対して2023年6月8日~30日に行ったアンケート(対象:2021年以降に、初回申請のためにMRCTを実施した品目)結果より抜粋
18
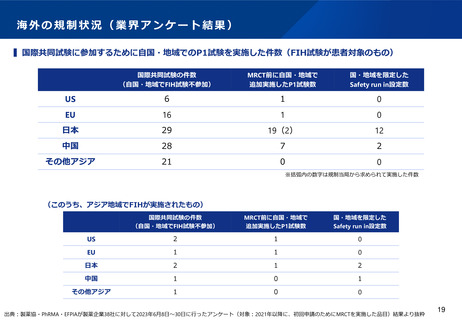
▍国際共同試験に参加するために自国・地域でのP1試験を実施した件数(FIH試験が健康成人対象のもの)
国際共同試験の件数
(自国・地域でFIH試験不参加)
MRCT前に自国・地域で
追加実施したP1試験数
国・地域を限定した
Safety run in設定数
US
30
2
0
EU
42
1
0
日本
60
62(1)
2
中国
30
24(4)
0
その他アジア
36
3
0
※括弧内の数字は規制当局から求められて実施した件数
(このうち、アジア地域でFIHが実施されたもの)
国際共同試験の件数
(自国・地域でFIH試験不参加)
MRCT前に自国・地域で
追加実施したP1試験数
国・地域を限定した
Safety run in設定数
US
7
1
0
EU
8
0
0
日本
5
7
0
中国
3
3
0
その他アジア
0
0
0
出典:製薬協・PhRMA・EFPIAが製薬企業38社に対して2023年6月8日~30日に行ったアンケート(対象:2021年以降に、初回申請のためにMRCTを実施した品目)結果より抜粋
18