よむ、つかう、まなぶ。
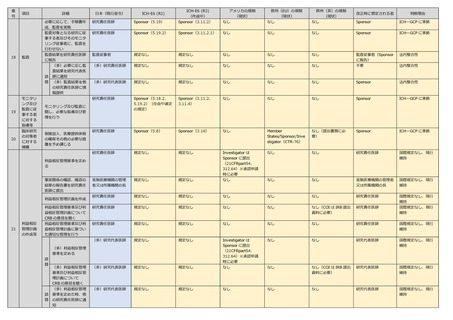
参考資料1:令和5年度厚生労働科学特別研究事業(沖田班)総括研究 報告書一部抜粋 (5 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_42147.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第35回 8/8)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
番
号
27
項目
個人情報
の取扱い
28
本人等の
同意
36
試料等に
係る個人
情報の保
護に関す
る措
37
39
記録の作
成
実施計画
の提出
原則に記載(2.11)
(プライバシーと秘密
の保全に配慮して保
護)
ICH-E6 (R3)
(作成中)
原則(1.6)(プライ
バシー及びデータ保護
要件に従って保護)
Investigator
(2.12.7)
Sponsor(3.16.1)
アメリカの規制
(現状)
なし
欧州(EU)の規制
(現状)
実施要件として記載
(責任者なし)(EU
CTR-28)
(95/46/EC)
欧州(英)の規制
(現状)
実施要件として記載
(責任者なし)
(2004/1031)
従事する者及び実施
医療機関の管理者
規定なし
規定なし
なし
なし
あらかじめ、本人又はそ
の配偶者、親権を行う
者、後見人その他これら
に準ずる者から同意を受
けている範囲又は通知
し、若しくは公表してい
る範囲を超えて、臨床研
究の実施に伴い取得した
個人情報を取り扱っては
ならない
個人情報の利用の目的の
達成に必要な範囲内にお
いて、個人情報を正確か
つ最新の内容に保つ
従事する者
規定なし
規定なし
なし
研究責任医師
規定なし
規定なし
個人情報を利用して臨床
研究を実施する場合にお
いては、本人等の同意を
得る
(多)他の研究責任医師
に対し試料等を提供する
場合にあっては、個人情
報の保護の観点から、個
人情報の全部又は一部を
削除するための措置をと
るよう努める
研究責任医師
Investigator(4.8)
(個人情報に係る特別
な規定はない)
研究責任医師
外国にある者と共同して
臨床研究を実施する場合
であって、外国にある者
に個人情報を含む試料等
を提供するときは、記録
を作成する
外国にある者から個人情
報を含む試料等の提供を
受ける場合には、確認を
行い記録を作成する
実施計画の新規・変更の
提出は、特定臨床研究を
開始する前に様式第一に
よる計画を提出して行う
詳細
日本(現行省令)
ICH-E6 (R2)
改正時に想定される者
判断理由
個人情報を取り扱うに当
たっては、個情法の規定
によるほか、同法におけ
る個人に関する情報の保
護の措置に準じて、個人
情報の漏えい、滅失又は
毀損の防止その他の個人
情報の適切な管理のため
に必要な措置を講じる
個人情報を取り扱うに当
たっては、前項の規定に
かかわらず、第三項及び
第四項並びに次条から第
三十八条までの規定の定
めるところによる。
従事する者及び実施
医療機関の管理者
従事する者及び実施医
療機関の管理者
国際規定なし、現行
維持
なし
従事する者及び実施医
療機関の管理者
国際規定なし、現行
維持
なし
なし
従事する者
国際規定なし、現行
維持
なし
なし
なし
研究責任医師
国際規定なし、現行
維持
Investigator(2.8)
(個人情報保護に係る
特別な規定はない)
なし
なし
なし
研究責任医師
国際規定なし、現行
維持
規定なし
規定なし
なし
なし
なし
研究責任医師
国際規定なし、現行
維持
研究責任医師
規定なし
規定なし
なし
なし
なし
研究責任医師
国際規定なし、現行
維持
研究責任医師
規定なし
規定なし
なし
なし
なし
研究責任医師
国際規定なし、現行
維持
研究責任医師
Sponsor(5.9)
Sponsor(3.8)
Sponsor(312.20)
Sponsor(EU CTR5)
Sponsor
(2004/1031-17)
Sponsor
ICHーGCP に準拠
号
27
項目
個人情報
の取扱い
28
本人等の
同意
36
試料等に
係る個人
情報の保
護に関す
る措
37
39
記録の作
成
実施計画
の提出
原則に記載(2.11)
(プライバシーと秘密
の保全に配慮して保
護)
ICH-E6 (R3)
(作成中)
原則(1.6)(プライ
バシー及びデータ保護
要件に従って保護)
Investigator
(2.12.7)
Sponsor(3.16.1)
アメリカの規制
(現状)
なし
欧州(EU)の規制
(現状)
実施要件として記載
(責任者なし)(EU
CTR-28)
(95/46/EC)
欧州(英)の規制
(現状)
実施要件として記載
(責任者なし)
(2004/1031)
従事する者及び実施
医療機関の管理者
規定なし
規定なし
なし
なし
あらかじめ、本人又はそ
の配偶者、親権を行う
者、後見人その他これら
に準ずる者から同意を受
けている範囲又は通知
し、若しくは公表してい
る範囲を超えて、臨床研
究の実施に伴い取得した
個人情報を取り扱っては
ならない
個人情報の利用の目的の
達成に必要な範囲内にお
いて、個人情報を正確か
つ最新の内容に保つ
従事する者
規定なし
規定なし
なし
研究責任医師
規定なし
規定なし
個人情報を利用して臨床
研究を実施する場合にお
いては、本人等の同意を
得る
(多)他の研究責任医師
に対し試料等を提供する
場合にあっては、個人情
報の保護の観点から、個
人情報の全部又は一部を
削除するための措置をと
るよう努める
研究責任医師
Investigator(4.8)
(個人情報に係る特別
な規定はない)
研究責任医師
外国にある者と共同して
臨床研究を実施する場合
であって、外国にある者
に個人情報を含む試料等
を提供するときは、記録
を作成する
外国にある者から個人情
報を含む試料等の提供を
受ける場合には、確認を
行い記録を作成する
実施計画の新規・変更の
提出は、特定臨床研究を
開始する前に様式第一に
よる計画を提出して行う
詳細
日本(現行省令)
ICH-E6 (R2)
改正時に想定される者
判断理由
個人情報を取り扱うに当
たっては、個情法の規定
によるほか、同法におけ
る個人に関する情報の保
護の措置に準じて、個人
情報の漏えい、滅失又は
毀損の防止その他の個人
情報の適切な管理のため
に必要な措置を講じる
個人情報を取り扱うに当
たっては、前項の規定に
かかわらず、第三項及び
第四項並びに次条から第
三十八条までの規定の定
めるところによる。
従事する者及び実施
医療機関の管理者
従事する者及び実施医
療機関の管理者
国際規定なし、現行
維持
なし
従事する者及び実施医
療機関の管理者
国際規定なし、現行
維持
なし
なし
従事する者
国際規定なし、現行
維持
なし
なし
なし
研究責任医師
国際規定なし、現行
維持
Investigator(2.8)
(個人情報保護に係る
特別な規定はない)
なし
なし
なし
研究責任医師
国際規定なし、現行
維持
規定なし
規定なし
なし
なし
なし
研究責任医師
国際規定なし、現行
維持
研究責任医師
規定なし
規定なし
なし
なし
なし
研究責任医師
国際規定なし、現行
維持
研究責任医師
規定なし
規定なし
なし
なし
なし
研究責任医師
国際規定なし、現行
維持
研究責任医師
Sponsor(5.9)
Sponsor(3.8)
Sponsor(312.20)
Sponsor(EU CTR5)
Sponsor
(2004/1031-17)
Sponsor
ICHーGCP に準拠