よむ、つかう、まなぶ。
資料2-1 医療機器・再生医療等製品の不具合等報告について(概要)[676KB] (13 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_53225.html |
| 出典情報 | 薬事審議会 医療機器・再生医療等製品安全対策部会(令和6年度第2回 3/6)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
2-3-2
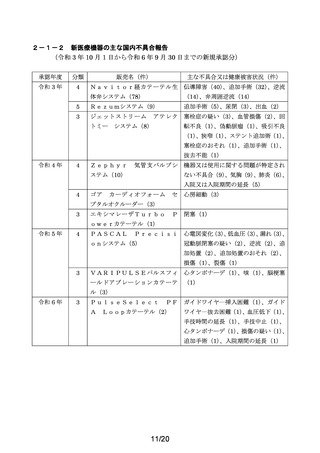
新再生医療等製品の主な国内不具合報告
(令和 3 年 10 月 1 日~令和 6 年 9 月 30 日までの新規承認分)
主な不具合又は健康被害状況※1(件)
承認年度
一般的名称等(件)
令和 3 年度
ヒト羊膜基質使用ヒト(自己)口腔粘 持続性角膜上皮欠損(1)
膜由来上皮細胞シート
(1件)
イデカブタゲン ビクルユーセル
サイトカイン放出症候群※2(55)、免
(75件)
疫エフェクター細胞関連神経毒性症候
群※3(10)
、好中球数減少(9)
※1 各製品における不具合報告件数の上位 3 位までを記載。
※2 CRS、CRS [サイトカイン放出症候群]、Cytokine release syndrome (CRS)、グレード 1 の CRS
(発熱)、サイトカイン放出症候群をまとめた。
※3 ICANS、ICANS(ICE スコア 1 点)、Immune effector cell-associated neurotoxicity syndrome
(ICANS)をまとめた。
13/20
新再生医療等製品の主な国内不具合報告
(令和 3 年 10 月 1 日~令和 6 年 9 月 30 日までの新規承認分)
主な不具合又は健康被害状況※1(件)
承認年度
一般的名称等(件)
令和 3 年度
ヒト羊膜基質使用ヒト(自己)口腔粘 持続性角膜上皮欠損(1)
膜由来上皮細胞シート
(1件)
イデカブタゲン ビクルユーセル
サイトカイン放出症候群※2(55)、免
(75件)
疫エフェクター細胞関連神経毒性症候
群※3(10)
、好中球数減少(9)
※1 各製品における不具合報告件数の上位 3 位までを記載。
※2 CRS、CRS [サイトカイン放出症候群]、Cytokine release syndrome (CRS)、グレード 1 の CRS
(発熱)、サイトカイン放出症候群をまとめた。
※3 ICANS、ICANS(ICE スコア 1 点)、Immune effector cell-associated neurotoxicity syndrome
(ICANS)をまとめた。
13/20