よむ、つかう、まなぶ。
資料2-1 医療機器基本計画に関する各省における取り組みの状況について (8 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_54795.html |
| 出典情報 | 国民が受ける医療の質の向上のための医療機器の研究開発及び普及の促進に関する検討会(第5回 3/17)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
該当箇所 列1 列2
列3
令和6年度の実績・状況
令和7年度の取組予定
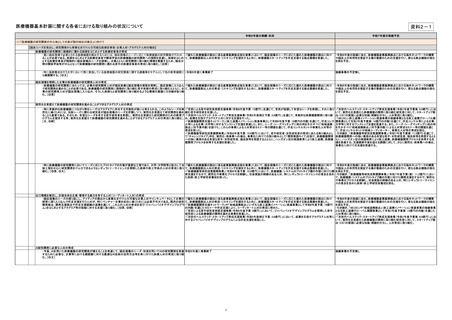
(2)「革新的な医療機器が世界に先駆けて我が国に上市される魅力的な環境の構築」に向けて
【早期実用化に向けた薬事承認制度・審査体制の構築】
Software as a Medical Device(SaMD)の実用化促進
・「プログラム医療機器の特性を踏まえた適切かつ迅速な承認及び開発のためのガイダンス(第二版)の公表について」(令和6年 ・引き続き「プログラム医療機器に係る優先的な審査等の試行的実施」を継続する。
進捗を引き続きフォローアップするとともに、医療機器の研究開発の進展を踏まえ、迅速な実用化に向け、必要に応じて新 6月5日事務連絡)を公表した。
・新たなプログラム医療機器の審査ポイント及び認証基準を策定する。
たな支援策に取り組む。[◎厚]
・「特定臨床研究で得られた試験成績を医療機器及び再生医療等製の承認申請に利用する場合の留意点・考え方の例示につい ・「プログラム医療機器実用化促進パッケージ戦略2(DASH for SaMD2)」を踏まえ、引
て」(令和6年6月5日事務連絡)を公表した。
き続き、薬事承認・保険適用までの予見可能性の確保や、日本発プログラム医療機器
・「「プログラム医療機器の特性を踏まえた二段階承認に係る取扱いについて」に関する質疑応答集について」(令和6年6月12日 の研究開発の加速・国際市場への展開の推進に向けた取組みを継続する。
事務連絡)を公表した。
・昨年度に引き続き、「プログラム医療機器に係る優先的な審査等の試行的実施」を実施した。
・「プログラム医療機器の薬事承認におけるデータ信頼性等の検討事業」において、更なるプログラム医療機器の早期実用化に
向けて、プログラム医療機器の変更計画確認手続制度(IDATEN)の更なる活用に向けた整理等を行っている。
・SaMDに関する萌芽的シーズの把握や、開発における考え方の整理に関する課題について、産学開発者と規制当局関係者とが ・引き続き経済産業省とも連携し、SaMD産学官連携フォーラム及びSaMD産学官サブ
その解決に向けた情報共有や忌憚のない意見交換を行うことを目的として、経済産業省とも連携し、「第4回SaMD産学官連携
フォーラムを開催する。
フォーラム」(令和6年9月3日)及び「SaMD産官学連携サブフォーラム2025」(令和7年2月10日)を開催した。
サイバーセキュリティに関する規格・手引きの整備
今後、SaMD等の外部のネットワークと接続し、機能を発揮する医療機器においてはユーザーを含む各ステークホルダー ・製造販売業者等が実施すべき医療機器のサイバーセキュリティ対策について、SBOMの利活用やレガシー医療機器に向けた対 ・医療機関における医療機器のサイバーセキュリティについて、製造販売業者と医療機
によるサイバーセキュリティの担保が重要であり、各ステークホルダーにおける責任分担等、現場への実装に向けて検討 策等の実態についての製造販売業者への調査及びそれを踏まえた今後の制度のあり方の議論を行っている。
関の連携のあり方等について議論を進める。
が必要な論点を整理しつつ、各製品において必要なサイバーセキュリティに関する規格や手引きの整備に取り組む。[◎
・SBOMを医療機関における医療機器サイバーセキュリティ確保に活用するため、SB
厚]
OMから得られる情報の活用方法について検討を行い、製造販売業者が医療機関に
対してSBOMの適切な活用方法を示すための指針の作成に向けた議論・検討を行う。
有事における新規医療機器の早期実用化に向けた取組
有事において、臨床現場に必要とされる医療機器が早期に研究開発され、上市されるために必要な環境の整備に取り組 令和4年5月薬機法改正により、感染症拡大などの有事における医療機器の緊急承認制度を導入した。(対応済み)
む。[◎厚]
【医療保険制度におけるイノベーションに対する適切な評価の実施】
イノベーションへの適切な評価
我が国におけるSaMDを含めた革新的な医療機器の実用化を進めるため、保険医療材料制度等におけるイノベーション 令和6年度保険医療材料制度改革において、
の適切な評価を、画期性・有用性に対する評価、新規医療材料を用いた技術の評価、機能区分の細分化、合理化及び定 ・チャレンジ申請の申請期限の延長や要件の明確化、体外診断用医薬品への対象の拡大
義の見直し等により引き続き推進する。[◎厚]
・経済性加算の新設
・再製造単回使用医療機器使用加算の新設
・希少疾病等の検査に用いる体外診断用医薬品等を評価する仕組みの新設
・プログラム医療機器(SaMD)の評価基準の明確化、原価計算方式の見直し、アップデート等により性能が向上した場合の再評
価、指導管理料・導入期加算や評価療養・選定療養の新設
等を実施したところ。
(対応済み)
・関係団体等の意見も伺いながら、令和8年度診療報酬改定に向けて検討を行う。
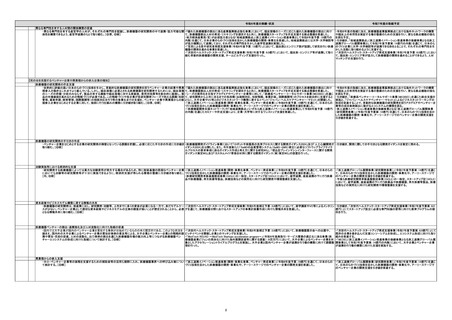
保険導入の手引きの作成
・令和6年度診療報酬改定を踏まえた「医療機器・体外診断用医薬品の保険適用に関するガイドブック」を作成した。
・「医療機器・体外診断用医薬品の保険適用に関するガイドブック」を活用し、保険適用
に
関する事前相談の充実を図っていく。
【規制調和の促進や日本を参照国制度の対象とする国の充実等による日本の薬事承認の国際的な意義の向上】
国際的な規制調和活動への積極的な参加
優れた医療機器の迅速な国内への導入を図れるようにするため、また国内に上市された製品を国際展開しようとした際に ○医療機器に関する国際的な規制調和活動に主体的に対応を行った。具体的には、
・引き続き、医療機器の国際的な規制調和の場への主体的な参加を通じて、国際的な
他国の規制が障壁とならないようにするため、IMDRFやHBD等国際的な規制調和活動に引き続き取り組む。[◎厚]
・IMDRFについては、管理委員会・各WGともに、日本の規制基準が国際的に活用できるよう活動を行った。また、2025年より日 ガイダンスの作成を進める。
本がIMDRF議長国となっているところ、議長として管理委員会等を主催し、規制調和に係る議論を主導した。
・特に、日本は2025年にIMDRF議長国となっているところ、議長として引き続き管理委
・HBDについては、日米産官学の関係者と毎月オンライン会議等の実施とともに、対面でのThink Tank Meetingをワシントンで開 員会等を主催し、規制調和に係る議論を主導していく。
催した。
・GHWPについては、正式メンバーとして年次会合・技術委員会に参加するとともに、他参加国と医療機器規制に関する意見交
換を行った。
新興国・途上国に対する規制調和の促進及び日本を参照国制度の対象とする国の充実
中長期の市場拡大を考慮し、東南アジア地域等の新興国・途上国への日本企業の医療機器の国際展開を促進する取組 ・令和6年度は、アジア医薬品・医療機器トレーニングセンターにおいて各国規制当局担当者向けに医療機器に関するセミナーを ・引き続き、アジア医薬品・医療機器トレーニングセンターにおいて東南アジア地域等の
も重要であり、アジア医薬品・医療機器トレーニングセンターの活動等を通じた規制調和や日本を参照国制度の対象とする 2回開催した(オンライン)。
各国規制当局担当者向けに医療機器に関するセミナーを開催するとともに、アジア諸
国の充実に向けて引き続き取り組む。[◎厚]
・また、令和6年度は、台湾の医療機器当局とのバイ会合を開催し、日本を参照国とする対応に向けた議論を進めた。
国と日本を参照国とする対応に向けた調整を進める。
8
列3
令和6年度の実績・状況
令和7年度の取組予定
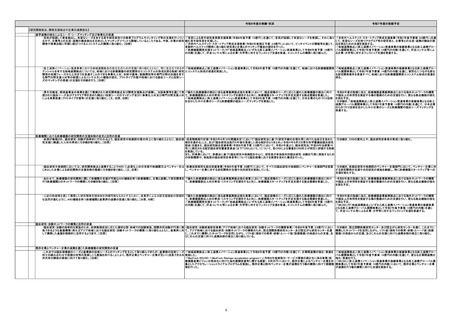
(2)「革新的な医療機器が世界に先駆けて我が国に上市される魅力的な環境の構築」に向けて
【早期実用化に向けた薬事承認制度・審査体制の構築】
Software as a Medical Device(SaMD)の実用化促進
・「プログラム医療機器の特性を踏まえた適切かつ迅速な承認及び開発のためのガイダンス(第二版)の公表について」(令和6年 ・引き続き「プログラム医療機器に係る優先的な審査等の試行的実施」を継続する。
進捗を引き続きフォローアップするとともに、医療機器の研究開発の進展を踏まえ、迅速な実用化に向け、必要に応じて新 6月5日事務連絡)を公表した。
・新たなプログラム医療機器の審査ポイント及び認証基準を策定する。
たな支援策に取り組む。[◎厚]
・「特定臨床研究で得られた試験成績を医療機器及び再生医療等製の承認申請に利用する場合の留意点・考え方の例示につい ・「プログラム医療機器実用化促進パッケージ戦略2(DASH for SaMD2)」を踏まえ、引
て」(令和6年6月5日事務連絡)を公表した。
き続き、薬事承認・保険適用までの予見可能性の確保や、日本発プログラム医療機器
・「「プログラム医療機器の特性を踏まえた二段階承認に係る取扱いについて」に関する質疑応答集について」(令和6年6月12日 の研究開発の加速・国際市場への展開の推進に向けた取組みを継続する。
事務連絡)を公表した。
・昨年度に引き続き、「プログラム医療機器に係る優先的な審査等の試行的実施」を実施した。
・「プログラム医療機器の薬事承認におけるデータ信頼性等の検討事業」において、更なるプログラム医療機器の早期実用化に
向けて、プログラム医療機器の変更計画確認手続制度(IDATEN)の更なる活用に向けた整理等を行っている。
・SaMDに関する萌芽的シーズの把握や、開発における考え方の整理に関する課題について、産学開発者と規制当局関係者とが ・引き続き経済産業省とも連携し、SaMD産学官連携フォーラム及びSaMD産学官サブ
その解決に向けた情報共有や忌憚のない意見交換を行うことを目的として、経済産業省とも連携し、「第4回SaMD産学官連携
フォーラムを開催する。
フォーラム」(令和6年9月3日)及び「SaMD産官学連携サブフォーラム2025」(令和7年2月10日)を開催した。
サイバーセキュリティに関する規格・手引きの整備
今後、SaMD等の外部のネットワークと接続し、機能を発揮する医療機器においてはユーザーを含む各ステークホルダー ・製造販売業者等が実施すべき医療機器のサイバーセキュリティ対策について、SBOMの利活用やレガシー医療機器に向けた対 ・医療機関における医療機器のサイバーセキュリティについて、製造販売業者と医療機
によるサイバーセキュリティの担保が重要であり、各ステークホルダーにおける責任分担等、現場への実装に向けて検討 策等の実態についての製造販売業者への調査及びそれを踏まえた今後の制度のあり方の議論を行っている。
関の連携のあり方等について議論を進める。
が必要な論点を整理しつつ、各製品において必要なサイバーセキュリティに関する規格や手引きの整備に取り組む。[◎
・SBOMを医療機関における医療機器サイバーセキュリティ確保に活用するため、SB
厚]
OMから得られる情報の活用方法について検討を行い、製造販売業者が医療機関に
対してSBOMの適切な活用方法を示すための指針の作成に向けた議論・検討を行う。
有事における新規医療機器の早期実用化に向けた取組
有事において、臨床現場に必要とされる医療機器が早期に研究開発され、上市されるために必要な環境の整備に取り組 令和4年5月薬機法改正により、感染症拡大などの有事における医療機器の緊急承認制度を導入した。(対応済み)
む。[◎厚]
【医療保険制度におけるイノベーションに対する適切な評価の実施】
イノベーションへの適切な評価
我が国におけるSaMDを含めた革新的な医療機器の実用化を進めるため、保険医療材料制度等におけるイノベーション 令和6年度保険医療材料制度改革において、
の適切な評価を、画期性・有用性に対する評価、新規医療材料を用いた技術の評価、機能区分の細分化、合理化及び定 ・チャレンジ申請の申請期限の延長や要件の明確化、体外診断用医薬品への対象の拡大
義の見直し等により引き続き推進する。[◎厚]
・経済性加算の新設
・再製造単回使用医療機器使用加算の新設
・希少疾病等の検査に用いる体外診断用医薬品等を評価する仕組みの新設
・プログラム医療機器(SaMD)の評価基準の明確化、原価計算方式の見直し、アップデート等により性能が向上した場合の再評
価、指導管理料・導入期加算や評価療養・選定療養の新設
等を実施したところ。
(対応済み)
・関係団体等の意見も伺いながら、令和8年度診療報酬改定に向けて検討を行う。
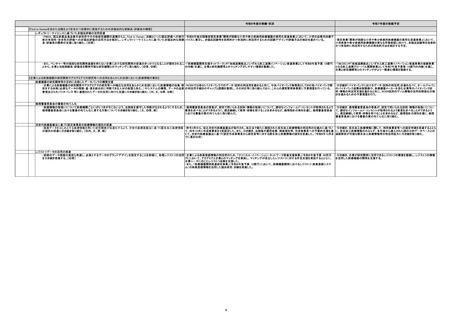
保険導入の手引きの作成
・令和6年度診療報酬改定を踏まえた「医療機器・体外診断用医薬品の保険適用に関するガイドブック」を作成した。
・「医療機器・体外診断用医薬品の保険適用に関するガイドブック」を活用し、保険適用
に
関する事前相談の充実を図っていく。
【規制調和の促進や日本を参照国制度の対象とする国の充実等による日本の薬事承認の国際的な意義の向上】
国際的な規制調和活動への積極的な参加
優れた医療機器の迅速な国内への導入を図れるようにするため、また国内に上市された製品を国際展開しようとした際に ○医療機器に関する国際的な規制調和活動に主体的に対応を行った。具体的には、
・引き続き、医療機器の国際的な規制調和の場への主体的な参加を通じて、国際的な
他国の規制が障壁とならないようにするため、IMDRFやHBD等国際的な規制調和活動に引き続き取り組む。[◎厚]
・IMDRFについては、管理委員会・各WGともに、日本の規制基準が国際的に活用できるよう活動を行った。また、2025年より日 ガイダンスの作成を進める。
本がIMDRF議長国となっているところ、議長として管理委員会等を主催し、規制調和に係る議論を主導した。
・特に、日本は2025年にIMDRF議長国となっているところ、議長として引き続き管理委
・HBDについては、日米産官学の関係者と毎月オンライン会議等の実施とともに、対面でのThink Tank Meetingをワシントンで開 員会等を主催し、規制調和に係る議論を主導していく。
催した。
・GHWPについては、正式メンバーとして年次会合・技術委員会に参加するとともに、他参加国と医療機器規制に関する意見交
換を行った。
新興国・途上国に対する規制調和の促進及び日本を参照国制度の対象とする国の充実
中長期の市場拡大を考慮し、東南アジア地域等の新興国・途上国への日本企業の医療機器の国際展開を促進する取組 ・令和6年度は、アジア医薬品・医療機器トレーニングセンターにおいて各国規制当局担当者向けに医療機器に関するセミナーを ・引き続き、アジア医薬品・医療機器トレーニングセンターにおいて東南アジア地域等の
も重要であり、アジア医薬品・医療機器トレーニングセンターの活動等を通じた規制調和や日本を参照国制度の対象とする 2回開催した(オンライン)。
各国規制当局担当者向けに医療機器に関するセミナーを開催するとともに、アジア諸
国の充実に向けて引き続き取り組む。[◎厚]
・また、令和6年度は、台湾の医療機器当局とのバイ会合を開催し、日本を参照国とする対応に向けた議論を進めた。
国と日本を参照国とする対応に向けた調整を進める。
8