よむ、つかう、まなぶ。
04【資料2】森内参考人提出資料 (34 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000192554_00016.html |
| 出典情報 | 厚生科学審議会 予防接種・ワクチン分科会(第29回 1/26)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
33
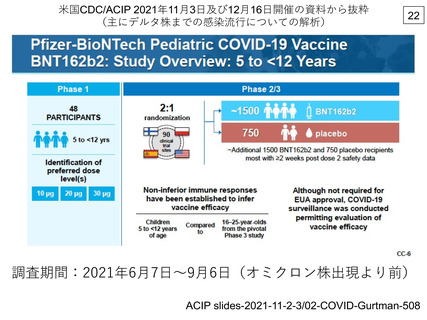
4) 国内で5~11歳を対象とする接種への承認申請が出されているワクチ
ンは、現時点ではファイザー社製のみです。同ワクチンは従来のワク
チンと⽐べ含有される mRNA量が1/3の製剤で、使⽤に際し注意が必
要です。海外では、5~11歳の⼩児に対する同ワクチンの発症予防効
果が 90%以上と報告されています 3)が、新しい変異ウイルス(オミク
ロン株など)への有効性を⽰すデータは⼗分に得られていません。
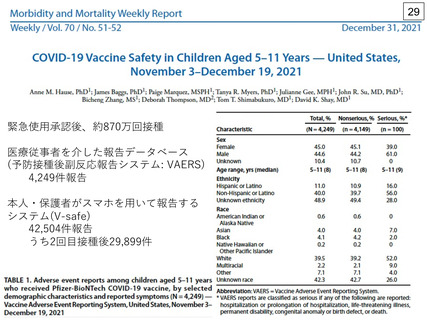
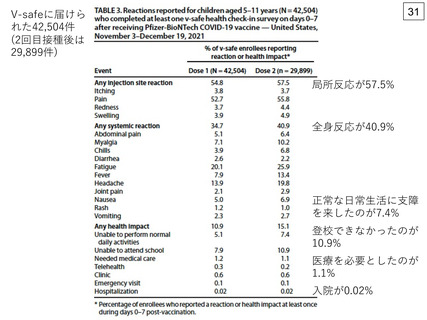
5) ⽶国では、2021年11⽉3⽇~12⽉19⽇までに5~11歳の⼩児に約870万
回のファイザー社製ワクチンが接種され、42,504⼈が⾃発的な健康状
況調査(v-safe)に登録されました。2回接種後、局所反応が57.5%、全
⾝反応が40.9%に認められ、発熱は1回⽬接種後 7.9%、2回⽬接種後
13.4%に認められました4)。
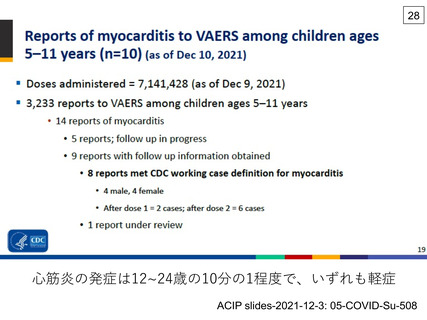
6) 上記と同期間に、⽶国の予防接種安全性監視システム(VAERS)には、
4,249 件の副反応疑い報告がありました。このうち97.6%(4,149件)が
⾮重篤でした 。重篤として報告された100件(2.4%)の中で最も多かっ
たのが発熱(29件)でした 。11件が⼼筋炎と判断されましたが、全員が
回復しました4)。
7) 5~11歳の⼩児では16~25歳の⼈と⽐べて⼀般的に接種後の副反応症状
の出現頻度は低かったと報告されています5)。
4) 国内で5~11歳を対象とする接種への承認申請が出されているワクチ
ンは、現時点ではファイザー社製のみです。同ワクチンは従来のワク
チンと⽐べ含有される mRNA量が1/3の製剤で、使⽤に際し注意が必
要です。海外では、5~11歳の⼩児に対する同ワクチンの発症予防効
果が 90%以上と報告されています 3)が、新しい変異ウイルス(オミク
ロン株など)への有効性を⽰すデータは⼗分に得られていません。
5) ⽶国では、2021年11⽉3⽇~12⽉19⽇までに5~11歳の⼩児に約870万
回のファイザー社製ワクチンが接種され、42,504⼈が⾃発的な健康状
況調査(v-safe)に登録されました。2回接種後、局所反応が57.5%、全
⾝反応が40.9%に認められ、発熱は1回⽬接種後 7.9%、2回⽬接種後
13.4%に認められました4)。
6) 上記と同期間に、⽶国の予防接種安全性監視システム(VAERS)には、
4,249 件の副反応疑い報告がありました。このうち97.6%(4,149件)が
⾮重篤でした 。重篤として報告された100件(2.4%)の中で最も多かっ
たのが発熱(29件)でした 。11件が⼼筋炎と判断されましたが、全員が
回復しました4)。
7) 5~11歳の⼩児では16~25歳の⼈と⽐べて⼀般的に接種後の副反応症状
の出現頻度は低かったと報告されています5)。