よむ、つかう、まなぶ。
10参考資料1 新型コロナワクチンに関する資料 (33 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000192554_00027.html |
| 出典情報 | 厚生科学審議会 予防接種・ワクチン分科会 予防接種基本方針部会(第52回 2/8)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
(2)安全性の評価
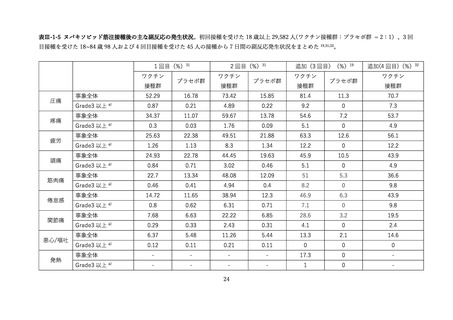
文献番号①33 の安全性の評価を表Ⅲ-2-2 に示す。局所反応は、多くは軽度から中等度で持
続期間は 1-2 日であった。
接種部位の疼痛が最も多く、ワクチン接種群において 1 回目 74%、
2 回目 71%が報告された。
全身反応は倦怠感が多く報告され、
ワクチン接種群で 1 回目 34%、
2 回目 39%に報告された。両群とも、観察期間中に重篤な副反応、死亡例は認められなかっ
た。
表Ⅲ-2-2 接種 7 日以内の局所及び全身反応 33
症状
2 回目(%)
ワクチン接種群
プラセボ群
ワクチン接種群
プラセボ群
発赤
15
6
19
5
腫脹
10
3
15
3
注射部位疼痛
74
31
71
29
発熱
3
1
7
1
倦怠感
34
31
39
24
頭痛
22
24
28
19
悪寒
5
5
10
4
嘔吐
2
1
2
1
下痢
6
4
5
5
筋肉痛
9
7
12
7
関節痛
3
5
5
4
解熱薬使用
14
8
20
8
局所反応
全身反応
a
1 回目(%)
a
38℃以上の発熱
また、米国からは v-safe(スマートフォンを用い、任意で新型コロナワクチン接種後の有
害事象を入力することで安全性をモニタリングするシステム)、VAERS(Vaccine Adverse
Event Reporting System 予防接種後の有害事象を受動的に収集しモニタリングするシステ
ム)
、VSD(Vaccine Safety Datalink 予防接種歴と医療記録を含み、心筋炎などの事象につ
いて能動的にモニタリングするシステム)の報告がされている 41。米国では 2021 年 10 月
29 日に FDA がファイザー社の 5-11 歳用のワクチンを承認し、2022 年 2 月 27 日までに
1600 万回以上の接種が行われた。v-safe では、2021 年 11 月3日から 2022 年 2 月 27 日に
おいてファイザー社のワクチンを受けた 5-11 歳の小児 48,795 例が登録された。ほとんど
の報告は軽度から中等度であり、接種の翌日に多く、2 回目の接種後に多く認められた。
VAERS では 7578 件の報告がされ、97%が非重篤であった。194 件の重篤な報告では 15 件
の心筋炎が報告され、8 件は男児で 2 回目の接種後(100 万回接種当たり 2.2 件)であった。
また、この年齢層における2回目の接種後の心筋炎の報告率は、12 歳から 15 歳と比較して
も低いものであった。VSD では毎週のモニタリングが行われたが、726,820 回の接種後に
33
文献番号①33 の安全性の評価を表Ⅲ-2-2 に示す。局所反応は、多くは軽度から中等度で持
続期間は 1-2 日であった。
接種部位の疼痛が最も多く、ワクチン接種群において 1 回目 74%、
2 回目 71%が報告された。
全身反応は倦怠感が多く報告され、
ワクチン接種群で 1 回目 34%、
2 回目 39%に報告された。両群とも、観察期間中に重篤な副反応、死亡例は認められなかっ
た。
表Ⅲ-2-2 接種 7 日以内の局所及び全身反応 33
症状
2 回目(%)
ワクチン接種群
プラセボ群
ワクチン接種群
プラセボ群
発赤
15
6
19
5
腫脹
10
3
15
3
注射部位疼痛
74
31
71
29
発熱
3
1
7
1
倦怠感
34
31
39
24
頭痛
22
24
28
19
悪寒
5
5
10
4
嘔吐
2
1
2
1
下痢
6
4
5
5
筋肉痛
9
7
12
7
関節痛
3
5
5
4
解熱薬使用
14
8
20
8
局所反応
全身反応
a
1 回目(%)
a
38℃以上の発熱
また、米国からは v-safe(スマートフォンを用い、任意で新型コロナワクチン接種後の有
害事象を入力することで安全性をモニタリングするシステム)、VAERS(Vaccine Adverse
Event Reporting System 予防接種後の有害事象を受動的に収集しモニタリングするシステ
ム)
、VSD(Vaccine Safety Datalink 予防接種歴と医療記録を含み、心筋炎などの事象につ
いて能動的にモニタリングするシステム)の報告がされている 41。米国では 2021 年 10 月
29 日に FDA がファイザー社の 5-11 歳用のワクチンを承認し、2022 年 2 月 27 日までに
1600 万回以上の接種が行われた。v-safe では、2021 年 11 月3日から 2022 年 2 月 27 日に
おいてファイザー社のワクチンを受けた 5-11 歳の小児 48,795 例が登録された。ほとんど
の報告は軽度から中等度であり、接種の翌日に多く、2 回目の接種後に多く認められた。
VAERS では 7578 件の報告がされ、97%が非重篤であった。194 件の重篤な報告では 15 件
の心筋炎が報告され、8 件は男児で 2 回目の接種後(100 万回接種当たり 2.2 件)であった。
また、この年齢層における2回目の接種後の心筋炎の報告率は、12 歳から 15 歳と比較して
も低いものであった。VSD では毎週のモニタリングが行われたが、726,820 回の接種後に
33