よむ、つかう、まなぶ。
○医薬品の新規薬価収載について 総-5-4 (11 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000212500_00223.html |
| 出典情報 | 中央社会保険医療協議会 総会(第564回 11/15)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
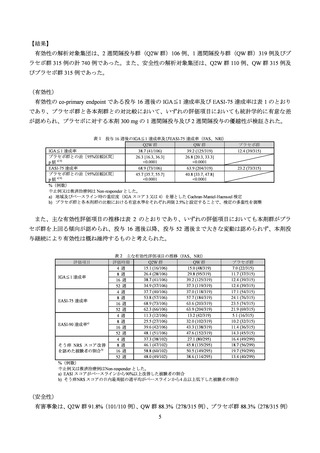
証された。
表 8 有効性の主要評価項目の成績(ITT 集団、NRI-MI)
本剤群
プラセボ群
投与 16 週時における EASI-75 達成率
43.3 (13/30)
18.8 (6/32)
プラセボ群との差[95%CI]a)
25.1 [3.3, 46.9]
0.0304
p 値 b)
%(例数)、投与 16 週以前に併用禁止薬及び併用禁止療法又は救済治療を受けた被験者、有害事象により治験
を中止した被験者並びに被験者又は保護者による同意撤回により治験を中止した被験者はノンレスポンダーと
され、その他の理由(COVID-19 を含む)で投与 16 週時のデータが欠測となった場合は、多重補完法により補
完された。
a) ベースライン時の年齢(生後 6 カ月以上 6 歳未満/6 歳以上 12 歳未満/12 歳以上)及び 6 歳以上 12 歳未満
の患者のベースライン時の IGA スコア(3/4)を層別因子とした Mantel-Haenszel 法
b) ベースライン時の年齢(生後 6 カ月以上 6 歳未満/6 歳以上 12 歳未満/12 歳以上)及び 6 歳以上 12 歳未満
の患者のベースライン時の IGA スコア(3/4)を層別因子とした Cochran-Mantel-Haenszel 検定
また、主な有効性評価項目の推移は表 9 のとおりであった。
表 9 主な有効性評価項目の推移(ITT 集団、NRI-MI)
EASI-75 達成率
IGA (0/1)達成率
本剤群
プラセボ→本剤群 a)
本剤群
プラセボ→本剤群 a)
16.7 (5/30)
0 (0/32)
3.3 (1/30)
3.1 (1/32)
43.3 (13/30)
18.8 (6/32)
10.0 (3/30)
9.4 (3/32)
62.9 (19/30)
56.3 (18/32)
37.8 (11/30)
43.8 (14/32)
4週
16 週
52 週
%(例数)
併用禁止治療若しくは救済治療を開始、又は有害事象、有効性欠如若しくは同意撤回により試験を中止し
た被験者は以降ノンレスポンダーとされた。その他の理由(COVID-19 を含む)による欠測値は多重補完
法により補完され、算出されたレスポンダーの割合を Rubin’s rule より統合し、反応が得られた被験者数が
算出された。
a) 投与 16 週以降(非盲検延長投与期)は体重に応じた用法・用量で本剤が投与された。
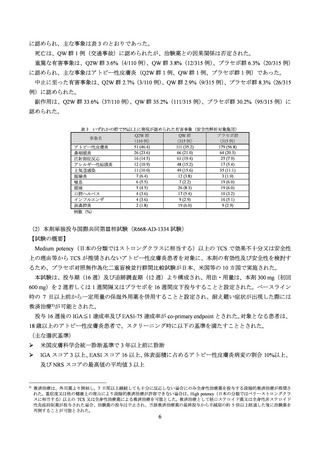
(安全性)
二重盲検投与期における有害事象は、本剤群 63.3%(19/30 例)
、プラセボ群 59.4%(19/32 例)に認め
られ、主な事象は表 10 のとおりであった。
死亡及び投与中止に至った有害事象は認められなかった。
重篤な有害事象は本剤群 3.3%(1/30 例、末端回腸炎)
、プラセボ群 3.1%(1/32 例、COVID-19)に認め
られたが、いずれも治験薬との因果関係は否定された。
副作用は、本剤群 16.7%(5/30 例)
、プラセボ群 9.4%(3/32 例)に認められた。
いずれかの群で 2 例以上に認められた有害事象(二重盲検投与期、安全性解析対象集団)
本剤群
プラセボ群
事象名
(30 例)
(32 例)
アレルギー性結膜炎
4 (13.3)
0
上咽頭炎
3 (10.0)
7 (21.9)
発熱
3 (10.0)
0
口腔ヘルペス
2 (6.7)
0
失神
2 (6.7)
0
便秘
2 (6.7)
0
齲歯
1 (3.3)
2 (6.3)
アトピー性皮膚炎
0
2 (6.3)
節足動物咬傷
0
2 (6.3)
例数(%)
表10
10
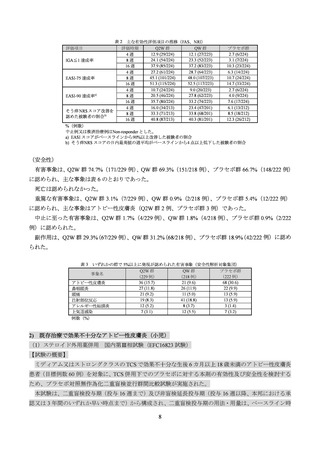
表 8 有効性の主要評価項目の成績(ITT 集団、NRI-MI)
本剤群
プラセボ群
投与 16 週時における EASI-75 達成率
43.3 (13/30)
18.8 (6/32)
プラセボ群との差[95%CI]a)
25.1 [3.3, 46.9]
0.0304
p 値 b)
%(例数)、投与 16 週以前に併用禁止薬及び併用禁止療法又は救済治療を受けた被験者、有害事象により治験
を中止した被験者並びに被験者又は保護者による同意撤回により治験を中止した被験者はノンレスポンダーと
され、その他の理由(COVID-19 を含む)で投与 16 週時のデータが欠測となった場合は、多重補完法により補
完された。
a) ベースライン時の年齢(生後 6 カ月以上 6 歳未満/6 歳以上 12 歳未満/12 歳以上)及び 6 歳以上 12 歳未満
の患者のベースライン時の IGA スコア(3/4)を層別因子とした Mantel-Haenszel 法
b) ベースライン時の年齢(生後 6 カ月以上 6 歳未満/6 歳以上 12 歳未満/12 歳以上)及び 6 歳以上 12 歳未満
の患者のベースライン時の IGA スコア(3/4)を層別因子とした Cochran-Mantel-Haenszel 検定
また、主な有効性評価項目の推移は表 9 のとおりであった。
表 9 主な有効性評価項目の推移(ITT 集団、NRI-MI)
EASI-75 達成率
IGA (0/1)達成率
本剤群
プラセボ→本剤群 a)
本剤群
プラセボ→本剤群 a)
16.7 (5/30)
0 (0/32)
3.3 (1/30)
3.1 (1/32)
43.3 (13/30)
18.8 (6/32)
10.0 (3/30)
9.4 (3/32)
62.9 (19/30)
56.3 (18/32)
37.8 (11/30)
43.8 (14/32)
4週
16 週
52 週
%(例数)
併用禁止治療若しくは救済治療を開始、又は有害事象、有効性欠如若しくは同意撤回により試験を中止し
た被験者は以降ノンレスポンダーとされた。その他の理由(COVID-19 を含む)による欠測値は多重補完
法により補完され、算出されたレスポンダーの割合を Rubin’s rule より統合し、反応が得られた被験者数が
算出された。
a) 投与 16 週以降(非盲検延長投与期)は体重に応じた用法・用量で本剤が投与された。
(安全性)
二重盲検投与期における有害事象は、本剤群 63.3%(19/30 例)
、プラセボ群 59.4%(19/32 例)に認め
られ、主な事象は表 10 のとおりであった。
死亡及び投与中止に至った有害事象は認められなかった。
重篤な有害事象は本剤群 3.3%(1/30 例、末端回腸炎)
、プラセボ群 3.1%(1/32 例、COVID-19)に認め
られたが、いずれも治験薬との因果関係は否定された。
副作用は、本剤群 16.7%(5/30 例)
、プラセボ群 9.4%(3/32 例)に認められた。
いずれかの群で 2 例以上に認められた有害事象(二重盲検投与期、安全性解析対象集団)
本剤群
プラセボ群
事象名
(30 例)
(32 例)
アレルギー性結膜炎
4 (13.3)
0
上咽頭炎
3 (10.0)
7 (21.9)
発熱
3 (10.0)
0
口腔ヘルペス
2 (6.7)
0
失神
2 (6.7)
0
便秘
2 (6.7)
0
齲歯
1 (3.3)
2 (6.3)
アトピー性皮膚炎
0
2 (6.3)
節足動物咬傷
0
2 (6.3)
例数(%)
表10
10