よむ、つかう、まなぶ。
【資料10】山梨大学岩崎副学長提出資料 (4 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_26202.html |
| 出典情報 | 革新的医薬品・医療機器創出のための官民対話(第5回 6/14)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
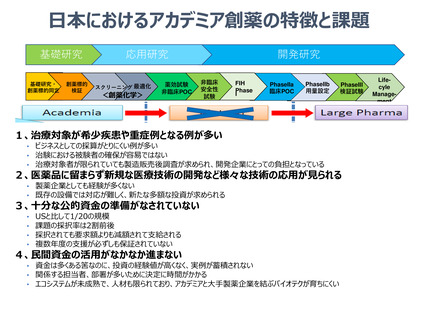
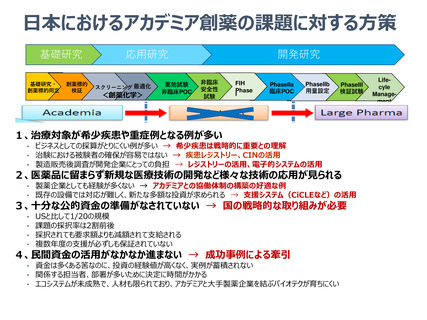
本邦の医薬品開発の推進のための課題に対する方策
1、アカデミアと企業との対話・相互理解・スムーズなTransition
・ 産学官共同型の研究開発事業の推進、GAPGFEEの改良によるアカデミア研究の支援の強化
・ アカデミアと企業の研究課題に対する自由な検討の場としてのAMED-FLuXなどの取り組み
・ AMED-FLuXの再生医療開発などへの展開での、より広い分野での相互の対話や理解の場の提供
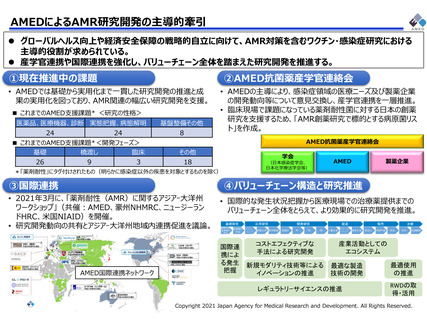
2、希少疾患や薬剤耐性菌(AMR)に対する治療薬の臨床現場への提供
・ 研究開発課題に対しての支援、AMED抗菌薬産学官連絡会の活用による開発への取り組み支援
・ 定期定額購買制度などのプル型インセンティブの導入
・ 後期開発、薬事承認、臨床現場への提供を行う官製(AMED)の製薬会社の設立
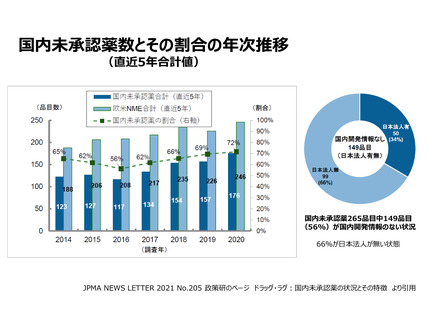
3、最近のドラッグラグに関する課題
・ 日本における臨床開発から薬事承認を担うCROの養成による海外ベンチャーへの働きかけ
・ (2)で示された官製の製薬会社による開発・承認・製造販売
・ 先駆け制度の活用等による日本での開発の推進策の強化
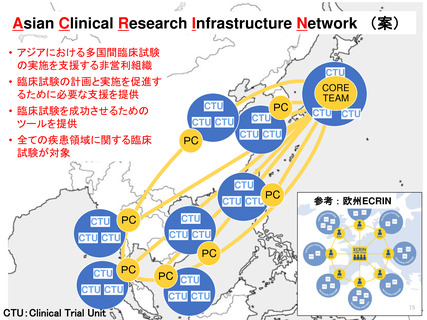
4、日本がリードする国際共同試験体制の構築
・ 臨床研究中核病院を核とするAROによる共同試験体制の構築
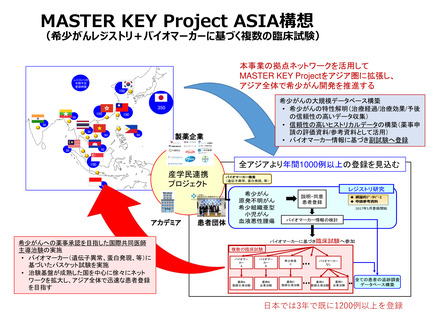
・ がんセンターやNCGMによる実績を活用したASEAN諸国との連携によるアジア共同試験体制の構築
・ アジア共同試験を企画・実施を管理・運営できる実効性の高い事務局の設置
5、新規医薬品開発に対する社会の理解・支援
・ 国民等への治験・臨床研究の普及啓発活動に関する調査・研究の推進
・ 臨床試験に対する患者・市民参画(PPI)活動の推進
・ 医療現場や研究者、開発企業における研究開発インテグリティの向上による信頼性の確保
1、アカデミアと企業との対話・相互理解・スムーズなTransition
・ 産学官共同型の研究開発事業の推進、GAPGFEEの改良によるアカデミア研究の支援の強化
・ アカデミアと企業の研究課題に対する自由な検討の場としてのAMED-FLuXなどの取り組み
・ AMED-FLuXの再生医療開発などへの展開での、より広い分野での相互の対話や理解の場の提供
2、希少疾患や薬剤耐性菌(AMR)に対する治療薬の臨床現場への提供
・ 研究開発課題に対しての支援、AMED抗菌薬産学官連絡会の活用による開発への取り組み支援
・ 定期定額購買制度などのプル型インセンティブの導入
・ 後期開発、薬事承認、臨床現場への提供を行う官製(AMED)の製薬会社の設立
3、最近のドラッグラグに関する課題
・ 日本における臨床開発から薬事承認を担うCROの養成による海外ベンチャーへの働きかけ
・ (2)で示された官製の製薬会社による開発・承認・製造販売
・ 先駆け制度の活用等による日本での開発の推進策の強化
4、日本がリードする国際共同試験体制の構築
・ 臨床研究中核病院を核とするAROによる共同試験体制の構築
・ がんセンターやNCGMによる実績を活用したASEAN諸国との連携によるアジア共同試験体制の構築
・ アジア共同試験を企画・実施を管理・運営できる実効性の高い事務局の設置
5、新規医薬品開発に対する社会の理解・支援
・ 国民等への治験・臨床研究の普及啓発活動に関する調査・研究の推進
・ 臨床試験に対する患者・市民参画(PPI)活動の推進
・ 医療現場や研究者、開発企業における研究開発インテグリティの向上による信頼性の確保