よむ、つかう、まなぶ。
【資料No.1】1.7_同種同効品一覧表 (11 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_26901.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会(令和4年度第3回 7/20)、医薬品第二部会(令和4年度第6回 7/20)(合同開催)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
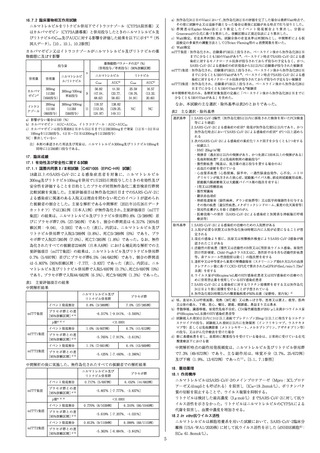
16. 薬物動態
16.1 血中濃度
16.1.1 健康成人
モルヌピラビルはNHCのプロドラッグであり、全身循環へ到達す
る前に主要代謝物であるNHCへ加水分解され細胞内に取り込まれ
た後、活性型であるリボヌクレオシド三リン酸化体(NHC-TP)
にリン酸化される。
(1)単回投与
健康成人にモルヌピラビル800mgを単回経口投与した際のNHCの
血漿中濃度推移を図1に、血漿中薬物動態パラメータを表1に示す。
モルヌピラビル50~1600mgの範囲で、NHCのCmax及びAUCは概
して用量に比例して増加した(外国人データ)。
図1 健康成人にモルヌピラビル800mgを単回経口投与した際の
NHCの血漿中濃度推移(平均値+標準偏差)
16.6.2 肝機能障害者
肝機能障害者におけるモルヌピラビル及びNHCの薬物動態の評価
は実施していない。非臨床試験の結果、NHCの主要な消失経路は
肝代謝ではないと考えられた。また、モルヌピラビルは主に消化
管及び肝臓でNHCへ代謝される一方、モルヌピラビルの加水分解
に必要な代謝酵素は広範な組織に分布しているため、肝機能障害
がモルヌピラビル及びNHCの曝露量に影響を及ぼす可能性は低い。
16.6.3 高齢者
母集団薬物動態解析の結果、高齢者におけるNHCの薬物動態は若
年者と同様であった(外国人データ)。
16.7 薬物相互作用
16.7.1 In vitro試験成績
モルヌピラビル及びNHCは主要な薬物代謝酵素及びトランスポー
ターの基質ではない。また、モルヌピラビル及びNHCは主要な薬
物代謝酵素及びトランスポーターに対する阻害作用又は誘導作用
を示さなかった。
16.7.2 臨床における薬物相互作用試験
臨床薬物相互作用試験は実施していない。
注)本剤の承認された用法及び用量は、1回800mgを1日2回5日間経口投与
である。
17. 臨床成績
表1
健康成人にモルヌピラビル800mgを単回経口投与した際のNHCの血
漿中薬物動態パラメータ
例数
6
Tmax†
(hr)
1.75
(1.50-2.50)
Cmax‡
(ng/mL)
2770
(13.3)
AUC0-12hr‡
(ng・hr/mL)
8190
(21.5)
†中央値(範囲)
‡幾何平均(変動係数%)
(2)反復投与
健康成人にモルヌピラビル800mgを12時間ごとに反復経口投与した
際のNHCの血漿中薬物動態パラメータは表2のとおりであった。1日
2回の反復経口投与で得られたNHCのAUC0-12hrの累積係数(1.09)
に基づく有効半減期は3.3時間であった(外国人データ)。
表2
17.1 有効性及び安全性に関する試験
17.1.1 国際共同第Ⅱ/Ⅲ相試験[MOVe-OUT(002)試験]
18歳以上のSARS-CoV-2による感染症患者を対象に、モルヌピラ
ビルの有効性、安全性等を評価することを目的として、プラセボ
対照無作為化二重盲検並行群間比較試験を実施した。主要評価項
目は、無作為化29日目までの理由を問わないすべての入院又は死
亡した被験者の割合とした。第Ⅲ相パートでは、モルヌピラビル
800mgを1日2回(12時間ごと)5日間経口投与した。主要な解析
である中間解析では775例が無作為割り付けされ、無作為化29日
目までの追跡を完了した時点(日本人被験者は含まれなかった)
での主要評価項目の結果は、モルヌピラビル800mg群7.3%
(28/385例)及びプラセボ群14.1%(53/377例)であり、割合の
群間差は-6.8%(95%信頼区間:-11.3, -2.4)であった(表1)。
なお、無作為割り付けされた1433例(日本人被験者8例を含む)
全例における補足的な解析での主要評価項目の結果は、モルヌピ
ラビル800mg群6.8%(48/709例)及びプラセボ群9.7%
(68/699例)であり、割合の群間差は-3.0%(95%信頼区間:
-5.9, -0.1)であった。内訳は、モルヌピラビル800mg群で入院
48/709例(6.8%)、死亡1/709例(0.1%)であり、プラセボ群で
入院67/699例(9.6%)、死亡9/699例(1.3%)、不明1/699例
(0.1%)であった。
表1
中間解析の主要評価項目の結果(Modified Intent-To-Treat集団)
モルヌピラビル
800mg群
(385例)
例数(%)
健康成人にモルヌピラビル800mgを12時間ごとに反復経口投与した際
の定常状態におけるNHCの血漿中薬物動態パラメータ
例数
5
Tmax†
(hr)
1.50
(1.00-2.02)
Cmax‡
(ng/mL)
2970
(16.8)
AUC0-12hr‡
(ng・hr/mL)
8330
(17.9)
†中央値(範囲)
‡幾何平均(変動係数%)
16.2 吸収
16.2.1 食事の影響
健康成人にモルヌピラビル200mgを単回経口投与注)した際、高脂
肪食摂取後投与では空腹時投与に比べてNHCのCmaxは35%減少し、
AUCは両条件下で同程度であった(外国人データ)。本剤は、食
事とは関係なく投与可能である。
16.3 分布
NHCのヒト血漿蛋白に対する結合率は0%であった(in vitroデータ)
。
16.4 代謝
モルヌピラビルはNHCのプロドラッグであり、全身循環へ到達する前
に主要代謝物であるNHCへ加水分解される。NHCは内因性ピリミジ
ンの代謝と同じ経路でウリジン及びシチジンへ代謝され、消失する。
16.5 排泄
健康成人にモルヌピラビル800mgを1日2回5.5日間反復経口投与注)し
た際、NHCの尿中排泄率は3%であった(外国人データ)。
16.6 特定の背景を有する患者
16.6.1 腎機能障害者
モルヌピラビル及びNHCの主要な消失経路は腎排泄ではないため、
腎機能障害がこれらの排泄に影響を及ぼす可能性は低い。母集団
薬物動態解析の結果、軽度及び中等度の腎機能障害がNHCの薬物
動態に及ぼす意味のある影響はみられなかった(外国人データ)。
重度腎機能障害患者(eGFR 30mL/min/1.73m2未満)又は透析
を必要とする患者におけるモルヌピラビル及びNHCの薬物動態の
評価は実施していない。
無作為化29日目
までの理由を問
わないすべての
入院又は死亡§
入院
死亡
不明||
プラセボ群
割合の群間差†
P値†‡
(377例)
(95%信頼区間)
例数(%)
28
(7.3%)
53
(14.1%)
28
(7.3%)
0
(0%)
0
(0%)
52
(13.8%)
8
(2.1%)
1
(0.3%)
-6.8
0.0012
(-11.3, -2.4)
†SARS-CoV-2による感染症の症状発現から無作為割付け日までの期間(3
日間以下/3日間超)を層別因子とした層別Miettinen and Nurminen法。
試験全体の有意水準は片側2.5%で、中間解析による仮説検定の多重性の調
整方法としてGamma family型(γ=-1)の消費関数を用いた(有意水準
片側0.0092)。
‡片側P値。
§病院又は急性期治療施設(例、救急救命室)において24時間以上の急性期
治療を行った場合と定義した。
|| 無作為化29日目の状況が不明な被験者は、有効性解析において、入院又は
死亡としてカウントされた。
注:無作為化29日目までに死亡したすべての症例は、入院後の死亡であった。
なお、本試験の主な選択・除外基準は表2のとおりであった。
-2-
16.1 血中濃度
16.1.1 健康成人
モルヌピラビルはNHCのプロドラッグであり、全身循環へ到達す
る前に主要代謝物であるNHCへ加水分解され細胞内に取り込まれ
た後、活性型であるリボヌクレオシド三リン酸化体(NHC-TP)
にリン酸化される。
(1)単回投与
健康成人にモルヌピラビル800mgを単回経口投与した際のNHCの
血漿中濃度推移を図1に、血漿中薬物動態パラメータを表1に示す。
モルヌピラビル50~1600mgの範囲で、NHCのCmax及びAUCは概
して用量に比例して増加した(外国人データ)。
図1 健康成人にモルヌピラビル800mgを単回経口投与した際の
NHCの血漿中濃度推移(平均値+標準偏差)
16.6.2 肝機能障害者
肝機能障害者におけるモルヌピラビル及びNHCの薬物動態の評価
は実施していない。非臨床試験の結果、NHCの主要な消失経路は
肝代謝ではないと考えられた。また、モルヌピラビルは主に消化
管及び肝臓でNHCへ代謝される一方、モルヌピラビルの加水分解
に必要な代謝酵素は広範な組織に分布しているため、肝機能障害
がモルヌピラビル及びNHCの曝露量に影響を及ぼす可能性は低い。
16.6.3 高齢者
母集団薬物動態解析の結果、高齢者におけるNHCの薬物動態は若
年者と同様であった(外国人データ)。
16.7 薬物相互作用
16.7.1 In vitro試験成績
モルヌピラビル及びNHCは主要な薬物代謝酵素及びトランスポー
ターの基質ではない。また、モルヌピラビル及びNHCは主要な薬
物代謝酵素及びトランスポーターに対する阻害作用又は誘導作用
を示さなかった。
16.7.2 臨床における薬物相互作用試験
臨床薬物相互作用試験は実施していない。
注)本剤の承認された用法及び用量は、1回800mgを1日2回5日間経口投与
である。
17. 臨床成績
表1
健康成人にモルヌピラビル800mgを単回経口投与した際のNHCの血
漿中薬物動態パラメータ
例数
6
Tmax†
(hr)
1.75
(1.50-2.50)
Cmax‡
(ng/mL)
2770
(13.3)
AUC0-12hr‡
(ng・hr/mL)
8190
(21.5)
†中央値(範囲)
‡幾何平均(変動係数%)
(2)反復投与
健康成人にモルヌピラビル800mgを12時間ごとに反復経口投与した
際のNHCの血漿中薬物動態パラメータは表2のとおりであった。1日
2回の反復経口投与で得られたNHCのAUC0-12hrの累積係数(1.09)
に基づく有効半減期は3.3時間であった(外国人データ)。
表2
17.1 有効性及び安全性に関する試験
17.1.1 国際共同第Ⅱ/Ⅲ相試験[MOVe-OUT(002)試験]
18歳以上のSARS-CoV-2による感染症患者を対象に、モルヌピラ
ビルの有効性、安全性等を評価することを目的として、プラセボ
対照無作為化二重盲検並行群間比較試験を実施した。主要評価項
目は、無作為化29日目までの理由を問わないすべての入院又は死
亡した被験者の割合とした。第Ⅲ相パートでは、モルヌピラビル
800mgを1日2回(12時間ごと)5日間経口投与した。主要な解析
である中間解析では775例が無作為割り付けされ、無作為化29日
目までの追跡を完了した時点(日本人被験者は含まれなかった)
での主要評価項目の結果は、モルヌピラビル800mg群7.3%
(28/385例)及びプラセボ群14.1%(53/377例)であり、割合の
群間差は-6.8%(95%信頼区間:-11.3, -2.4)であった(表1)。
なお、無作為割り付けされた1433例(日本人被験者8例を含む)
全例における補足的な解析での主要評価項目の結果は、モルヌピ
ラビル800mg群6.8%(48/709例)及びプラセボ群9.7%
(68/699例)であり、割合の群間差は-3.0%(95%信頼区間:
-5.9, -0.1)であった。内訳は、モルヌピラビル800mg群で入院
48/709例(6.8%)、死亡1/709例(0.1%)であり、プラセボ群で
入院67/699例(9.6%)、死亡9/699例(1.3%)、不明1/699例
(0.1%)であった。
表1
中間解析の主要評価項目の結果(Modified Intent-To-Treat集団)
モルヌピラビル
800mg群
(385例)
例数(%)
健康成人にモルヌピラビル800mgを12時間ごとに反復経口投与した際
の定常状態におけるNHCの血漿中薬物動態パラメータ
例数
5
Tmax†
(hr)
1.50
(1.00-2.02)
Cmax‡
(ng/mL)
2970
(16.8)
AUC0-12hr‡
(ng・hr/mL)
8330
(17.9)
†中央値(範囲)
‡幾何平均(変動係数%)
16.2 吸収
16.2.1 食事の影響
健康成人にモルヌピラビル200mgを単回経口投与注)した際、高脂
肪食摂取後投与では空腹時投与に比べてNHCのCmaxは35%減少し、
AUCは両条件下で同程度であった(外国人データ)。本剤は、食
事とは関係なく投与可能である。
16.3 分布
NHCのヒト血漿蛋白に対する結合率は0%であった(in vitroデータ)
。
16.4 代謝
モルヌピラビルはNHCのプロドラッグであり、全身循環へ到達する前
に主要代謝物であるNHCへ加水分解される。NHCは内因性ピリミジ
ンの代謝と同じ経路でウリジン及びシチジンへ代謝され、消失する。
16.5 排泄
健康成人にモルヌピラビル800mgを1日2回5.5日間反復経口投与注)し
た際、NHCの尿中排泄率は3%であった(外国人データ)。
16.6 特定の背景を有する患者
16.6.1 腎機能障害者
モルヌピラビル及びNHCの主要な消失経路は腎排泄ではないため、
腎機能障害がこれらの排泄に影響を及ぼす可能性は低い。母集団
薬物動態解析の結果、軽度及び中等度の腎機能障害がNHCの薬物
動態に及ぼす意味のある影響はみられなかった(外国人データ)。
重度腎機能障害患者(eGFR 30mL/min/1.73m2未満)又は透析
を必要とする患者におけるモルヌピラビル及びNHCの薬物動態の
評価は実施していない。
無作為化29日目
までの理由を問
わないすべての
入院又は死亡§
入院
死亡
不明||
プラセボ群
割合の群間差†
P値†‡
(377例)
(95%信頼区間)
例数(%)
28
(7.3%)
53
(14.1%)
28
(7.3%)
0
(0%)
0
(0%)
52
(13.8%)
8
(2.1%)
1
(0.3%)
-6.8
0.0012
(-11.3, -2.4)
†SARS-CoV-2による感染症の症状発現から無作為割付け日までの期間(3
日間以下/3日間超)を層別因子とした層別Miettinen and Nurminen法。
試験全体の有意水準は片側2.5%で、中間解析による仮説検定の多重性の調
整方法としてGamma family型(γ=-1)の消費関数を用いた(有意水準
片側0.0092)。
‡片側P値。
§病院又は急性期治療施設(例、救急救命室)において24時間以上の急性期
治療を行った場合と定義した。
|| 無作為化29日目の状況が不明な被験者は、有効性解析において、入院又は
死亡としてカウントされた。
注:無作為化29日目までに死亡したすべての症例は、入院後の死亡であった。
なお、本試験の主な選択・除外基準は表2のとおりであった。
-2-