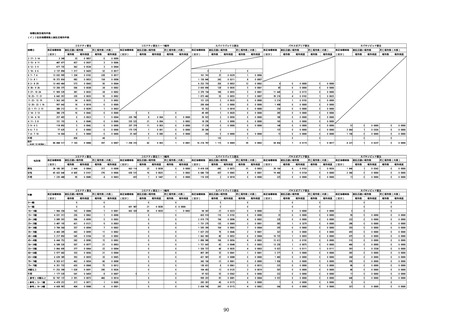
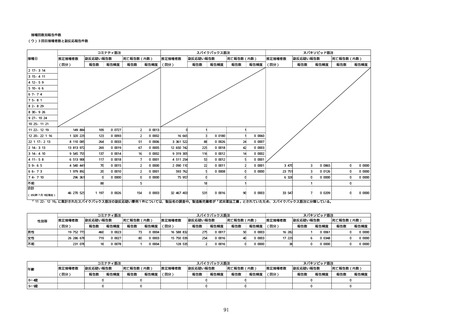
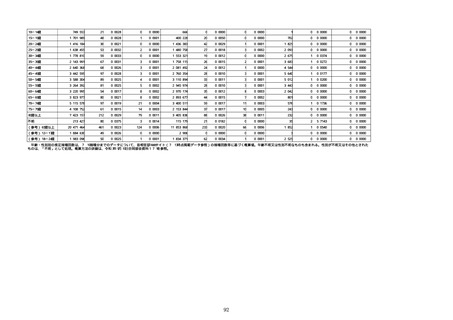
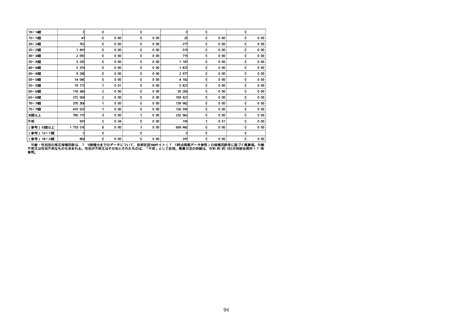
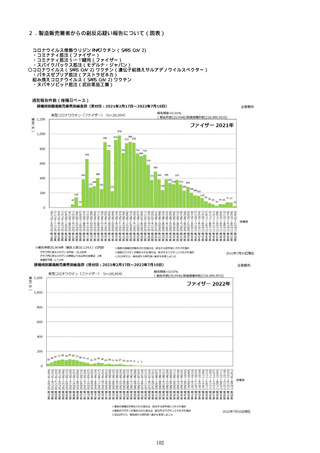
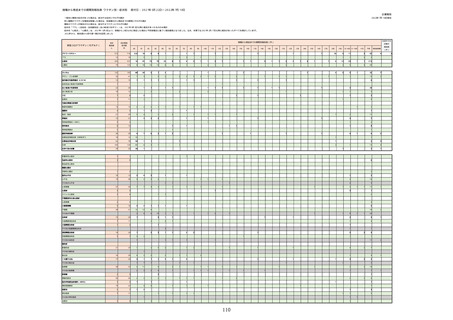
資料1-2-1 薬機法に基づく製造販売業者からの副反応疑い報告状況について (51 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000208910_00046.html |
| 出典情報 | 第82回厚生科学審議会予防接種・ワクチン分科会副反応検討部会、令和4年度第8回薬事・食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会(合同開催)(8/5)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
起立障害
強直性痙攣
傾眠
失神
失神寸前の状態
振戦
体位性めまい
大脳石灰化
単麻痺
中枢神経系血管炎
鎮静
頭痛
熱性痙攣
反射減弱
肘部管症候群
末梢性ニューロパチー
痙攣発作
代謝および栄養障害
栄養補給障害
食欲減退
脱水
低血糖
皮膚および皮下組織障害
そう痒症
紅斑
水疱
多汗症
多形紅斑
点状出血
冷汗
蕁麻疹
免疫系障害
アナフィラキシーショック
アナフィラキシー反応
過敏症
臨床検査
C−反応性蛋白増加
アスパラギン酸アミノトランスフェラーゼ増加
アラニンアミノトランスフェラーゼ増加
トロポニンI増加
ヘマトクリット減少
ヘモグロビン減少
握力低下
外来血圧低下
血圧測定不能
血圧低下
血中クレアチニン減少
血中ナトリウム減少
血中ビリルビン増加
血中ブドウ糖減少
血中乳酸脱水素酵素増加
血中尿酸減少
昏睡尺度異常
酸素飽和度低下
心拍数減少
脳性ナトリウム利尿ペプチド前駆体N端フラグメント増加
白血球数増加
平均赤血球ヘモグロビン濃度増加
平均赤血球容積減少
総計
3
1
1
1
3
2
1
1
1
1
1
1
4
3
1
1
2
5
1
2
4
3
1
2
1
1
1
1
1
1
2
2
1
1
1
1
1
1
1
1
1
1
3
1
1
1
1
1
1
1
1
3
1
1
1
1
206
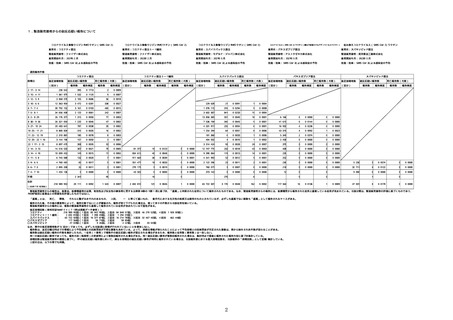
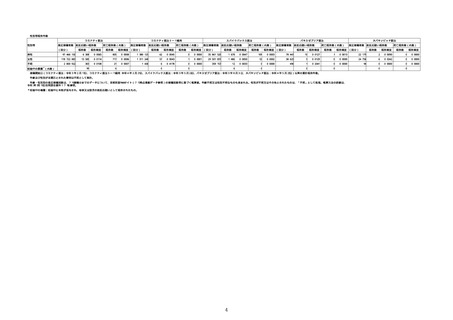
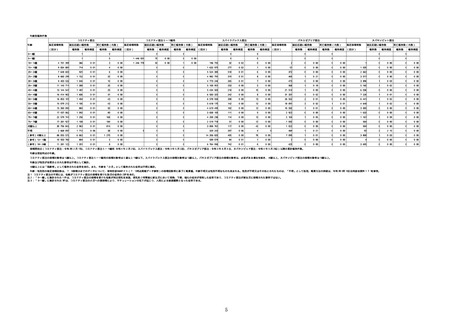
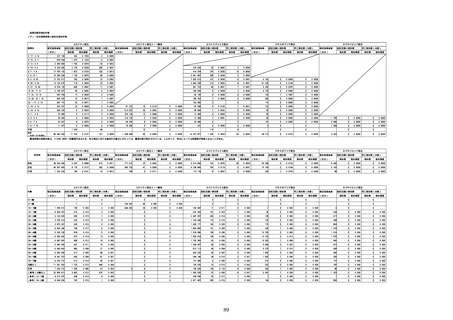
※接種開始日(コミナティ筋注:令和3年2月17日、コミナティ筋注5〜
11歳用:令和4年2月21日、スパイクバックス筋注:令和3年5月22日、バ
キスゼブリア筋注:令和3年8月3日、ヌバキソビッド筋注:令和4年5
月25日)以降の累計報告件数。
※資料1−1−2−4「3.報告症例一覧(製造販売業者からの報告)」
を基に、MedDRA SOC(太字部)及びPTを元に分類の上集計。
※コミナティ筋注については、取り下げ処理前の報告内容に基づき集計し
ている。今後、副反応疑い報告が取り下げになった場合、当該報告に記載
されていた事象は、次回以降の合同部会資料では、集計件数から除外され
る。
51