よむ、つかう、まなぶ。
資料2-2 チェストベリー乾燥エキスのリスク区分について (1 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_29975.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会安全対策調査会(令和4年度第22回 12/27)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
令和4年 12 月 27 日
令和4年度医薬品等安全対策調査会
資料2-2
チェストベリー乾燥エキスのリスク区分について
成分・含量
薬効分類
投与経路
販売名(製造販売業者)
効能・効果
用法・用量
承認年月日
製造販売開始日
評価を行う理由
製造販売後調査概要
(P.9~使用成績調査)
チェストベリー乾燥エキス 40 ㎎
(原生薬換算 180 ㎎)
生薬
経口
プレフェミン(ゼリア新薬工業株式会社)
月経前の次の諸症状(月経前症候群)の緩和:乳房のはり、頭痛、イ
ライラ、怒りっぽい、気分変調
成人女性(18 歳以上)1回1錠、1日1回服用する。
2014 年4月3日
2014 年9月 10 日
再審査が終了したため(現在のリスク区分:第1類)
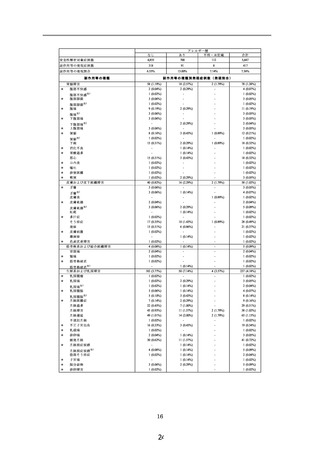
特別調査:5,709 症例(うち、安全性解析対象は 5,667 例)
調査期間:2014 年9月 10 日~2021 年2月 17 日
副作用:417 例 544 件(7.36%)
うち重篤な副作用:乳癌 1 件
未知の副作用:不正子宮出血※119 件、便秘 12 件、腹痛及び傾眠各
11 件 等
一般調査
調査期間:2014 年9月 10 日~2022 年4月2日
副作用:87 例 101 件
うち重篤な副作用:なし
未知の副作用:月経中間期出血※114 件、頭痛 12 件、腹痛7件 等
※1
MedDRA のバージョン変更に伴い、特別調査においては「不正子宮出
血」として報告を集積している事象について、一般調査では「月経
中間期出血」とされている。
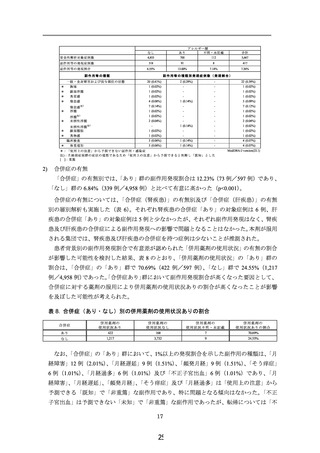
医薬品医療機器法第 使用成績調査のデータロック後に、製造販売業者が報告した副作用の
68 条の 10 第1項に基 個別症例報告
づき、製造販売業者が
2022 年4月3日~2022 年 12 月6日:0件
報告した副作用の個
別症例報告
使用上の注意の改訂 なし
の指導
【参考】
本剤と類似の有効成分等を含む医薬品はない。
1
令和4年度医薬品等安全対策調査会
資料2-2
チェストベリー乾燥エキスのリスク区分について
成分・含量
薬効分類
投与経路
販売名(製造販売業者)
効能・効果
用法・用量
承認年月日
製造販売開始日
評価を行う理由
製造販売後調査概要
(P.9~使用成績調査)
チェストベリー乾燥エキス 40 ㎎
(原生薬換算 180 ㎎)
生薬
経口
プレフェミン(ゼリア新薬工業株式会社)
月経前の次の諸症状(月経前症候群)の緩和:乳房のはり、頭痛、イ
ライラ、怒りっぽい、気分変調
成人女性(18 歳以上)1回1錠、1日1回服用する。
2014 年4月3日
2014 年9月 10 日
再審査が終了したため(現在のリスク区分:第1類)
特別調査:5,709 症例(うち、安全性解析対象は 5,667 例)
調査期間:2014 年9月 10 日~2021 年2月 17 日
副作用:417 例 544 件(7.36%)
うち重篤な副作用:乳癌 1 件
未知の副作用:不正子宮出血※119 件、便秘 12 件、腹痛及び傾眠各
11 件 等
一般調査
調査期間:2014 年9月 10 日~2022 年4月2日
副作用:87 例 101 件
うち重篤な副作用:なし
未知の副作用:月経中間期出血※114 件、頭痛 12 件、腹痛7件 等
※1
MedDRA のバージョン変更に伴い、特別調査においては「不正子宮出
血」として報告を集積している事象について、一般調査では「月経
中間期出血」とされている。
医薬品医療機器法第 使用成績調査のデータロック後に、製造販売業者が報告した副作用の
68 条の 10 第1項に基 個別症例報告
づき、製造販売業者が
2022 年4月3日~2022 年 12 月6日:0件
報告した副作用の個
別症例報告
使用上の注意の改訂 なし
の指導
【参考】
本剤と類似の有効成分等を含む医薬品はない。
1