よむ、つかう、まなぶ。
患-2○患者申出療養の総括報告書に関する評価について (1 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000203222_00025.html |
| 出典情報 | 患者申出療養評価会議(第41回 6/22)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
患
-
2
5.6.22
(別紙)
患者申出療養 総括報告書に関する評価表(告示旧2)
評価委員
主担当: 上村 尚人
副担当: 山崎 力
患者申出療養の名称
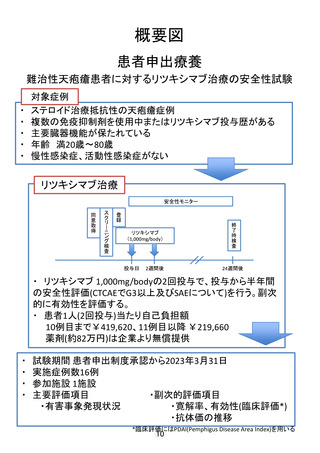
難治性天疱瘡患者に対するリツキシマブ治療
申請医療機関の名称
慶應義塾大学病院
医療技術の概要
(概要)
現時点で天疱瘡に投与できる薬剤や治療法は保険収載され
ているものは少なく、実臨床で用いられている免疫抑制剤に関
しても保険収載されていない。そのような現状において、それら
の治療を行ってもなお治療抵抗性の患者に対して本邦では現
時点では対応策がなく、長期間に及ぶ高用量のステロイド内服
を余儀なくされている。そのような患者に対して、海外では追加
治療の第一選択薬としてリツキシマブが使用されており、その
有効性と安全性が報告されている。
本邦では2016年から医師主導治験が行われておりリツキシ
マブの保険収載を目指しているが、より多くの患者にリツキシ
マブ治療を提供し安全性と有効性について検討を行い保険収
載の際の参考データとして提供する。また本試験及び医師主
導治験でのリツキシマブの用法・用量(1000mg/body ×2回/
月)は、日本では未承認であり、安全性情報の集積が必要であ
る。かつその安全情報収集が医薬品医療機器総合機構からも
求められている。
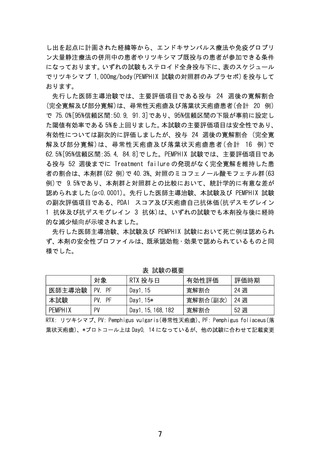
本試験は、オープンラベルシングルアームとして実施され
る。治療として、ステロイド治療抵抗性の天疱瘡患者に対して、
ステロイドや他の併用療法を継続した状態でリツキシマブ
1,000 mg/bodyを2週間隔で2回(0週目:Day0、2週目:Day14)点
滴静脈内投与を行う。その後、外来治療を継続(PSLおよび併
用薬については症状に応じ、医師の判断で漸減可能)する。
Day168もしくは中止時まで、有害事象及び有効性について
観察する。
(効果)
1
-
2
5.6.22
(別紙)
患者申出療養 総括報告書に関する評価表(告示旧2)
評価委員
主担当: 上村 尚人
副担当: 山崎 力
患者申出療養の名称
難治性天疱瘡患者に対するリツキシマブ治療
申請医療機関の名称
慶應義塾大学病院
医療技術の概要
(概要)
現時点で天疱瘡に投与できる薬剤や治療法は保険収載され
ているものは少なく、実臨床で用いられている免疫抑制剤に関
しても保険収載されていない。そのような現状において、それら
の治療を行ってもなお治療抵抗性の患者に対して本邦では現
時点では対応策がなく、長期間に及ぶ高用量のステロイド内服
を余儀なくされている。そのような患者に対して、海外では追加
治療の第一選択薬としてリツキシマブが使用されており、その
有効性と安全性が報告されている。
本邦では2016年から医師主導治験が行われておりリツキシ
マブの保険収載を目指しているが、より多くの患者にリツキシ
マブ治療を提供し安全性と有効性について検討を行い保険収
載の際の参考データとして提供する。また本試験及び医師主
導治験でのリツキシマブの用法・用量(1000mg/body ×2回/
月)は、日本では未承認であり、安全性情報の集積が必要であ
る。かつその安全情報収集が医薬品医療機器総合機構からも
求められている。
本試験は、オープンラベルシングルアームとして実施され
る。治療として、ステロイド治療抵抗性の天疱瘡患者に対して、
ステロイドや他の併用療法を継続した状態でリツキシマブ
1,000 mg/bodyを2週間隔で2回(0週目:Day0、2週目:Day14)点
滴静脈内投与を行う。その後、外来治療を継続(PSLおよび併
用薬については症状に応じ、医師の判断で漸減可能)する。
Day168もしくは中止時まで、有害事象及び有効性について
観察する。
(効果)
1