よむ、つかう、まなぶ。
【資料1】柳本構成員提出資料 (3 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_37787.html |
| 出典情報 | 創薬力の強化・安定供給の確保等のための薬事規制のあり方に関する検討会(第8回 2/8)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
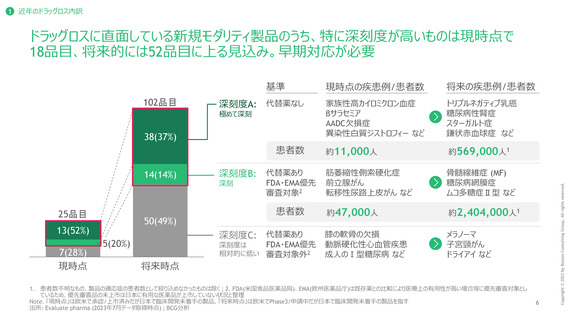
1 近年のドラッグロス内訳
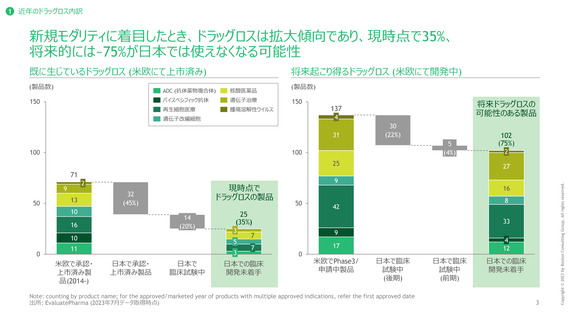
既存モダリティのドラッグロス割合27%に対し、新規モダリティのドラッグロス割合は35%と
深刻なドラッグロス(=日本での開発未着手)の傾向が認められる
米欧で2014年以降承認・上市済み製品の日本での開発状況
既存モダリティ
新規モダリティ
日本で開発未着手の製品: 27%
518
32
(45%)
• 狂犬病, 炭疽, 天然痘,
マラリア等の感染症
• 鎌状赤血球症
• オピオイド中毒治療薬
85
(16%)
71
14
(20%)
17
(3%)
0
(0%)
25
(35%)
141
(27%)
米欧で承認・上
市済み(2014-)
日本で承認・
上市済み
日本で臨
床試験中
日本に原則として
存在しない疾患1
日本でも存
在する疾患
米欧で承認・上
市済み(2014-)
日本で承認・
上市済み
日本での臨床開発未着手
1. 狂犬病, 炭疽, 天然痘, エボラ出血熱, マラリア, リーシュマニア, トリパノソーマ, エボラ出血熱, ヘビ毒, 鎌状赤血球症, オピオイド中毒治療薬を除外
Note: 集計は製品名単位; 複数Indicationを持つ場合は最初の承認年を参照
出所: EvaluatePharma (2023年7月データ取得時点)
日本で臨
床試験中
日本に原則として
存在しない疾患
日本でも存
在する疾患
日本での臨床開発未着手
2
Copyright © 2023 by Boston Consulting Group. All rights reserved.
275
(53%)
日本で開発未着手の製品: 35%
(製品数)
既存モダリティのドラッグロス割合27%に対し、新規モダリティのドラッグロス割合は35%と
深刻なドラッグロス(=日本での開発未着手)の傾向が認められる
米欧で2014年以降承認・上市済み製品の日本での開発状況
既存モダリティ
新規モダリティ
日本で開発未着手の製品: 27%
518
32
(45%)
• 狂犬病, 炭疽, 天然痘,
マラリア等の感染症
• 鎌状赤血球症
• オピオイド中毒治療薬
85
(16%)
71
14
(20%)
17
(3%)
0
(0%)
25
(35%)
141
(27%)
米欧で承認・上
市済み(2014-)
日本で承認・
上市済み
日本で臨
床試験中
日本に原則として
存在しない疾患1
日本でも存
在する疾患
米欧で承認・上
市済み(2014-)
日本で承認・
上市済み
日本での臨床開発未着手
1. 狂犬病, 炭疽, 天然痘, エボラ出血熱, マラリア, リーシュマニア, トリパノソーマ, エボラ出血熱, ヘビ毒, 鎌状赤血球症, オピオイド中毒治療薬を除外
Note: 集計は製品名単位; 複数Indicationを持つ場合は最初の承認年を参照
出所: EvaluatePharma (2023年7月データ取得時点)
日本で臨
床試験中
日本に原則として
存在しない疾患
日本でも存
在する疾患
日本での臨床開発未着手
2
Copyright © 2023 by Boston Consulting Group. All rights reserved.
275
(53%)
日本で開発未着手の製品: 35%
(製品数)