よむ、つかう、まなぶ。
資料4 医療機器基本計画に関する産業界における取組みについて (10 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_38515.html |
| 出典情報 | 国民が受ける医療の質の向上のための医療機器の研究開発及び普及の促進に関する検討会(第4回 3/12)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
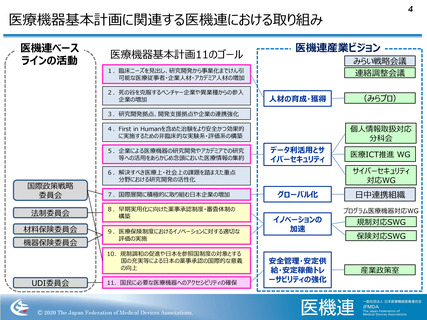
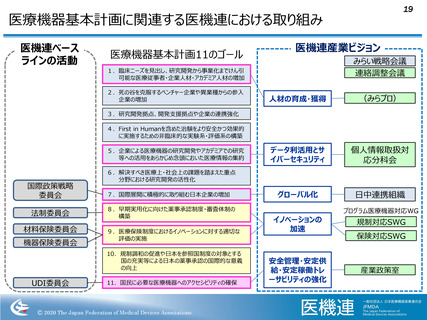
7.国際展開に積極的に取り組む日本企業の増加
10
10.規制調和の促進や日本を参照国制度の対象とする国の充実等による
日本の薬事承認の国際的な意義の向上
国際政策戦略委員会
【活動内容と成果】
◆海外展開における医療機器登録審査の整合化
•
•
•
•
•
業界として関心の高い国において、各国の課題や要望を集約し厚労省・PMDAと情報を共有、各年
次毎の取り組みについての意見交換・整合を実施している。
台湾、タイ、インドは二ヵ国シンポを継続実施しており、今年度は日台交流会議、日タイ合同シンポジ
ウムが開催され、規制動向の把握と共に業界要望事項を議論した。イベント後に行政間の協議結
果を業界側に共有する仕組みもしっかり機能している。これらの二ヵ国シンポは開催を重ね薬事規制
の大きな問題は解決してきており、PMDAは開催頻度を減らし内容の充実を図る検討を進めている。
欧州MDR/IVDRでは状況を監視ししつつ、経産省と連携し、6月、11月、3月(予定)の
WTO/TBT会合にて日本の要望・意見を提示した。
国際的な規制調和を目的とする国際組織であるIMDRF (International Medical Device Regulators Forum)
のAI/ML、Cybersecurity、SaMDの3つのWG活動に参画すると共に、厚労省・PMDAと協力し
第2回IMDRF活動報告会を開催し、国内企業に向け国際規制調和の動向を発信した。
同じく国際規制調和を進めるGHWP (Global Harmonization Working Party) への日本の正式加盟を受け
、医機連内に活動体制を構築し、各WGにメンバー登録申請を行い具体的な活動に着手している。
◆海外展開における課題への対応
•
日本はアジアをはじめとする多数の国から参照国に位置付けられているが、医療機器申請において各
国の参照国制度の活用が進んでいないとの声がある。今後、各国の申請事例の収集と分析を行い、
制度による迅速化を阻害する要因がある場合は行政とも連携し改善に結び付ける。
Ⓒ 2020 The Japan Federation of Medical Devices Associations.
10
10.規制調和の促進や日本を参照国制度の対象とする国の充実等による
日本の薬事承認の国際的な意義の向上
国際政策戦略委員会
【活動内容と成果】
◆海外展開における医療機器登録審査の整合化
•
•
•
•
•
業界として関心の高い国において、各国の課題や要望を集約し厚労省・PMDAと情報を共有、各年
次毎の取り組みについての意見交換・整合を実施している。
台湾、タイ、インドは二ヵ国シンポを継続実施しており、今年度は日台交流会議、日タイ合同シンポジ
ウムが開催され、規制動向の把握と共に業界要望事項を議論した。イベント後に行政間の協議結
果を業界側に共有する仕組みもしっかり機能している。これらの二ヵ国シンポは開催を重ね薬事規制
の大きな問題は解決してきており、PMDAは開催頻度を減らし内容の充実を図る検討を進めている。
欧州MDR/IVDRでは状況を監視ししつつ、経産省と連携し、6月、11月、3月(予定)の
WTO/TBT会合にて日本の要望・意見を提示した。
国際的な規制調和を目的とする国際組織であるIMDRF (International Medical Device Regulators Forum)
のAI/ML、Cybersecurity、SaMDの3つのWG活動に参画すると共に、厚労省・PMDAと協力し
第2回IMDRF活動報告会を開催し、国内企業に向け国際規制調和の動向を発信した。
同じく国際規制調和を進めるGHWP (Global Harmonization Working Party) への日本の正式加盟を受け
、医機連内に活動体制を構築し、各WGにメンバー登録申請を行い具体的な活動に着手している。
◆海外展開における課題への対応
•
日本はアジアをはじめとする多数の国から参照国に位置付けられているが、医療機器申請において各
国の参照国制度の活用が進んでいないとの声がある。今後、各国の申請事例の収集と分析を行い、
制度による迅速化を阻害する要因がある場合は行政とも連携し改善に結び付ける。
Ⓒ 2020 The Japan Federation of Medical Devices Associations.