よむ、つかう、まなぶ。
資料2-1 令和5年度の安全対策について[850KB] (3 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_40727.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会(令和6年度第1回 6/19)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
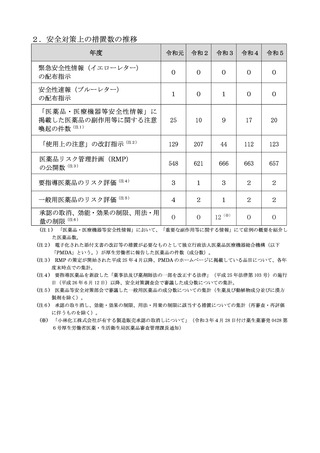
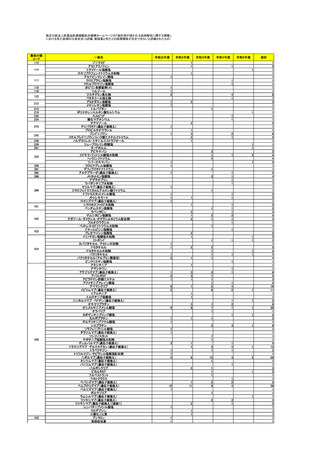
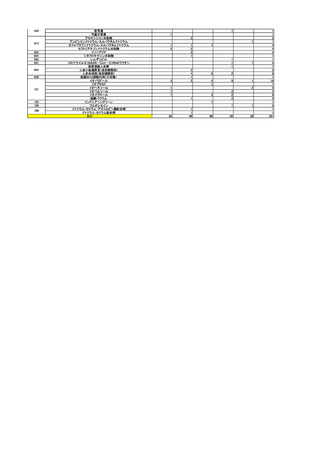
2.安全対策上の措置数の推移
年度
令和元
令和2
令和3
令和4
令和5
緊急安全性情報(イエローレター)
の配布指示
0
0
0
0
0
安全性速報(ブルーレター)
の配布指示
1
0
1
0
0
「医薬品・医療機器等安全性情報」に
掲載した医薬品の副作用等に関する注意
喚起の件数(注1)
25
10
9
17
20
「使用上の注意」の改訂指示(注2)
129
207
44
112
123
医薬品リスク管理計画(RMP)
の公開数(注3)
548
621
666
663
657
要指導医薬品のリスク評価(注4)
3
1
3
2
2
一般用医薬品のリスク評価(注5)
4
2
1
2
2
承認の取消、効能・効果の制限、用法・用
量の制限(注6)
0
0
12(※)
0
0
(注1)
「医薬品・医療機器等安全性情報」において、「重要な副作用等に関する情報」にて症例の概要を紹介し
た医薬品数。
(注2)
電子化された添付文書の改訂等の措置が必要なものとして独立行政法人医薬品医療機器総合機構(以下
「PMDA」という。)が厚生労働省に報告した医薬品の件数(成分数)。
(注3)
RMP の策定が開始された平成 25 年4月以降、PMDA のホームページに掲載している品目について、各年
度末時点での集計。
(注4)
要指導医薬品を新設した「薬事法及び薬剤師法の一部を改正する法律」(平成 25 年法律第 103 号)の施行
日(平成 26 年6月 12 日)以降、安全対策調査会で審議した成分数についての集計。
(注5)
医薬品等安全対策部会で審議した一般用医薬品の成分数についての集計(生薬及び動植物成分並びに漢方
製剤を除く)。
(注6)
承認の取り消し、効能・効果の制限、用法・用量の制限に該当する措置についての集計(再審査・再評価
に伴うものを除く)。
(※)
「小林化工株式会社が有する製造販売承認の取消しについて」(令和3年4月 28 日付け薬生薬審発 0428 第
6号厚生労働省医薬・生活衛生局医薬品審査管理課長通知)
2
年度
令和元
令和2
令和3
令和4
令和5
緊急安全性情報(イエローレター)
の配布指示
0
0
0
0
0
安全性速報(ブルーレター)
の配布指示
1
0
1
0
0
「医薬品・医療機器等安全性情報」に
掲載した医薬品の副作用等に関する注意
喚起の件数(注1)
25
10
9
17
20
「使用上の注意」の改訂指示(注2)
129
207
44
112
123
医薬品リスク管理計画(RMP)
の公開数(注3)
548
621
666
663
657
要指導医薬品のリスク評価(注4)
3
1
3
2
2
一般用医薬品のリスク評価(注5)
4
2
1
2
2
承認の取消、効能・効果の制限、用法・用
量の制限(注6)
0
0
12(※)
0
0
(注1)
「医薬品・医療機器等安全性情報」において、「重要な副作用等に関する情報」にて症例の概要を紹介し
た医薬品数。
(注2)
電子化された添付文書の改訂等の措置が必要なものとして独立行政法人医薬品医療機器総合機構(以下
「PMDA」という。)が厚生労働省に報告した医薬品の件数(成分数)。
(注3)
RMP の策定が開始された平成 25 年4月以降、PMDA のホームページに掲載している品目について、各年
度末時点での集計。
(注4)
要指導医薬品を新設した「薬事法及び薬剤師法の一部を改正する法律」(平成 25 年法律第 103 号)の施行
日(平成 26 年6月 12 日)以降、安全対策調査会で審議した成分数についての集計。
(注5)
医薬品等安全対策部会で審議した一般用医薬品の成分数についての集計(生薬及び動植物成分並びに漢方
製剤を除く)。
(注6)
承認の取り消し、効能・効果の制限、用法・用量の制限に該当する措置についての集計(再審査・再評価
に伴うものを除く)。
(※)
「小林化工株式会社が有する製造販売承認の取消しについて」(令和3年4月 28 日付け薬生薬審発 0428 第
6号厚生労働省医薬・生活衛生局医薬品審査管理課長通知)
2