よむ、つかう、まなぶ。
総-2参考2 (15 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_46580.html |
| 出典情報 | 中央社会保険医療協議会 総会(第599回 12/11)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
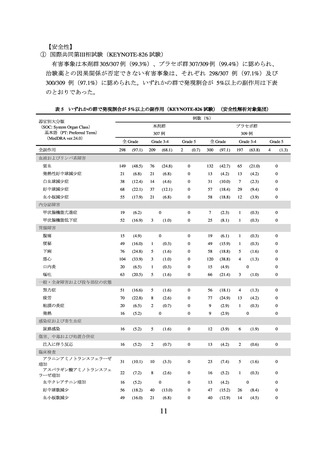
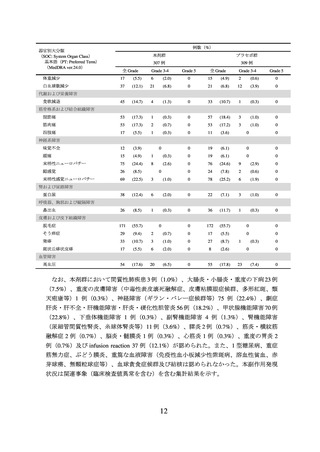
器官別大分類
(SOC: System Organ Class)
基本語(PT: Preferred Term)
(MedDRA ver.26.1)
例数(%)
全 Grade
本剤+CCRT 群
プラセボ+CCRT 群
528 例
530 例
Grade 3-4
Grade 5
全 Grade
Grade 3-4
Grade 5
血小板数減少
116
(22.0)
25
(4.7)
0
109
(20.6)
13
(2.5)
0
体重減少
55
(10.4)
6
(1.1)
0
54
(10.2)
3
(0.6)
0
白血球数減少
173
(32.8)
104
(19.7)
0
183
(34.5)
111
(20.9)
0
食欲減退
83
(15.7)
3
(0.6)
0
88
(16.6)
2
(0.4)
0
低カルシウム血症
26
(4.9)
6
(1.1)
0
29
(5.5)
4
(0.8)
0
低カリウム血症
74
(14.0)
22
(4.2)
0
58
(10.9)
15
(2.8)
0
低マグネシウム血症
91
(17.2)
13
(2.5)
0
88
(16.6)
11
(2.1)
0
低ナトリウム血症
45
(8.5)
5
(0.9)
0
45
(8.5)
7
(1.3)
0
39
(7.4)
2
(0.4)
0
34
(6.4)
0
0
22
(4.2)
0
28
(5.3)
0
0
60
(11.4)
1
(0.2)
0
47
(8.9)
0
0
29
(5.5)
3
(0.6)
0
29
(5.5)
0
0
そう痒症
28
(5.3)
1
(0.2)
0
17
(3.2)
0
0
発疹
30
(5.7)
2
(0.4)
0
21
(4.0)
0
0
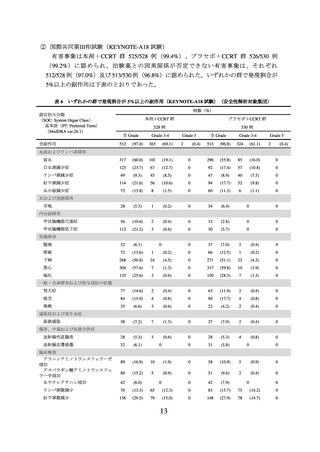
代謝および栄養障害
筋骨格系および結合組織障害
関節痛
神経系障害
味覚不全
0
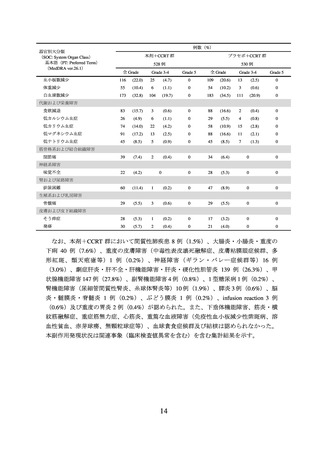
腎および尿路障害
排尿困難
生殖系および乳房障害
骨盤痛
皮膚および皮下組織障害
なお、本剤+CCRT 群において間質性肺疾患 8 例(1.5%)、大腸炎・小腸炎・重度の
下痢 40 例(7.6%)、重度の皮膚障害(中毒性表皮壊死融解症、皮膚粘膜眼症候群、多
形紅斑、類天疱瘡等)1 例(0.2%)、神経障害(ギラン・バレー症候群等) 16 例
(3.0%)、劇症肝炎・肝不全・肝機能障害・肝炎・硬化性胆管炎 139 例(26.3%)、甲
状腺機能障害 147 例(27.8%)、副腎機能障害 4 例(0.8%)、1 型糖尿病 1 例(0.2%)、
腎機能障害(尿細管間質性腎炎、糸球体腎炎等)10 例(1.9%)、膵炎 3 例(0.6%)、脳
炎・髄膜炎・脊髄炎 1 例(0.2%)、ぶどう膜炎 1 例(0.2%)、infusion reaction 3 例
(0.6%)及び重度の胃炎 2 例(0.4%)が認められた。また、下垂体機能障害、筋炎・横
紋筋融解症、重症筋無力症、心筋炎、重篤な血液障害(免疫性血小板減少性紫斑病、溶
血性貧血、赤芽球癆、無顆粒球症等)、血球貪食症候群及び結核は認められなかった。
本副作用発現状況は関連事象(臨床検査値異常を含む)を含む集計結果を示す。
14
(SOC: System Organ Class)
基本語(PT: Preferred Term)
(MedDRA ver.26.1)
例数(%)
全 Grade
本剤+CCRT 群
プラセボ+CCRT 群
528 例
530 例
Grade 3-4
Grade 5
全 Grade
Grade 3-4
Grade 5
血小板数減少
116
(22.0)
25
(4.7)
0
109
(20.6)
13
(2.5)
0
体重減少
55
(10.4)
6
(1.1)
0
54
(10.2)
3
(0.6)
0
白血球数減少
173
(32.8)
104
(19.7)
0
183
(34.5)
111
(20.9)
0
食欲減退
83
(15.7)
3
(0.6)
0
88
(16.6)
2
(0.4)
0
低カルシウム血症
26
(4.9)
6
(1.1)
0
29
(5.5)
4
(0.8)
0
低カリウム血症
74
(14.0)
22
(4.2)
0
58
(10.9)
15
(2.8)
0
低マグネシウム血症
91
(17.2)
13
(2.5)
0
88
(16.6)
11
(2.1)
0
低ナトリウム血症
45
(8.5)
5
(0.9)
0
45
(8.5)
7
(1.3)
0
39
(7.4)
2
(0.4)
0
34
(6.4)
0
0
22
(4.2)
0
28
(5.3)
0
0
60
(11.4)
1
(0.2)
0
47
(8.9)
0
0
29
(5.5)
3
(0.6)
0
29
(5.5)
0
0
そう痒症
28
(5.3)
1
(0.2)
0
17
(3.2)
0
0
発疹
30
(5.7)
2
(0.4)
0
21
(4.0)
0
0
代謝および栄養障害
筋骨格系および結合組織障害
関節痛
神経系障害
味覚不全
0
腎および尿路障害
排尿困難
生殖系および乳房障害
骨盤痛
皮膚および皮下組織障害
なお、本剤+CCRT 群において間質性肺疾患 8 例(1.5%)、大腸炎・小腸炎・重度の
下痢 40 例(7.6%)、重度の皮膚障害(中毒性表皮壊死融解症、皮膚粘膜眼症候群、多
形紅斑、類天疱瘡等)1 例(0.2%)、神経障害(ギラン・バレー症候群等) 16 例
(3.0%)、劇症肝炎・肝不全・肝機能障害・肝炎・硬化性胆管炎 139 例(26.3%)、甲
状腺機能障害 147 例(27.8%)、副腎機能障害 4 例(0.8%)、1 型糖尿病 1 例(0.2%)、
腎機能障害(尿細管間質性腎炎、糸球体腎炎等)10 例(1.9%)、膵炎 3 例(0.6%)、脳
炎・髄膜炎・脊髄炎 1 例(0.2%)、ぶどう膜炎 1 例(0.2%)、infusion reaction 3 例
(0.6%)及び重度の胃炎 2 例(0.4%)が認められた。また、下垂体機能障害、筋炎・横
紋筋融解症、重症筋無力症、心筋炎、重篤な血液障害(免疫性血小板減少性紫斑病、溶
血性貧血、赤芽球癆、無顆粒球症等)、血球貪食症候群及び結核は認められなかった。
本副作用発現状況は関連事象(臨床検査値異常を含む)を含む集計結果を示す。
14