よむ、つかう、まなぶ。
参考資料13 Vaccines and Related Biological Products Advisory Committee June 7, 2022 Meeting Presentation - FDA Review of Effectiveness and Safety of Novavax COVID-19 Vaccine in Adults > 18 Years of Age - Emergency Use Authorization Request(Vaccines and Related Biological Products Advisory Committee June 7, 2022 Meeting FDA提出資料) (43 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000208910_00043.html |
| 出典情報 | 第80回厚生科学審議会予防接種・ワクチン分科会副反応検討部会、令和4年度第5回薬事・食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会(合同開催)(6/10)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
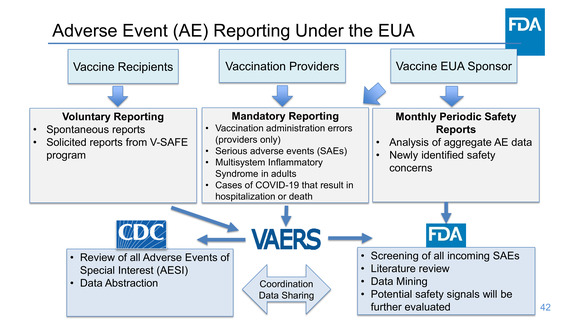
Adverse Event (AE) Reporting Under the EUA
Vaccine Recipients
Voluntary Reporting
• Spontaneous reports
• Solicited reports from V-SAFE
program
Vaccination Providers
Vaccine EUA Sponsor
Mandatory Reporting
Monthly Periodic Safety
Reports
• Analysis of aggregate AE data
• Newly identified safety
concerns
• Vaccination administration errors
(providers only)
• Serious adverse events (SAEs)
• Multisystem Inflammatory
Syndrome in adults
• Cases of COVID-19 that result in
hospitalization or death
• Review of all Adverse Events of
Special Interest (AESI)
• Data Abstraction
Coordination
Data Sharing
•
•
•
•
Screening of all incoming SAEs
Literature review
Data Mining
Potential safety signals will be
further evaluated
42
Vaccine Recipients
Voluntary Reporting
• Spontaneous reports
• Solicited reports from V-SAFE
program
Vaccination Providers
Vaccine EUA Sponsor
Mandatory Reporting
Monthly Periodic Safety
Reports
• Analysis of aggregate AE data
• Newly identified safety
concerns
• Vaccination administration errors
(providers only)
• Serious adverse events (SAEs)
• Multisystem Inflammatory
Syndrome in adults
• Cases of COVID-19 that result in
hospitalization or death
• Review of all Adverse Events of
Special Interest (AESI)
• Data Abstraction
Coordination
Data Sharing
•
•
•
•
Screening of all incoming SAEs
Literature review
Data Mining
Potential safety signals will be
further evaluated
42