よむ、つかう、まなぶ。
【資料1-2】認証基準(告示)改正案 (15 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_28311.html |
| 出典情報 | 薬事・食品衛生審議会 医療機器・体外診断薬部会(令和4年度第6回 10/3)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
単回使用眼内照明プローブ認証基準(案)
(別表第三)
基 準
医療機器の名称(一般的名称)
1 単回使用眼内照明プローブ
日本産業規格又は
国際電気標準会議
使用目的又は効果
が定める規格
T 0993-1
眼科手術において、眼内照明
等に用いること。
ただし、形状、構造及び原理、使用方法及び操作方法若しくは性能等が既存の医療機
器と明らかに異なるときは、本基準は適用しない。
日本産業規格
T 0993-1:医療機器の生物学的評価-第 1 部:リスクマネジメントプロセスにおける
評価及び試験
(参考)一般的名称の定義
一般的名称
定
義
(JMDN コード)
単回使用眼内照明プロ 眼科手術を行う際に、眼内に挿入し、接続先の照明器等の光
ーブ
源の光を導き、眼内照明するために用いる眼内プローブをい
(新規制定案)
う。例えば、先端部にピック等を備えるものもある。本品は
単回使用である。
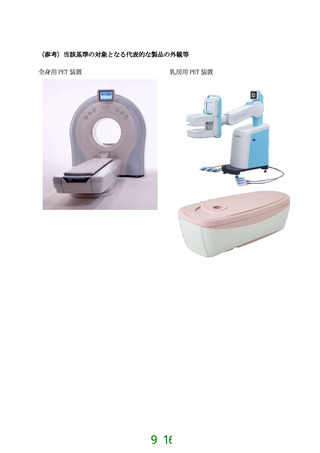
(参考)当該基準の対象となる代表的な製品の外観等
15/16
(別表第三)
基 準
医療機器の名称(一般的名称)
1 単回使用眼内照明プローブ
日本産業規格又は
国際電気標準会議
使用目的又は効果
が定める規格
T 0993-1
眼科手術において、眼内照明
等に用いること。
ただし、形状、構造及び原理、使用方法及び操作方法若しくは性能等が既存の医療機
器と明らかに異なるときは、本基準は適用しない。
日本産業規格
T 0993-1:医療機器の生物学的評価-第 1 部:リスクマネジメントプロセスにおける
評価及び試験
(参考)一般的名称の定義
一般的名称
定
義
(JMDN コード)
単回使用眼内照明プロ 眼科手術を行う際に、眼内に挿入し、接続先の照明器等の光
ーブ
源の光を導き、眼内照明するために用いる眼内プローブをい
(新規制定案)
う。例えば、先端部にピック等を備えるものもある。本品は
単回使用である。
(参考)当該基準の対象となる代表的な製品の外観等
15/16
関連画像
ページ内で利用されている画像ファイルです。
有料会員登録をして頂くことで、このページ内で利用されている画像を個別に閲覧・ダウンロードすることができるようになります。
有料会員登録のお問い合わせはこちらから。