よむ、つかう、まなぶ。
資料1-1-1 予防接種法に基づく医療機関からの副反応疑い報告状況について (5 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000208910_00056.html |
| 出典情報 | 第89回厚生科学審議会予防接種・ワクチン分科会副反応検討部会、令和4年度第21回薬事・食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会(合同開催)(12/16)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
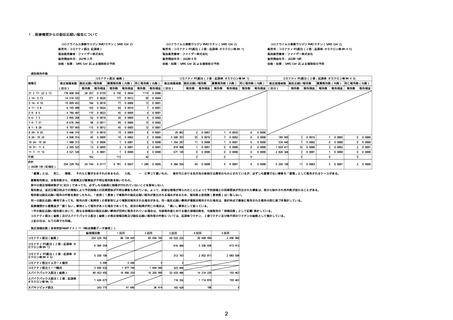
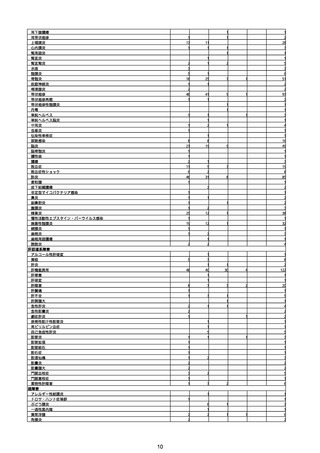
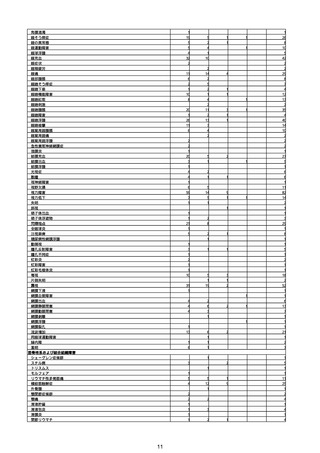
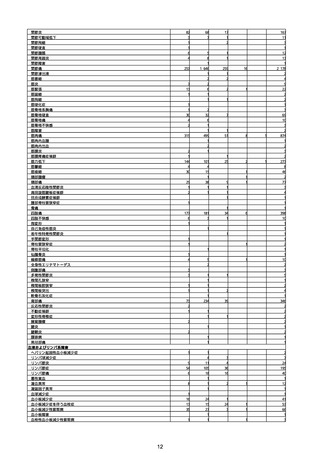
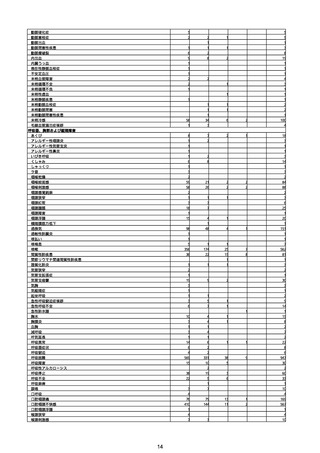
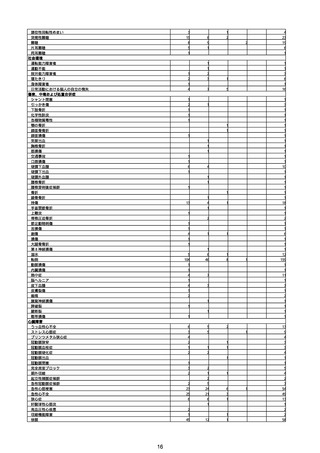
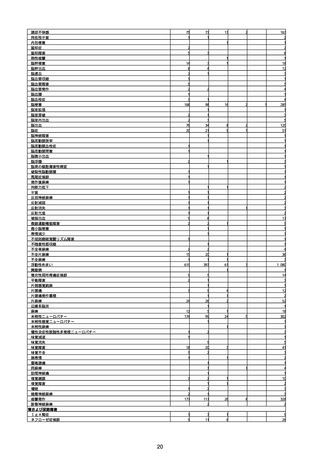
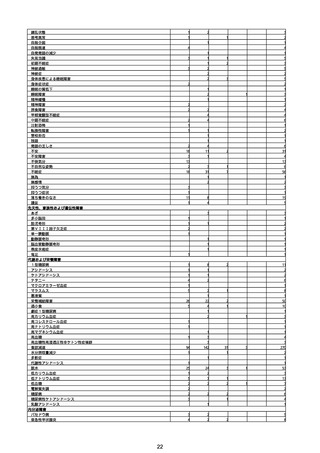
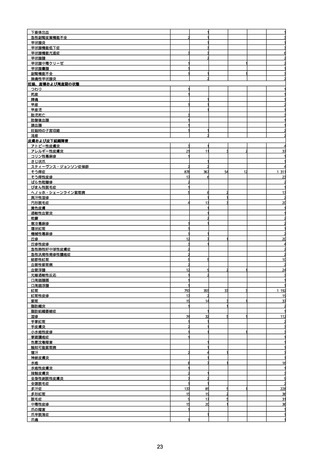
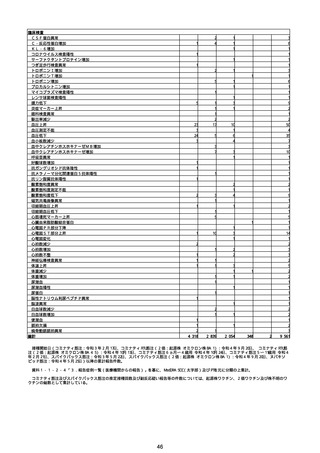
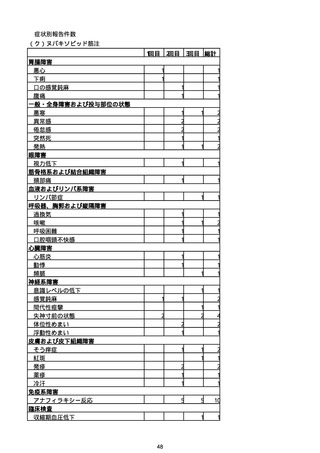
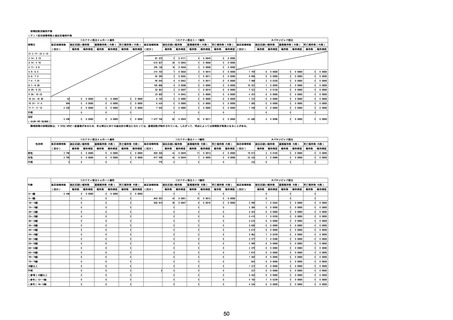
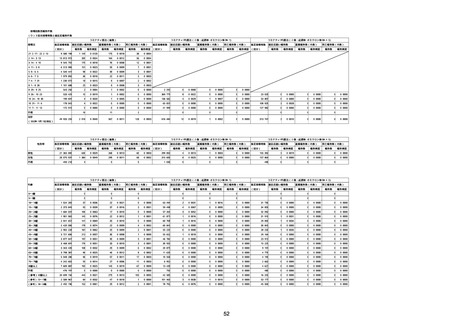
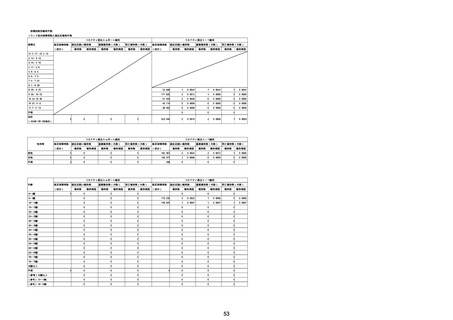
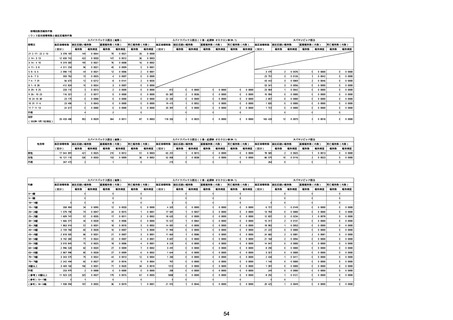
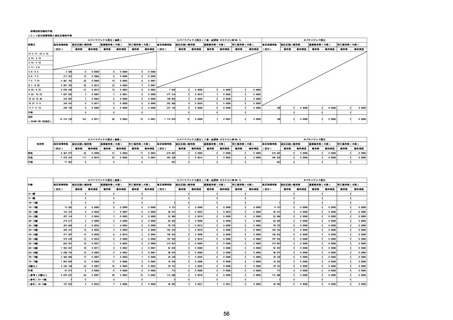
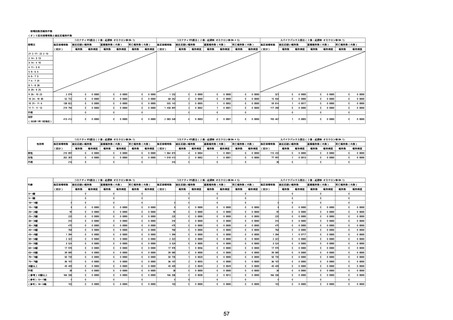
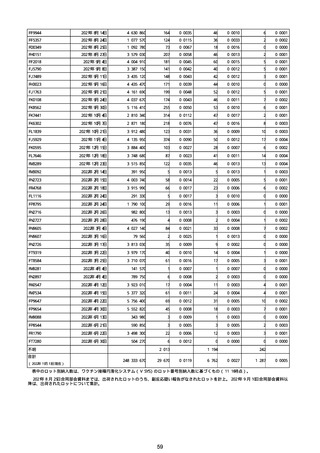
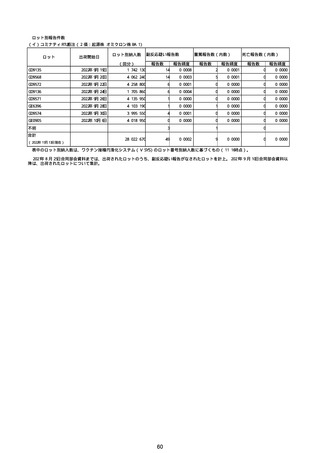
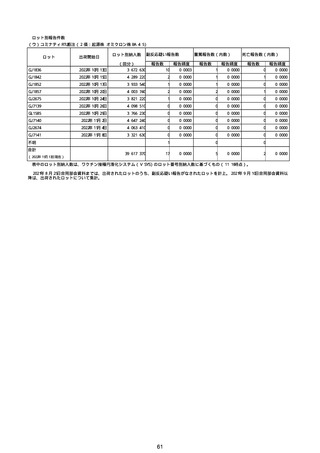
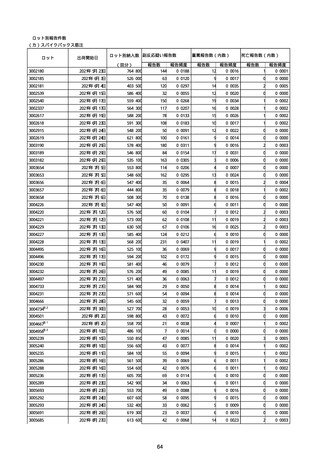
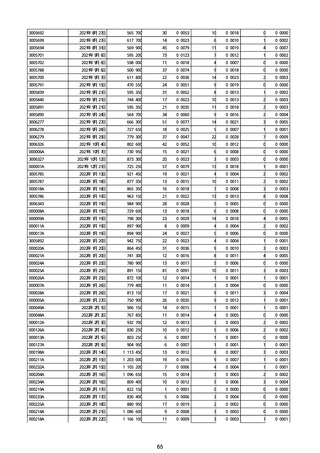
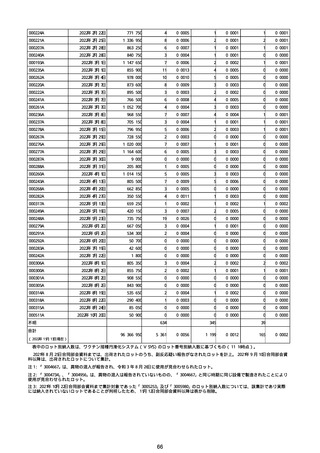
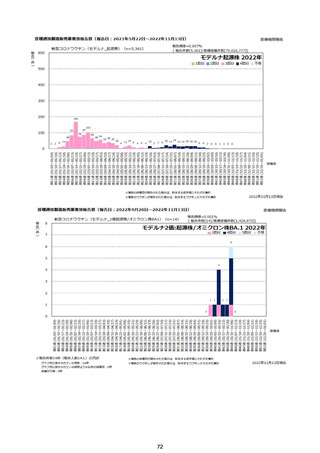
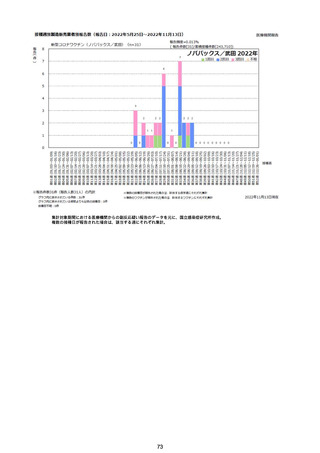
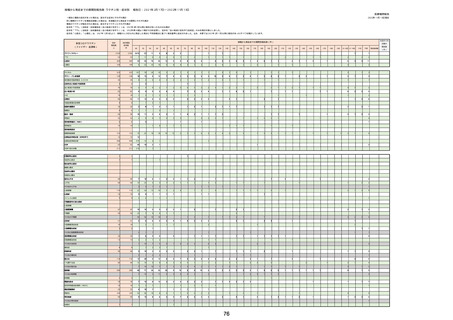
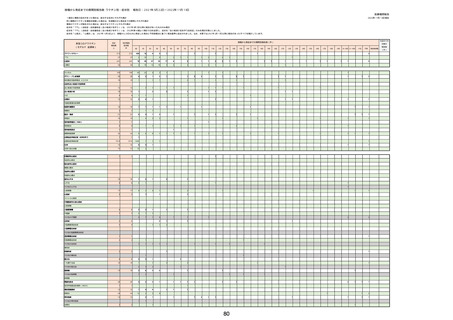
②副反応疑い報告の報告基準別報告件数
コミナティRTU筋注
コミナティRTU筋注
(2価:起源株/オミクロン (2価:起源株/オミクロン
株BA.1)
株BA.4-5)
コミナティ筋注(総数)
アナフィラキシー
コミナティ筋注
6ヵ月〜4歳用
コミナティ筋注
5〜11歳用
2,770
5
1
0
10
53
0
0
0
0
心筋炎
142
2
0
0
6
心膜炎
47
0
1
0
2
1
0
0
0
0
TTS
熱性痙攣
スパイクバックス筋注
(2価:起源株/オミクロン
株BA.1)
スパイクバックス筋注
(総数)
アナフィラキシー
ヌバキソビッド筋注
514
1
10
TTS
27
0
0
心筋炎
95
0
1
心膜炎
27
0
0
0
0
0
熱性痙攣
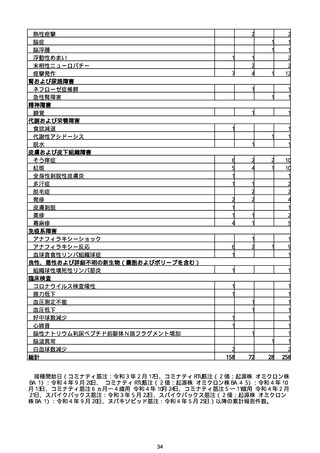
※接種開始日(コミナティ筋注:令和3年2月17日、コミナティRTU筋注(2価:起源株/オミクロン株BA.1):令和4年9月20日、 コミナティRTU筋注(2価:起源株/オミ
クロン株BA.4-5):令和4年10月13日、コミナティ筋注6ヵ月〜4歳用:令和4年10月24日、コミナティ筋注5〜11歳用:令和4年2月21日、スパイクバックス筋注:令和3
年5月22日、スパイクバックス筋注(2価:起源株/オミクロン株BA.1):令和4年9月20日、ヌバキソビッド筋注:令和4年5月25日)以降の累計報告件数。TTSは、いず
れのワクチンも令和3年8月3日以降に第一報の報告がなされたものの累計件数。心筋炎及び心膜炎は、いずれのワクチンも令和3年12月6日以降に第一報の報告がなされ
たものの累計件数。熱性痙攣は、いずれのワクチンも令和4年10月24日以降に第一報の報告がなされたものの累計件数。
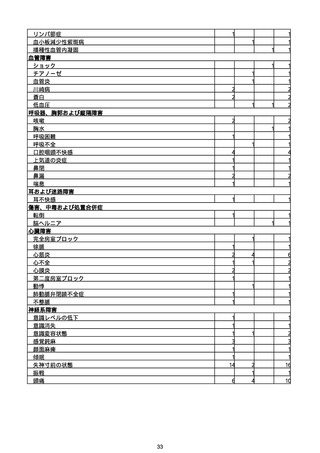
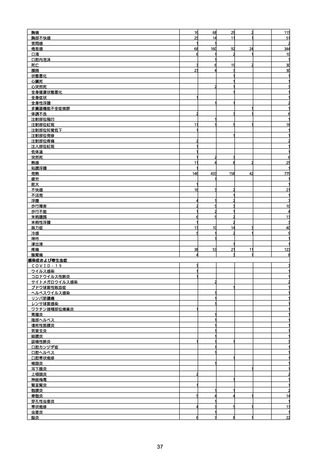
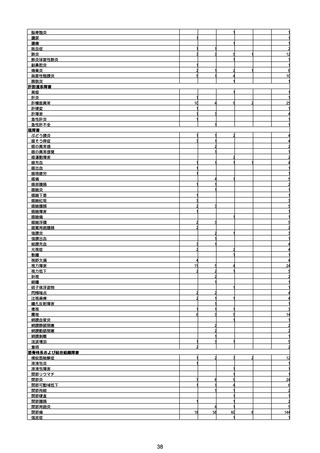
※予防接種後副反応疑い報告書の別紙様式1の報告基準に記載のある症状(「その他の反応」は除く。)について、報告状況をもとに集計を行った。
※アナフィラキシー、心筋炎又は心膜炎、TTS事例として医療機関から報告されたものを集計したものであり、ブライトン分類による評価を経て集計したものではない。ブラ
イトン分類でレベル4又は5と分類されたものを含む。
※TTS:血栓症(血栓塞栓症を含む。)(血小板減少症を伴うものに限る。)
なお、集計対象のMedDRA PT(ver.25.1)は以下のとおり。
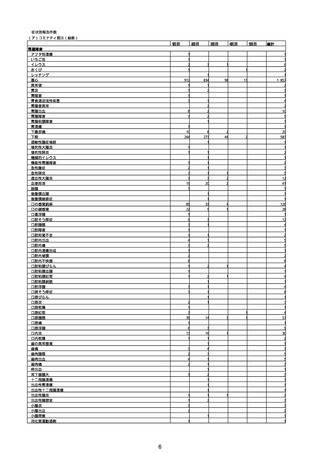
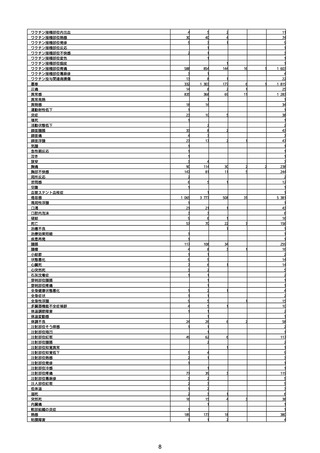
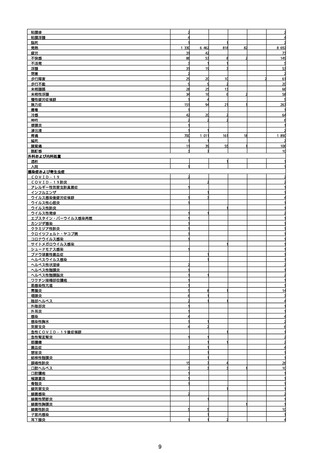
【アナフィラキシー】:アナフィラキシーショック、アナフィラキシー様ショック、アナフィラキシー反応、アナフィラキシー様反応
【TTS】:血小板減少症を伴う血栓症
【心筋炎】:免疫性心筋炎、好酸球性心筋炎、巨細胞性心筋炎、心筋炎、自己免疫性心筋炎、心筋心膜炎
【心膜炎】:心膜炎、胸膜心膜炎、自己免疫性心膜炎、免疫性心膜炎
【熱性痙攣】:熱性痙攣
5
コミナティRTU筋注
コミナティRTU筋注
(2価:起源株/オミクロン (2価:起源株/オミクロン
株BA.1)
株BA.4-5)
コミナティ筋注(総数)
アナフィラキシー
コミナティ筋注
6ヵ月〜4歳用
コミナティ筋注
5〜11歳用
2,770
5
1
0
10
53
0
0
0
0
心筋炎
142
2
0
0
6
心膜炎
47
0
1
0
2
1
0
0
0
0
TTS
熱性痙攣
スパイクバックス筋注
(2価:起源株/オミクロン
株BA.1)
スパイクバックス筋注
(総数)
アナフィラキシー
ヌバキソビッド筋注
514
1
10
TTS
27
0
0
心筋炎
95
0
1
心膜炎
27
0
0
0
0
0
熱性痙攣
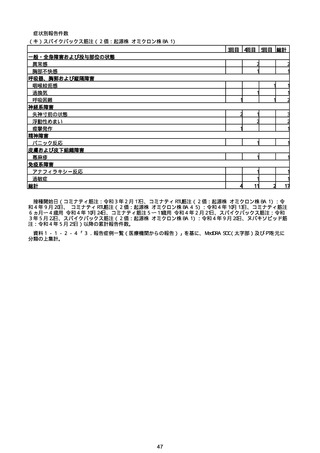
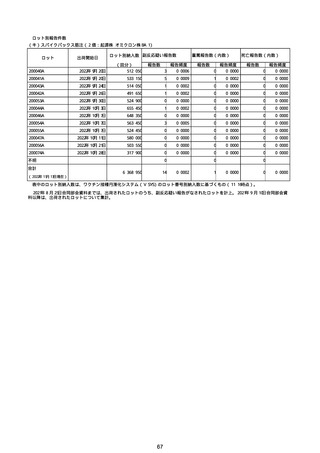
※接種開始日(コミナティ筋注:令和3年2月17日、コミナティRTU筋注(2価:起源株/オミクロン株BA.1):令和4年9月20日、 コミナティRTU筋注(2価:起源株/オミ
クロン株BA.4-5):令和4年10月13日、コミナティ筋注6ヵ月〜4歳用:令和4年10月24日、コミナティ筋注5〜11歳用:令和4年2月21日、スパイクバックス筋注:令和3
年5月22日、スパイクバックス筋注(2価:起源株/オミクロン株BA.1):令和4年9月20日、ヌバキソビッド筋注:令和4年5月25日)以降の累計報告件数。TTSは、いず
れのワクチンも令和3年8月3日以降に第一報の報告がなされたものの累計件数。心筋炎及び心膜炎は、いずれのワクチンも令和3年12月6日以降に第一報の報告がなされ
たものの累計件数。熱性痙攣は、いずれのワクチンも令和4年10月24日以降に第一報の報告がなされたものの累計件数。
※予防接種後副反応疑い報告書の別紙様式1の報告基準に記載のある症状(「その他の反応」は除く。)について、報告状況をもとに集計を行った。
※アナフィラキシー、心筋炎又は心膜炎、TTS事例として医療機関から報告されたものを集計したものであり、ブライトン分類による評価を経て集計したものではない。ブラ
イトン分類でレベル4又は5と分類されたものを含む。
※TTS:血栓症(血栓塞栓症を含む。)(血小板減少症を伴うものに限る。)
なお、集計対象のMedDRA PT(ver.25.1)は以下のとおり。
【アナフィラキシー】:アナフィラキシーショック、アナフィラキシー様ショック、アナフィラキシー反応、アナフィラキシー様反応
【TTS】:血小板減少症を伴う血栓症
【心筋炎】:免疫性心筋炎、好酸球性心筋炎、巨細胞性心筋炎、心筋炎、自己免疫性心筋炎、心筋心膜炎
【心膜炎】:心膜炎、胸膜心膜炎、自己免疫性心膜炎、免疫性心膜炎
【熱性痙攣】:熱性痙攣
5