よむ、つかう、まなぶ。
資料2-2 第Ⅳ回要望に係る専門作業班(WG)の検討状況の概要等について (15 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00025.html |
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第53回 12/21)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
No.
要望番号
成分名
14
Ⅳ-62
ロムスチン(CCNU)
15
Ⅳ-39
チオテパ
17
Ⅳ-97
カルボプラチン
要請内容
要望者
会社名
未承認薬
適応外薬
の分類
小児WG
開発要請に対する企業見解
(概略)注
検討状況等
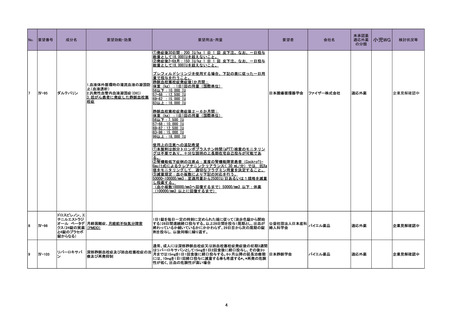
当該医薬品は「新有効成分含有医薬品」
に該当し、承認申請において日本人にお
ける当該医薬品の有効性及び安全性を
より慎重に評価する必要があり、その際
に日本人を対象とした臨床試験成績は必
要である。
詳細な試験計画については、これまでに
得られた情報を整理し、実施可能性も考
慮した上で機構と治験相談等を実施する
ことを推奨する。
なお、開発方針について、以下の点に留
意すること。
要望書の内容、海外診療ガイドライン等
を踏まえると、少なくとも①再発例におけ
るロムスチン単独投与及び②切除術等施
行後の患者を対象としたロムスチンと他
剤との併用投与の2つについて開発する
ことが望ましいこと。
英国の承認内容のうち、120 mg/m2の
設定根拠となる臨床試験成績が、企業見
解からは確認できないことから、当該用
法・用量の適切性については英国での承
認の経緯も含めて確認・検討する必要が
あること。
神経膠腫
日本脳腫瘍学会
medac Pharma
未承認薬
公知申請を希望する。
中枢神経系リンパ腫(原発性およびその
他のリンパ腫の中枢神経系浸潤を含む)
頭頸部癌, 肺小細胞癌, 睾丸腫瘍, 卵巣
癌, 子宮頸癌, 悪性リンパ腫, 非小細胞肺
癌, 乳癌, 子宮体癌
日本リンパ網内系
学会
大日本住友製薬株
式会社
適応外薬
公知申請を希望する。
企業見解確認中
公益社団法人日本 ブリストル・マイヤー
適応外薬
臨床腫瘍学会
ズスクイブ株式会社
公知申請を希望する。
企業見解確認中
注)提出された企業見解より適宜抜粋した。
11
未承認薬
1
適応外薬
14
迅速実用化
1
合計
16
要望番号
成分名
14
Ⅳ-62
ロムスチン(CCNU)
15
Ⅳ-39
チオテパ
17
Ⅳ-97
カルボプラチン
要請内容
要望者
会社名
未承認薬
適応外薬
の分類
小児WG
開発要請に対する企業見解
(概略)注
検討状況等
当該医薬品は「新有効成分含有医薬品」
に該当し、承認申請において日本人にお
ける当該医薬品の有効性及び安全性を
より慎重に評価する必要があり、その際
に日本人を対象とした臨床試験成績は必
要である。
詳細な試験計画については、これまでに
得られた情報を整理し、実施可能性も考
慮した上で機構と治験相談等を実施する
ことを推奨する。
なお、開発方針について、以下の点に留
意すること。
要望書の内容、海外診療ガイドライン等
を踏まえると、少なくとも①再発例におけ
るロムスチン単独投与及び②切除術等施
行後の患者を対象としたロムスチンと他
剤との併用投与の2つについて開発する
ことが望ましいこと。
英国の承認内容のうち、120 mg/m2の
設定根拠となる臨床試験成績が、企業見
解からは確認できないことから、当該用
法・用量の適切性については英国での承
認の経緯も含めて確認・検討する必要が
あること。
神経膠腫
日本脳腫瘍学会
medac Pharma
未承認薬
公知申請を希望する。
中枢神経系リンパ腫(原発性およびその
他のリンパ腫の中枢神経系浸潤を含む)
頭頸部癌, 肺小細胞癌, 睾丸腫瘍, 卵巣
癌, 子宮頸癌, 悪性リンパ腫, 非小細胞肺
癌, 乳癌, 子宮体癌
日本リンパ網内系
学会
大日本住友製薬株
式会社
適応外薬
公知申請を希望する。
企業見解確認中
公益社団法人日本 ブリストル・マイヤー
適応外薬
臨床腫瘍学会
ズスクイブ株式会社
公知申請を希望する。
企業見解確認中
注)提出された企業見解より適宜抜粋した。
11
未承認薬
1
適応外薬
14
迅速実用化
1
合計
16