よむ、つかう、まなぶ。
総-3-2○最適使用推進ガイドラインについて (13 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000212500_00177.html |
| 出典情報 | 中央社会保険医療協議会 総会(第540回 3/8)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
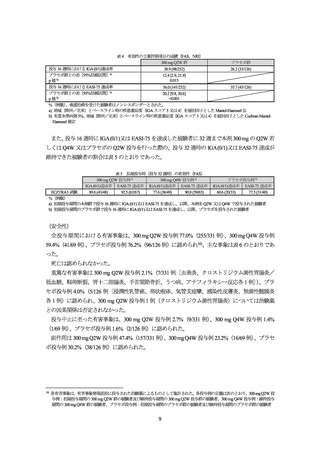
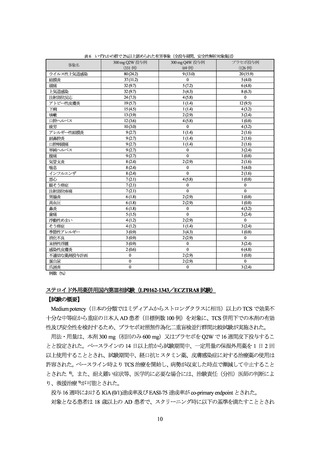
表 8 いずれかの群で 2%以上に認められた有害事象(安全性解析対象集団)
300 mg Q2W 群
プラセボ群
事象名
(53 例)
(53 例)
ざ瘡
6 (11.3)
4 (7.5)
注射部位反応
5 (9.4)
0
上咽頭炎
3 (5.7)
5 (9.4)
注射部位紅斑
3 (5.7)
0
発熱
3 (5.7)
0
季節性アレルギー
3 (5.7)
0
蕁麻疹
2 (3.8)
2 (3.8)
便秘
2 (3.8)
1 (1.9)
背部痛
2 (3.8)
1 (1.9)
胃炎
2 (3.8)
0
麦粒腫
2 (3.8)
0
蜂巣炎
1 (1.9)
2 (3.8)
アトピー性皮膚炎
0
2 (3.8)
失神寸前の状態
0
2 (3.8)
例数(%)
12
300 mg Q2W 群
プラセボ群
事象名
(53 例)
(53 例)
ざ瘡
6 (11.3)
4 (7.5)
注射部位反応
5 (9.4)
0
上咽頭炎
3 (5.7)
5 (9.4)
注射部位紅斑
3 (5.7)
0
発熱
3 (5.7)
0
季節性アレルギー
3 (5.7)
0
蕁麻疹
2 (3.8)
2 (3.8)
便秘
2 (3.8)
1 (1.9)
背部痛
2 (3.8)
1 (1.9)
胃炎
2 (3.8)
0
麦粒腫
2 (3.8)
0
蜂巣炎
1 (1.9)
2 (3.8)
アトピー性皮膚炎
0
2 (3.8)
失神寸前の状態
0
2 (3.8)
例数(%)
12