よむ、つかう、まなぶ。
総-3-2○最適使用推進ガイドラインについて (7 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000212500_00177.html |
| 出典情報 | 中央社会保険医療協議会 総会(第540回 3/8)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
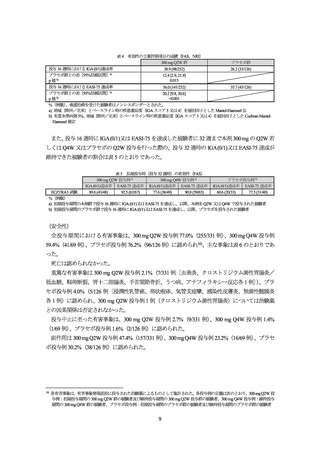
表 2 長期投与時(投与 52 週時)の有効性(FAS)
300 mg Q2W 投与例
300 mg Q4W 投与例
IGA (0/1)達成率 EASI-75 達成率 IGA (0/1)達成率 EASI-75 達成率
51.3 (20/39)
59.6 (28/47)
38.9 (14/36)
49.1 (28/57)
プラセボ投与例
IGA (0/1)達成率 EASI-75 達成率
47.4 (9/19)
33.3 (10/30)
ECZTRA1 試験
%(例数)
初期投与期間の本剤群で投与 16 週時に IGA (0/1)又は EASI-75 を達成し、以降、本剤を Q2W 若しくは Q4W 又はプラセボを Q2W
で投与された被験者
(安全性)
全投与期間における有害事象は、300 mg Q2W 投与例 77.7%(468/602 例)
、300 mg Q4W 投
与例 69.7%(53/76 例)
、非盲検投与例(300 mg Q2W+TCS〔任意〕
)77.3%(435/563 例)
、
プラセボ投与例 78.4%(181/231 例)に認められ6)、主な事象は表 3 のとおりであった。
死亡は認めなかった。
重篤な有害事象は、300 mg Q2W 投与例 4.0%(24/602 例〔アトピー性皮膚炎 4 例、全身性剥
脱性皮膚炎 2 例、急性左室不全、蜂巣炎、注射部位反応、喘息、高血圧性脳症、多発骨折/嵌頓臍
ヘルニア、心臓副伝導路、上肢骨折、末梢動脈狭窄、自然気胸、鹿角状結石、アルコール中毒、リ
ーシュマニア症、気管支炎、多汗症、好酸球増加症、心房細動、憩室炎各 1 例〕
)
、300 mg Q4W 投
与例 3.9%(3/76 例〔自然気胸、椎間板突出、喘息/肺炎各 1 例〕
)、非盲検投与例 4.8%(27/563
例〔急性心筋梗塞、浸潤性乳癌、アトピー性皮膚炎各 2 例、高カリウム血症、高血糖、急性
心筋梗塞/大動脈弁狭窄、脱水/失神、手根管症候群、血胸、水晶体脱臼、運動失調、卵巣
囊胞破裂、蜂巣炎/静脈血栓症、潰瘍性角膜炎、肝炎、肩回旋筋腱板症候群、好酸球増加症、
皮膚筋炎、蜂巣炎、肉芽腫、細菌性胃腸炎、肝障害、膀胱炎、せつ各 1 例〕
)、プラセボ投与
例 3.9%(9/231 例〔喘息 2 例、気管支炎、深部静脈血栓症、進行性高血圧、全身性剥脱性皮膚炎、
変形性関節症/リウマチ性多発筋痛/変形性脊椎症、慢性閉塞性肺疾患、アトピー性皮膚炎/丹毒
各 1 例〕
)に認められ、300 mg Q2W 投与例 7 例(注射部位反応、喘息、全身性剥脱性皮膚炎、リ
ーシュマニア症、気管支炎、多汗症、好酸球増加症各 1 例)
、非盲検投与例 11 例(浸潤性乳癌 2
例、蜂巣炎/静脈血栓症、潰瘍性角膜炎、肝炎、好酸球増加症、皮膚筋炎、蜂巣炎、膀胱炎、
せつ、アトピー性皮膚炎各 1 例)については治験薬との因果関係は否定されなかった。
投与中止に至った有害事象は、300 mg Q2W 投与例 3.5%(21/602 例)
、300 mg Q4W 投与
例 1.3%(1/76 例)
、非盲検投与例 3.0%(17/563 例)
、プラセボ投与例 3.5%(8/231 例)に認
められた。
副作用は、300 mg Q2W 投与例 34.1%(205/602 例)
、300 mg Q4W 投与例 28.9%(22/76 例)
、
非盲検投与例 34.8%(196/563 例)
、プラセボ投与例 31.6%(73/231 例)に認められた。
6)
各有害事象は、有害事象発現直前に投与された治験薬によるものとして集計された。各投与例の定義は次のとおり。300 mg Q2W 投
与例:初期投与期間の 300 mg Q2W 群の被験者及び維持投与期間の 300 mg Q2W 投与群の被験者、300 mg Q4W 投与例:維持投与期
間の 300 mg Q4W 群の被験者、プラセボ投与例:初期投与期間のプラセボ群の被験者及び維持投与期間のプラセボ群の被験者、非
盲検投与例:維持投与期間に非盲検下で 300 mg Q2W(必要に応じて TCS 併用)の投与を受けた被験者
6
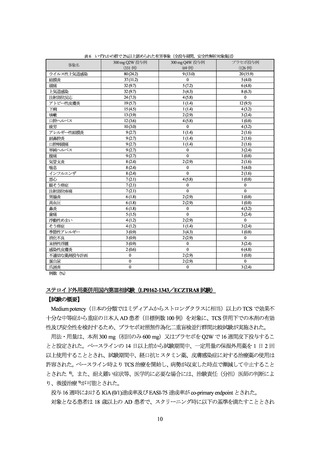
300 mg Q2W 投与例
300 mg Q4W 投与例
IGA (0/1)達成率 EASI-75 達成率 IGA (0/1)達成率 EASI-75 達成率
51.3 (20/39)
59.6 (28/47)
38.9 (14/36)
49.1 (28/57)
プラセボ投与例
IGA (0/1)達成率 EASI-75 達成率
47.4 (9/19)
33.3 (10/30)
ECZTRA1 試験
%(例数)
初期投与期間の本剤群で投与 16 週時に IGA (0/1)又は EASI-75 を達成し、以降、本剤を Q2W 若しくは Q4W 又はプラセボを Q2W
で投与された被験者
(安全性)
全投与期間における有害事象は、300 mg Q2W 投与例 77.7%(468/602 例)
、300 mg Q4W 投
与例 69.7%(53/76 例)
、非盲検投与例(300 mg Q2W+TCS〔任意〕
)77.3%(435/563 例)
、
プラセボ投与例 78.4%(181/231 例)に認められ6)、主な事象は表 3 のとおりであった。
死亡は認めなかった。
重篤な有害事象は、300 mg Q2W 投与例 4.0%(24/602 例〔アトピー性皮膚炎 4 例、全身性剥
脱性皮膚炎 2 例、急性左室不全、蜂巣炎、注射部位反応、喘息、高血圧性脳症、多発骨折/嵌頓臍
ヘルニア、心臓副伝導路、上肢骨折、末梢動脈狭窄、自然気胸、鹿角状結石、アルコール中毒、リ
ーシュマニア症、気管支炎、多汗症、好酸球増加症、心房細動、憩室炎各 1 例〕
)
、300 mg Q4W 投
与例 3.9%(3/76 例〔自然気胸、椎間板突出、喘息/肺炎各 1 例〕
)、非盲検投与例 4.8%(27/563
例〔急性心筋梗塞、浸潤性乳癌、アトピー性皮膚炎各 2 例、高カリウム血症、高血糖、急性
心筋梗塞/大動脈弁狭窄、脱水/失神、手根管症候群、血胸、水晶体脱臼、運動失調、卵巣
囊胞破裂、蜂巣炎/静脈血栓症、潰瘍性角膜炎、肝炎、肩回旋筋腱板症候群、好酸球増加症、
皮膚筋炎、蜂巣炎、肉芽腫、細菌性胃腸炎、肝障害、膀胱炎、せつ各 1 例〕
)、プラセボ投与
例 3.9%(9/231 例〔喘息 2 例、気管支炎、深部静脈血栓症、進行性高血圧、全身性剥脱性皮膚炎、
変形性関節症/リウマチ性多発筋痛/変形性脊椎症、慢性閉塞性肺疾患、アトピー性皮膚炎/丹毒
各 1 例〕
)に認められ、300 mg Q2W 投与例 7 例(注射部位反応、喘息、全身性剥脱性皮膚炎、リ
ーシュマニア症、気管支炎、多汗症、好酸球増加症各 1 例)
、非盲検投与例 11 例(浸潤性乳癌 2
例、蜂巣炎/静脈血栓症、潰瘍性角膜炎、肝炎、好酸球増加症、皮膚筋炎、蜂巣炎、膀胱炎、
せつ、アトピー性皮膚炎各 1 例)については治験薬との因果関係は否定されなかった。
投与中止に至った有害事象は、300 mg Q2W 投与例 3.5%(21/602 例)
、300 mg Q4W 投与
例 1.3%(1/76 例)
、非盲検投与例 3.0%(17/563 例)
、プラセボ投与例 3.5%(8/231 例)に認
められた。
副作用は、300 mg Q2W 投与例 34.1%(205/602 例)
、300 mg Q4W 投与例 28.9%(22/76 例)
、
非盲検投与例 34.8%(196/563 例)
、プラセボ投与例 31.6%(73/231 例)に認められた。
6)
各有害事象は、有害事象発現直前に投与された治験薬によるものとして集計された。各投与例の定義は次のとおり。300 mg Q2W 投
与例:初期投与期間の 300 mg Q2W 群の被験者及び維持投与期間の 300 mg Q2W 投与群の被験者、300 mg Q4W 投与例:維持投与期
間の 300 mg Q4W 群の被験者、プラセボ投与例:初期投与期間のプラセボ群の被験者及び維持投与期間のプラセボ群の被験者、非
盲検投与例:維持投与期間に非盲検下で 300 mg Q2W(必要に応じて TCS 併用)の投与を受けた被験者
6