よむ、つかう、まなぶ。
薬-2別添○関係業界からの意見聴取について (5 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000212451_00065.html |
| 出典情報 | 中央社会保険医療協議会 薬価専門部会(第203回 7/5)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
Ⅰ 市場実勢価格に基づく薬価改定の見直し
1. 中期的な検討課題:市場実勢価格に基づく薬価改定方式の見直し
課題認識:
現行の医薬品の流通制度下では薬価差は必然的に発生する。薬価差の是正を目
的に実勢価改定を行えば、価格乖離が調整幅の範囲に収まらない限り、改定の都
度、薬価は必然的に下落する。
特許期間中の新薬を対象に定期的・循環的に下落させる制度をルール化している
のは、主要先進国中日本だけであり、本邦での投資回収,本邦への革新的医薬品
の導入,患者の新薬へのアクセスに負の影響をもたらすとして、改革の必要性が以
前より指摘されてきた。
そうした中、こうした状況の改善を目的に、薬価制度においては、2010 年度に、特許
期間中の新薬の薬価維持を図る「新薬創出・適応外薬解消等促進加算」(以下、
「新薬創出等加算」という)が導入された。この制度導入により、特許期間中の新薬
のうち約 8 割の品目において薬価維持ができるようになり、当時懸念が深まってい
たドラッグ・ラグの問題も解消の方向を見た。併せて、長期収載品の後発医薬品へ
の置き換えが進み、後発医薬品の使用率は 2015 年に政府が新たな目標として設
定した「80%以上」を達成するに至った。
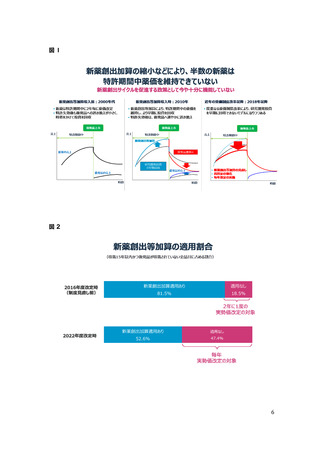
しかしながら、2018 年度の薬価制度の抜本改革において、新薬創出等加算の対象
品目等の大幅な見直しが行われ、新薬創出等加算の対象となる品目数はそれまで
の約 8 割から約 5 割へと後退した。<図 1,図 2> また、企業要件が新たに導入さ
れたことにより、新薬創出等加算の対象であっても、薬価を維持できない品目数が
増加。改定前の薬価を維持できる品目は、特許期間中の新薬全体の約 3 割にまで
減少した。
また、2019 年 10 月の消費税増税時に行われた市場実勢価改定に続き、2021 年
度からは中間年改定が施行され、実勢価改定の影響が再び大きく拡大するようにな
った。2018 年度以降すでに 6 年連続で実勢価改定が行われており、薬価水準は
大きく低下している。<図 3> 今後の医薬品市場見通しにおいて、 主要国の中で日
本のみが市場のマイナス成長が予想される国となっている。<図 4,5>
市場のマイナス成長の主たる要因は薬価の下落にある。<図 6> 特許期間中の新
薬の薬価がこのまま下落する状況が続けば、研究開発投資力を低下させるとともに、
日本の低い薬価がアジア等の他国の薬価算定に直接的・間接的に影響を与える懸
念から、日本で早期に新薬を上市する意欲を削ぐことにつながる。また、新薬の薬価
算定において、著しく低下した既存薬の薬価が基準となる可能性があるため、日本
での新薬上市の阻害要因になる。その他、将来の後発品の薬価水準にも影響し、安
定供給に支障を来す可能性も考えられる。
このように 2018 年度以降の薬価制度の大幅な見直しは、日本市場への投資に負
の影響をもたらしている。現行の薬価制度は、新薬創出サイクルを促進する政策とし
て今や十分に機能しなくなっており、ドラッグ・ラグ/ロスも再燃の兆しを見せている。
制度の大幅な見直しが急務と考える。<図 7~9>
3
1. 中期的な検討課題:市場実勢価格に基づく薬価改定方式の見直し
課題認識:
現行の医薬品の流通制度下では薬価差は必然的に発生する。薬価差の是正を目
的に実勢価改定を行えば、価格乖離が調整幅の範囲に収まらない限り、改定の都
度、薬価は必然的に下落する。
特許期間中の新薬を対象に定期的・循環的に下落させる制度をルール化している
のは、主要先進国中日本だけであり、本邦での投資回収,本邦への革新的医薬品
の導入,患者の新薬へのアクセスに負の影響をもたらすとして、改革の必要性が以
前より指摘されてきた。
そうした中、こうした状況の改善を目的に、薬価制度においては、2010 年度に、特許
期間中の新薬の薬価維持を図る「新薬創出・適応外薬解消等促進加算」(以下、
「新薬創出等加算」という)が導入された。この制度導入により、特許期間中の新薬
のうち約 8 割の品目において薬価維持ができるようになり、当時懸念が深まってい
たドラッグ・ラグの問題も解消の方向を見た。併せて、長期収載品の後発医薬品へ
の置き換えが進み、後発医薬品の使用率は 2015 年に政府が新たな目標として設
定した「80%以上」を達成するに至った。
しかしながら、2018 年度の薬価制度の抜本改革において、新薬創出等加算の対象
品目等の大幅な見直しが行われ、新薬創出等加算の対象となる品目数はそれまで
の約 8 割から約 5 割へと後退した。<図 1,図 2> また、企業要件が新たに導入さ
れたことにより、新薬創出等加算の対象であっても、薬価を維持できない品目数が
増加。改定前の薬価を維持できる品目は、特許期間中の新薬全体の約 3 割にまで
減少した。
また、2019 年 10 月の消費税増税時に行われた市場実勢価改定に続き、2021 年
度からは中間年改定が施行され、実勢価改定の影響が再び大きく拡大するようにな
った。2018 年度以降すでに 6 年連続で実勢価改定が行われており、薬価水準は
大きく低下している。<図 3> 今後の医薬品市場見通しにおいて、 主要国の中で日
本のみが市場のマイナス成長が予想される国となっている。<図 4,5>
市場のマイナス成長の主たる要因は薬価の下落にある。<図 6> 特許期間中の新
薬の薬価がこのまま下落する状況が続けば、研究開発投資力を低下させるとともに、
日本の低い薬価がアジア等の他国の薬価算定に直接的・間接的に影響を与える懸
念から、日本で早期に新薬を上市する意欲を削ぐことにつながる。また、新薬の薬価
算定において、著しく低下した既存薬の薬価が基準となる可能性があるため、日本
での新薬上市の阻害要因になる。その他、将来の後発品の薬価水準にも影響し、安
定供給に支障を来す可能性も考えられる。
このように 2018 年度以降の薬価制度の大幅な見直しは、日本市場への投資に負
の影響をもたらしている。現行の薬価制度は、新薬創出サイクルを促進する政策とし
て今や十分に機能しなくなっており、ドラッグ・ラグ/ロスも再燃の兆しを見せている。
制度の大幅な見直しが急務と考える。<図 7~9>
3