よむ、つかう、まなぶ。
材-4○ 医療機器業界からの意見聴取について (7 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000212455_00033.html |
| 出典情報 | 中央社会保険医療協議会 保険医療材料専門部会(第121回 8/30)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
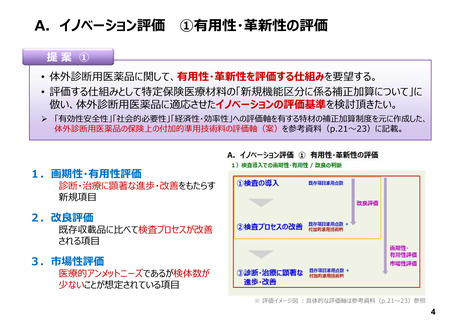
A.イノベーション評価
② 使用実績を踏まえた評価(チャレンジ申請)
背景・現状
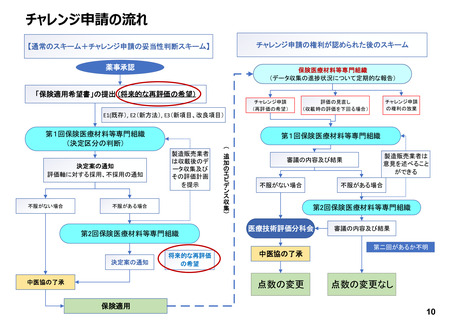
1. 特材について新規C1申請に対し、使用実績を踏まえて保険収載後に再度評価を行うことができる仕組み(チャ
レンジ申請)が創設され、令和4年度には技術料に一体として包括して評価される医療機器に関してもチャレン
ジ申請が導入された(以下参照)。
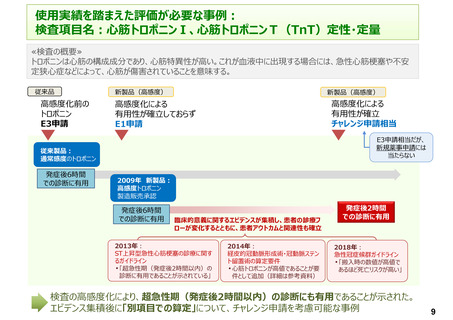
2. 一方、同様に技術料である体外診断用医薬品の再評価は学会提案に基づき行われるが、体外診断用医薬品
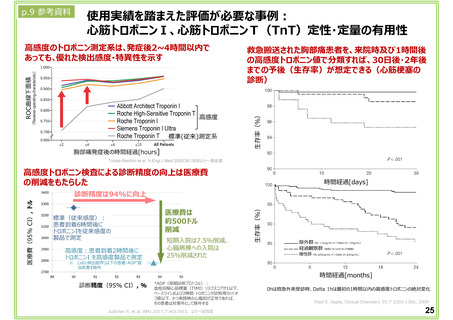
においても検査による患者への臨床的効果等が示される診療報酬項目も存在する(p.9)。 当該技術に関し、
臨床上の有用性が市販後に証明された際は、イノベーションを適切かつ迅速に評価する観点や、体外診断用医
薬品に関する保有情報、関連学会の技術取り扱い状況を総合的に判断し、技術料の再評価を企業から申請す
る方が望ましい場合もある。
C2チャレンジ申請に関する前回改定時の議論
保険医療材料専門部会(令和3年9月22日)
中医協(令和3年12月22日)
令和4年度保険医療材料
制度改革の骨子(案)
技術料に一体として包括して評価される
医療機器についても、製造販売業者が
チャレンジ申請を希望する場合には、保
険医療材料等専門組織でチャレンジ申
請の権利の付与に関する審議を行うこと
ができるようにすることとする。
7
② 使用実績を踏まえた評価(チャレンジ申請)
背景・現状
1. 特材について新規C1申請に対し、使用実績を踏まえて保険収載後に再度評価を行うことができる仕組み(チャ
レンジ申請)が創設され、令和4年度には技術料に一体として包括して評価される医療機器に関してもチャレン
ジ申請が導入された(以下参照)。
2. 一方、同様に技術料である体外診断用医薬品の再評価は学会提案に基づき行われるが、体外診断用医薬品
においても検査による患者への臨床的効果等が示される診療報酬項目も存在する(p.9)。 当該技術に関し、
臨床上の有用性が市販後に証明された際は、イノベーションを適切かつ迅速に評価する観点や、体外診断用医
薬品に関する保有情報、関連学会の技術取り扱い状況を総合的に判断し、技術料の再評価を企業から申請す
る方が望ましい場合もある。
C2チャレンジ申請に関する前回改定時の議論
保険医療材料専門部会(令和3年9月22日)
中医協(令和3年12月22日)
令和4年度保険医療材料
制度改革の骨子(案)
技術料に一体として包括して評価される
医療機器についても、製造販売業者が
チャレンジ申請を希望する場合には、保
険医療材料等専門組織でチャレンジ申
請の権利の付与に関する審議を行うこと
ができるようにすることとする。
7