よむ、つかう、まなぶ。
総-3-1○最適使用推進ガイドラインについて (10 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000212500_00251.html |
| 出典情報 | 中央社会保険医療協議会 総会(第587回 4/10)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
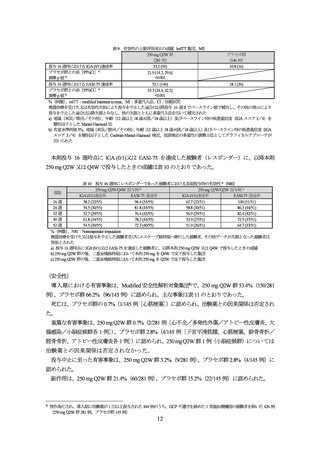
治療6)が可能とされた。
投与 16 週時における IGA (0/1)達成率及び EASI-75 達成率が co-primary endpoint とされた。
対象となる患者は、12 歳以上の AD 患者で、以下の基準を満たすこととされた。
(主な選択基準)
1 年以上前に American Academy of Dermatology Consensus Criteria に基づき AD と診断されてい
る
過去に外用薬治療で効果不十分又は外用薬治療が医学的に推奨されない
ベースライン時の AD による病変が体表面積の 10%以上、EASI スコアが 16 以上及び IGA ス
コアが 3 以上
12 歳以上 18 歳未満の場合は体重が 40 kg 以上
【結果】
(有効性)
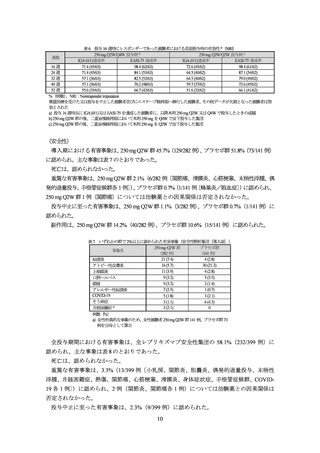
有効性の co-primary endpoint である投与 16 週時における IGA (0/1)達成率及び EASI-75 達成率は表
5 のとおりであり、プラセボ群と 250 mg Q2W 群との対比較において、いずれの評価項目について
も統計学的に有意な差が認められ、プラセボに対する本剤 250 mg Q2W 投与の優越性が検証された。
表 5 有効性の主要評価項目の成績(ITT 集団、MI)
250 mg Q2W 群
(283 例)
投与 16 週時における IGA (0/1)達成率
43.1 (122)
プラセボ群との差[95%CI]a)
29.7 [21.6, 37.8]
<0.001
調整 p 値 b)
プラセボ群
(141 例)
12.7 (18)
投与 16 週時における EASI-75 達成率
58.8 (166)
16.2 (23)
プラセボ群との差[95%CI]a)
42.0 [33.3, 50.6]
<0.001
調整 p 値 b)
%(例数)
、ITT:Intention to treat、MI:多重代入法、CI:信頼区間
救援治療を受けた又は有効性欠如により投与を中止した場合は以降投与 16 週までベースライン値で補完し、その他の理由によ
り投与を中止した場合は以降欠測とみなし、他の欠測とともに多重代入法を用いて補完された
a) 地域(米国/欧州/その他)
、年齢(12 歳以上 18 歳未満/18 歳以上)及びベースライン時の疾患重症度(IGA スコア 3/4)
を層別因子とした Mantel-Haenszel 法
b) 有意水準両側 5%、地域(米国/欧州/その他)
、年齢(12 歳以上 18 歳未満/18 歳以上)及びベースライン時の疾患重症度
(IGA スコア 3/4)を層別因子とした Cochran-Mantel-Haenszel 検定。仮説検定の多重性の調整方法としてグラフィカルアプ
ローチが用いられた
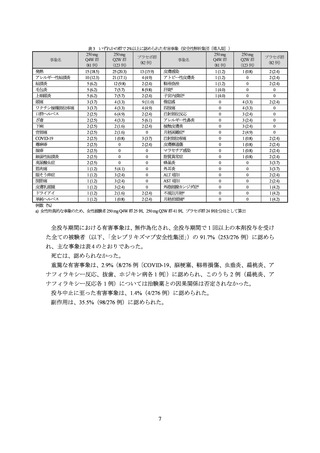
本剤投与 16 週時点に IGA (0/1)又は EASI-75 を達成した被験者(レスポンダー)に、以降本剤
250 mg Q2W 又は Q4W 投与を行った際の成績は表 6 のとおりであった。
6)
導入期では、まずは救援治療として外用薬治療(medium-potency TCS 等)を行うこととされ、全身療法(経口ステロイド、光線療
法、シクロスポリン等)による救援治療が必要となった被験者は、治験薬投与を直ちに中止することとされた。投与 16 週時までに
全身療法による救援治療を受けた被験者は、エスケープ維持期移行前に半減期の 5 倍以上のウォッシュアウト期間を設けることと
された。二重盲検維持期では救援治療として外用薬の間欠的使用が許容され、短期間の全身療法による救援治療が必要な被験者は
個別に評価され、治療開始前に治験依頼者の医学専門家との議論が必要とされた。エスケープ維持期では外用薬による救援治療の
間欠的使用が許容され、短期間の全身療法による救援治療が必要な被験者は個別に評価され、治療開始前に治験依頼者の医学専門
家との議論が必要とされた。また、長期間の全身療法による救援治療が必要とされる被験者は、試験を中止することとされた。
9
投与 16 週時における IGA (0/1)達成率及び EASI-75 達成率が co-primary endpoint とされた。
対象となる患者は、12 歳以上の AD 患者で、以下の基準を満たすこととされた。
(主な選択基準)
1 年以上前に American Academy of Dermatology Consensus Criteria に基づき AD と診断されてい
る
過去に外用薬治療で効果不十分又は外用薬治療が医学的に推奨されない
ベースライン時の AD による病変が体表面積の 10%以上、EASI スコアが 16 以上及び IGA ス
コアが 3 以上
12 歳以上 18 歳未満の場合は体重が 40 kg 以上
【結果】
(有効性)
有効性の co-primary endpoint である投与 16 週時における IGA (0/1)達成率及び EASI-75 達成率は表
5 のとおりであり、プラセボ群と 250 mg Q2W 群との対比較において、いずれの評価項目について
も統計学的に有意な差が認められ、プラセボに対する本剤 250 mg Q2W 投与の優越性が検証された。
表 5 有効性の主要評価項目の成績(ITT 集団、MI)
250 mg Q2W 群
(283 例)
投与 16 週時における IGA (0/1)達成率
43.1 (122)
プラセボ群との差[95%CI]a)
29.7 [21.6, 37.8]
<0.001
調整 p 値 b)
プラセボ群
(141 例)
12.7 (18)
投与 16 週時における EASI-75 達成率
58.8 (166)
16.2 (23)
プラセボ群との差[95%CI]a)
42.0 [33.3, 50.6]
<0.001
調整 p 値 b)
%(例数)
、ITT:Intention to treat、MI:多重代入法、CI:信頼区間
救援治療を受けた又は有効性欠如により投与を中止した場合は以降投与 16 週までベースライン値で補完し、その他の理由によ
り投与を中止した場合は以降欠測とみなし、他の欠測とともに多重代入法を用いて補完された
a) 地域(米国/欧州/その他)
、年齢(12 歳以上 18 歳未満/18 歳以上)及びベースライン時の疾患重症度(IGA スコア 3/4)
を層別因子とした Mantel-Haenszel 法
b) 有意水準両側 5%、地域(米国/欧州/その他)
、年齢(12 歳以上 18 歳未満/18 歳以上)及びベースライン時の疾患重症度
(IGA スコア 3/4)を層別因子とした Cochran-Mantel-Haenszel 検定。仮説検定の多重性の調整方法としてグラフィカルアプ
ローチが用いられた
本剤投与 16 週時点に IGA (0/1)又は EASI-75 を達成した被験者(レスポンダー)に、以降本剤
250 mg Q2W 又は Q4W 投与を行った際の成績は表 6 のとおりであった。
6)
導入期では、まずは救援治療として外用薬治療(medium-potency TCS 等)を行うこととされ、全身療法(経口ステロイド、光線療
法、シクロスポリン等)による救援治療が必要となった被験者は、治験薬投与を直ちに中止することとされた。投与 16 週時までに
全身療法による救援治療を受けた被験者は、エスケープ維持期移行前に半減期の 5 倍以上のウォッシュアウト期間を設けることと
された。二重盲検維持期では救援治療として外用薬の間欠的使用が許容され、短期間の全身療法による救援治療が必要な被験者は
個別に評価され、治療開始前に治験依頼者の医学専門家との議論が必要とされた。エスケープ維持期では外用薬による救援治療の
間欠的使用が許容され、短期間の全身療法による救援治療が必要な被験者は個別に評価され、治療開始前に治験依頼者の医学専門
家との議論が必要とされた。また、長期間の全身療法による救援治療が必要とされる被験者は、試験を中止することとされた。
9