総-1-3○医薬品の新規薬価収載等について (5 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000212500_00254.html |
| 出典情報 | 中央社会保険医療協議会 総会(第589回 5/15)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
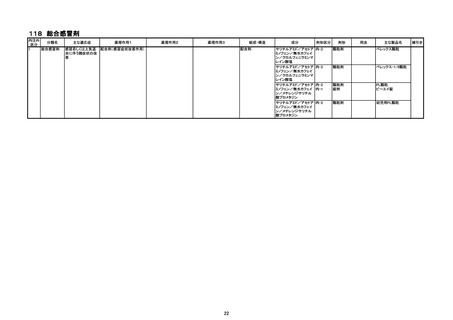
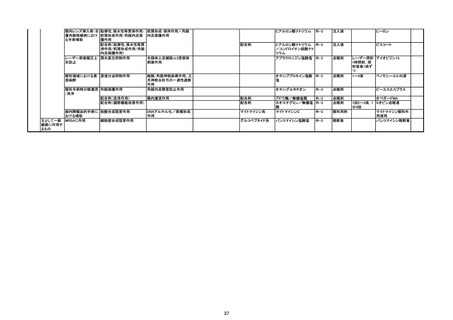
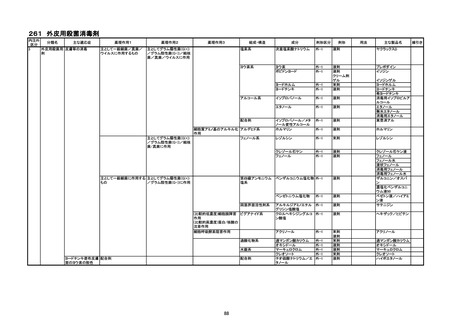
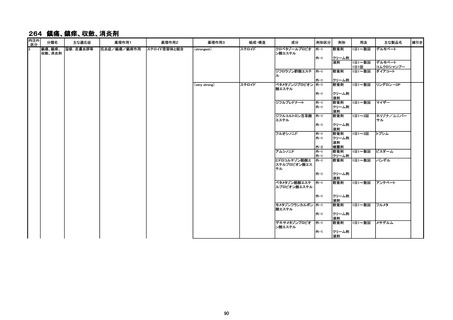
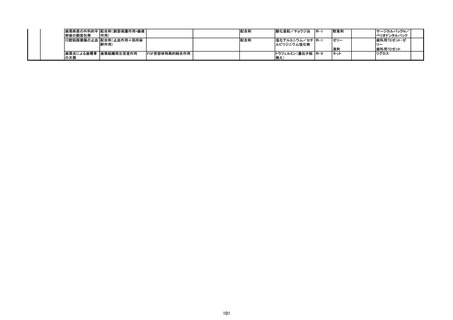
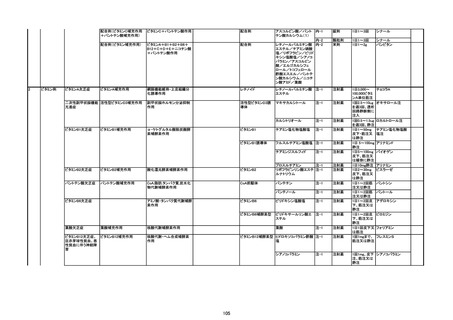
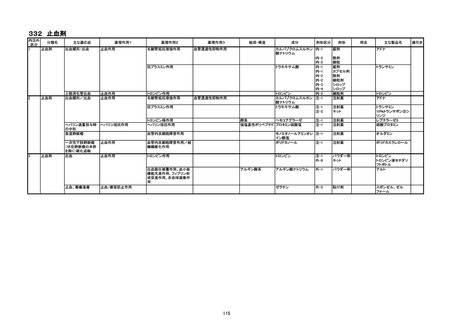
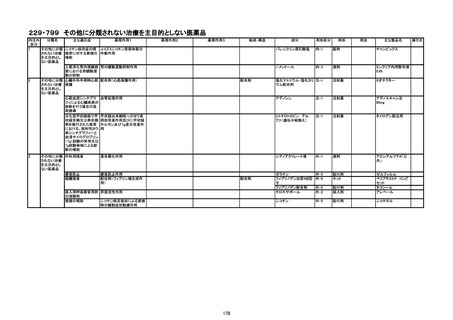
1.内注外区分
1:内用薬
2:注射薬
3:外用薬
2.分類名
原則として、従来の薬効分類名をもとにした。
3.主な適応症
薬事法上の承認に基づく「効能・効果」をもとに簡潔に記載。
但し、「効能・効果」が多岐にわたる場合は、同一「効能・効果」をもつ薬剤が比較的多い「効能・効果」をまとめて、当該
「効能・効果」を「主な適応症」として代表させた。
4.薬理作用1、2、3
添付文書の「薬効薬理」欄の記述をもとに、主な薬理作用を挙げた。同一の薬理作用をもつ薬剤を同一枠内に記載。
5.組成・構造
添付文書等から特徴的な構造群名が用いられていれば記載。配合剤については「配合剤」と記載。
6.成分
添付文書による。
7.剤形区分、剤形
薬価算定上の剤形分類による。
8.用法
特に必要な場合、投与回数等を参考として記載。
9.線引き
以上1~8の項目を勘案して、範疇が異なる領域を線により区分。これが投与経路が同じで薬理作用が類似している薬
理作用類似薬の範囲を示すこととなる。
5