よむ、つかう、まなぶ。
【資料2】テーマ③(国民からの信頼性確保に向けた体外診断用医薬品・医療機器の規制の見直し)について.pdf (16 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_44072.html |
| 出典情報 | 厚生科学審議会 医薬品医療機器制度部会(令和6年度第7回 10/3)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
参考
厚生科学審議会
医薬品医療機器制度部会
三役体制
資料1
令和6年7月25日
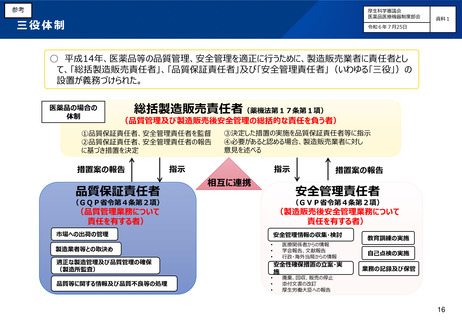
○ 平成14年、医薬品等の品質管理、安全管理を適正に行うために、製造販売業者に責任者とし
て、「総括製造販売責任者」、「品質保証責任者」及び「安全管理責任者」(いわゆる「三役」)の
設置が義務づけられた。
医薬品の場合の
体制
総括製造販売責任者(薬機法第17条第1項)
(品質管理及び製造販売後安全管理の総括的な責任を負う者)
①品質保証責任者、安全管理責任者を監督
②品質保証責任者、安全管理責任者の報告
に基づき措置を決定
措置案の報告
品質保証責任者
③決定した措置の実施を品質保証責任者等に指示
④必要があると認める場合、製造販売業者に対し
意見を述べる
指示
指示
相互に連携
措置案の報告
安全管理責任者
(GQP省令第4条第2項)
(GVP省令第4条第2項)
(品質管理業務について
責任を有する者)
(製造販売後安全管理業務について
責任を有する者)
市場への出荷の管理
製造業者等との取決め
適正な製造管理及び品質管理の確保
(製造所監査)
品質等に関する情報及び品質不良等の処理
安全管理情報の収集・検討
•
•
•
医療関係者からの情報
学会報告、文献報告
行政・海外当局からの情報
安全性確保措置の立案・実
施
•
•
•
教育訓練の実施
自己点検の実施
業務の記録及び保管
廃棄、回収、販売の停止
添付文書の改訂
厚生労働大臣への報告
16
厚生科学審議会
医薬品医療機器制度部会
三役体制
資料1
令和6年7月25日
○ 平成14年、医薬品等の品質管理、安全管理を適正に行うために、製造販売業者に責任者とし
て、「総括製造販売責任者」、「品質保証責任者」及び「安全管理責任者」(いわゆる「三役」)の
設置が義務づけられた。
医薬品の場合の
体制
総括製造販売責任者(薬機法第17条第1項)
(品質管理及び製造販売後安全管理の総括的な責任を負う者)
①品質保証責任者、安全管理責任者を監督
②品質保証責任者、安全管理責任者の報告
に基づき措置を決定
措置案の報告
品質保証責任者
③決定した措置の実施を品質保証責任者等に指示
④必要があると認める場合、製造販売業者に対し
意見を述べる
指示
指示
相互に連携
措置案の報告
安全管理責任者
(GQP省令第4条第2項)
(GVP省令第4条第2項)
(品質管理業務について
責任を有する者)
(製造販売後安全管理業務について
責任を有する者)
市場への出荷の管理
製造業者等との取決め
適正な製造管理及び品質管理の確保
(製造所監査)
品質等に関する情報及び品質不良等の処理
安全管理情報の収集・検討
•
•
•
医療関係者からの情報
学会報告、文献報告
行政・海外当局からの情報
安全性確保措置の立案・実
施
•
•
•
教育訓練の実施
自己点検の実施
業務の記録及び保管
廃棄、回収、販売の停止
添付文書の改訂
厚生労働大臣への報告
16