よむ、つかう、まなぶ。
03【資料1】新型コロナワクチンの接種について (11 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_29727.html |
| 出典情報 | 厚生科学審議会 予防接種・ワクチン分科会(第42回 12/13)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
【1】令和4年秋開始接種に使用するワクチンについて
(1)モデルナ社のオミクロン株対応2価ワクチンの対象年齢について
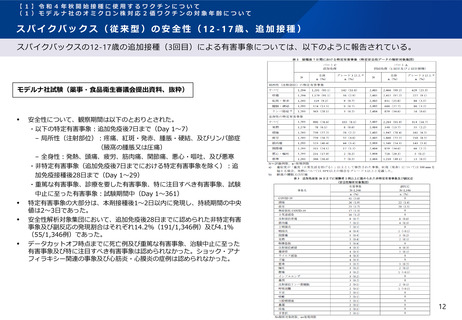
スパイクバックス(従来型)の有効性(12-17歳、追加接種)
スパイクバックスの12-17歳の追加接種(3回目)による免疫原性データについて、18~25歳の被験者データに対する
非劣性が示されたと報告されている。
モデルナ社試験(薬事・食品衛生審議会提出資料、抜粋)
mRNA-1273-P203試験(以下「本試験」という。)は、12~17歳の健
康人(目標例数3,000 例:本剤群約2,000例及びプラセボ群約1,000例)
を対象に、mRNA-1273(1価:起源株)(以下「本剤」という。)の安
全性、免疫原性及び有効性の検討を目的とした無作為化観察者盲検プラセ
ボ対照並行群間比較試験として米国25施設で開始された。
初回免疫(本剤100μgを2回筋肉内接種)を完了し、追加免疫に同意した
1,346例を対象に、初回免疫2回目接種から5カ月以上経過後に本剤を追加
免疫した際の免疫原性及び安全性が検討された。
2022年5月16日にデータカットオフされ、免疫原性及び安全性の解析が
実施された。データカットオフ日時点で、追加免疫後の追跡期間(中央
値)は117日であった。
免疫原性の主要目的は、本剤50μg追加免疫後(Day 29)における、
シュードウイルスに対する血清中和抗体の幾何平均濃度(以下「GMC」
という。)及び中和抗体応答率とされ、本試験の12~17歳の免疫原性に
ついて、mRNA-1273-P301試験(18歳以上の成人を対象とした第Ⅲ相
試験、以下「P301試験」という。)で本剤100μg を初回免疫された18
~25歳の被験者の免疫原性に対する非劣性が評価された。
結果は表1のとおりであり、GMC のGMR の両側95%信頼区間の下限値及
び中和抗体応答率の差の両側95%信頼区間の下限値は、いずれも事前に
設定された非劣性限界値を上回り、またGMCのGMR の点推定値は0.8以
上であり、中和抗体応答率の差の点推定値は−10%を上回ったことから、
本試験の12~17歳の被験者の免疫原性データについて、P301試験の18
~25歳の被験者データに対する非劣性が確認された。
非劣性の成功基準は、(1)「GMC の幾何平均比(本試験(Day 29)のGMC/P301 試験の18~25 歳(Day 57)のGMC)」の95%信頼区間の下限が0.67(1/1.5)を上回り、かつ点推定値が0.8 以上、
(2)中和抗体応答率の差の95%信頼区間の下限が−10%を上回ることとし、これら二つの基準を満たす場合に非劣性が示されたと判断することとされた。
11
(1)モデルナ社のオミクロン株対応2価ワクチンの対象年齢について
スパイクバックス(従来型)の有効性(12-17歳、追加接種)
スパイクバックスの12-17歳の追加接種(3回目)による免疫原性データについて、18~25歳の被験者データに対する
非劣性が示されたと報告されている。
モデルナ社試験(薬事・食品衛生審議会提出資料、抜粋)
mRNA-1273-P203試験(以下「本試験」という。)は、12~17歳の健
康人(目標例数3,000 例:本剤群約2,000例及びプラセボ群約1,000例)
を対象に、mRNA-1273(1価:起源株)(以下「本剤」という。)の安
全性、免疫原性及び有効性の検討を目的とした無作為化観察者盲検プラセ
ボ対照並行群間比較試験として米国25施設で開始された。
初回免疫(本剤100μgを2回筋肉内接種)を完了し、追加免疫に同意した
1,346例を対象に、初回免疫2回目接種から5カ月以上経過後に本剤を追加
免疫した際の免疫原性及び安全性が検討された。
2022年5月16日にデータカットオフされ、免疫原性及び安全性の解析が
実施された。データカットオフ日時点で、追加免疫後の追跡期間(中央
値)は117日であった。
免疫原性の主要目的は、本剤50μg追加免疫後(Day 29)における、
シュードウイルスに対する血清中和抗体の幾何平均濃度(以下「GMC」
という。)及び中和抗体応答率とされ、本試験の12~17歳の免疫原性に
ついて、mRNA-1273-P301試験(18歳以上の成人を対象とした第Ⅲ相
試験、以下「P301試験」という。)で本剤100μg を初回免疫された18
~25歳の被験者の免疫原性に対する非劣性が評価された。
結果は表1のとおりであり、GMC のGMR の両側95%信頼区間の下限値及
び中和抗体応答率の差の両側95%信頼区間の下限値は、いずれも事前に
設定された非劣性限界値を上回り、またGMCのGMR の点推定値は0.8以
上であり、中和抗体応答率の差の点推定値は−10%を上回ったことから、
本試験の12~17歳の被験者の免疫原性データについて、P301試験の18
~25歳の被験者データに対する非劣性が確認された。
非劣性の成功基準は、(1)「GMC の幾何平均比(本試験(Day 29)のGMC/P301 試験の18~25 歳(Day 57)のGMC)」の95%信頼区間の下限が0.67(1/1.5)を上回り、かつ点推定値が0.8 以上、
(2)中和抗体応答率の差の95%信頼区間の下限が−10%を上回ることとし、これら二つの基準を満たす場合に非劣性が示されたと判断することとされた。
11