よむ、つかう、まなぶ。
03【資料1】新型コロナワクチンの接種について (13 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_29727.html |
| 出典情報 | 厚生科学審議会 予防接種・ワクチン分科会(第42回 12/13)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
【1】令和4年秋開始接種に使用するワクチンについて
(1)モデルナ社のオミクロン株対応2価ワクチンの対象年齢について
スパイクバックスの対象年齢拡大の評価について
薬事・食品衛生審議会の事務局として、PMDA及び厚生労働省は、薬事・食品衛生審議会提出資料において、今般
提出された従来型ワクチンによる12~17歳への追加免疫の臨床試験結果を踏まえると、オミクロン株対応2価ワクチ
ンによる追加免疫の接種対象年齢についても12歳以上に拡大することは可能と判断している。
モデルナ社試験(薬事・食品衛生審議会提出資料、抜粋)
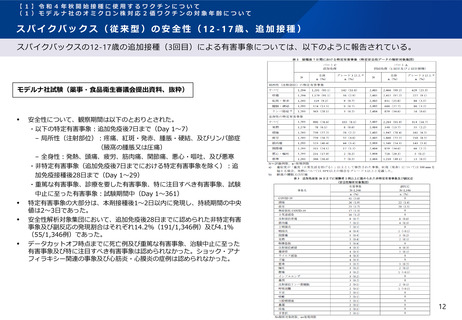
今般提出された本剤による12~17歳への追加免疫の臨床試験結果を踏まえると、起源
株1価ワクチンについては、12~17歳の年齢層では18~25歳の年齢層に対しSARSCoV-2 の起源株に対する中和抗体価の非劣性が示され、安全性についても重大な懸念は
認められず、忍容可能と考えられることから、追加免疫の接種対象年齢を12歳以上に拡
大することは可能と考える。
また、mRNA-1273.214(オミクロン株BA.1対応の2価ワクチン)の18歳以上への追
加免疫の臨床試験(mRNA-1273-P205 試験)の結果等から、オミクロン株対応の2価
ワクチンについて、接種対象年齢を18歳以上として追加免疫に係る用法及び用量が承認
されており、「新型コロナウイルス(SARS-CoV-2)ワクチンの評価に関する考え方
(補遺1)変異株に対するワクチンの評価について」(令和3年4月5日付け独立行政法
人医薬品医療機器総合機構ワクチン等審査部)において、単一の年齢層で実施した変異
株ワクチンの臨床試験の結果は、一般的に、親ワクチンで承認されている他の年齢層に
外挿可能とされていることから、親ワクチン(起源株1価ワクチン)の追加免疫の接種
対象年齢と同様に、オミクロン株対応の2価ワクチンの接種対象年齢についても12歳以
上に拡大することは可能と考える。
13
(1)モデルナ社のオミクロン株対応2価ワクチンの対象年齢について
スパイクバックスの対象年齢拡大の評価について
薬事・食品衛生審議会の事務局として、PMDA及び厚生労働省は、薬事・食品衛生審議会提出資料において、今般
提出された従来型ワクチンによる12~17歳への追加免疫の臨床試験結果を踏まえると、オミクロン株対応2価ワクチ
ンによる追加免疫の接種対象年齢についても12歳以上に拡大することは可能と判断している。
モデルナ社試験(薬事・食品衛生審議会提出資料、抜粋)
今般提出された本剤による12~17歳への追加免疫の臨床試験結果を踏まえると、起源
株1価ワクチンについては、12~17歳の年齢層では18~25歳の年齢層に対しSARSCoV-2 の起源株に対する中和抗体価の非劣性が示され、安全性についても重大な懸念は
認められず、忍容可能と考えられることから、追加免疫の接種対象年齢を12歳以上に拡
大することは可能と考える。
また、mRNA-1273.214(オミクロン株BA.1対応の2価ワクチン)の18歳以上への追
加免疫の臨床試験(mRNA-1273-P205 試験)の結果等から、オミクロン株対応の2価
ワクチンについて、接種対象年齢を18歳以上として追加免疫に係る用法及び用量が承認
されており、「新型コロナウイルス(SARS-CoV-2)ワクチンの評価に関する考え方
(補遺1)変異株に対するワクチンの評価について」(令和3年4月5日付け独立行政法
人医薬品医療機器総合機構ワクチン等審査部)において、単一の年齢層で実施した変異
株ワクチンの臨床試験の結果は、一般的に、親ワクチンで承認されている他の年齢層に
外挿可能とされていることから、親ワクチン(起源株1価ワクチン)の追加免疫の接種
対象年齢と同様に、オミクロン株対応の2価ワクチンの接種対象年齢についても12歳以
上に拡大することは可能と考える。
13