よむ、つかう、まなぶ。
03【資料1】新型コロナワクチンの接種について (12 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_29727.html |
| 出典情報 | 厚生科学審議会 予防接種・ワクチン分科会(第42回 12/13)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
【1】令和4年秋開始接種に使用するワクチンについて
(1)モデルナ社のオミクロン株対応2価ワクチンの対象年齢について
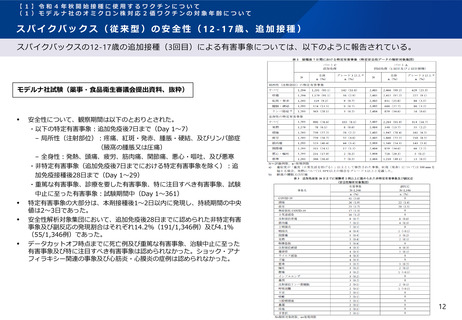
スパイクバックス(従来型)の安全性(12-17歳、追加接種)
スパイクバックスの12-17歳の追加接種(3回目)による有害事象については、以下のように報告されている。
モデルナ社試験(薬事・食品衛生審議会提出資料、抜粋)
安全性について、観察期間は以下のとおりとされた。
・以下の特定有害事象:追加免疫後7日まで(Day 1~7)
– 局所性(注射部位):疼痛、紅斑・発赤、腫脹・硬結、及びリンパ節症
(腋窩の腫脹又は圧痛)
– 全身性:発熱、頭痛、疲労、筋肉痛、関節痛、悪心・嘔吐、及び悪寒
・非特定有害事象(追加免疫後7日までにおける特定有害事象を除く):追
加免疫接種後28日まで(Day 1~29)
・重篤な有害事象、診療を要した有害事象、特に注目すべき有害事象、試験
中止に至った有害事象:試験期間中(Day 1~361)
特定有害事象の大部分は、本剤接種後1~2日以内に発現し、持続期間の中央
値は2~3日であった。
安全性解析対象集団において、追加免疫後28日までに認められた非特定有害
事象及び副反応の発現割合はそれぞれ14.2%(191/1,346例)及び4.1%
(55/1,346例)であった。
データカットオフ時点までに死亡例及び重篤な有害事象、治験中止に至った
有害事象及び特に注目すべき有害事象は認められなかった。ショック・アナ
フィラキシー関連の事象及び心筋炎・心膜炎の症例は認められなかった。
12
(1)モデルナ社のオミクロン株対応2価ワクチンの対象年齢について
スパイクバックス(従来型)の安全性(12-17歳、追加接種)
スパイクバックスの12-17歳の追加接種(3回目)による有害事象については、以下のように報告されている。
モデルナ社試験(薬事・食品衛生審議会提出資料、抜粋)
安全性について、観察期間は以下のとおりとされた。
・以下の特定有害事象:追加免疫後7日まで(Day 1~7)
– 局所性(注射部位):疼痛、紅斑・発赤、腫脹・硬結、及びリンパ節症
(腋窩の腫脹又は圧痛)
– 全身性:発熱、頭痛、疲労、筋肉痛、関節痛、悪心・嘔吐、及び悪寒
・非特定有害事象(追加免疫後7日までにおける特定有害事象を除く):追
加免疫接種後28日まで(Day 1~29)
・重篤な有害事象、診療を要した有害事象、特に注目すべき有害事象、試験
中止に至った有害事象:試験期間中(Day 1~361)
特定有害事象の大部分は、本剤接種後1~2日以内に発現し、持続期間の中央
値は2~3日であった。
安全性解析対象集団において、追加免疫後28日までに認められた非特定有害
事象及び副反応の発現割合はそれぞれ14.2%(191/1,346例)及び4.1%
(55/1,346例)であった。
データカットオフ時点までに死亡例及び重篤な有害事象、治験中止に至った
有害事象及び特に注目すべき有害事象は認められなかった。ショック・アナ
フィラキシー関連の事象及び心筋炎・心膜炎の症例は認められなかった。
12