よむ、つかう、まなぶ。
資料2.緊急時の薬事承認の在り方 (12 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_22281.html |
| 出典情報 | 厚生科学審議会 医薬品医療機器制度部会(令和3度第1回 11/18)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
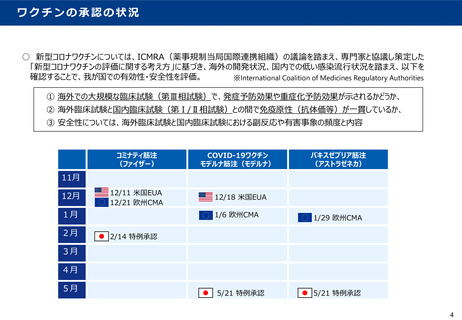
「新型コロナウイルスワクチンの評価に関する考え方」について①
○ PMDAが、ICMRA(欧米日等各国の薬事規制当局国際連携)の議論や米国FDAのガイダ
ンスの内容も踏まえ、専門家と協議して策定したもの(2020年9月2日公表)
【ポイント抜粋】
* 基本的な考え方はICMRAと同じであり、指針として明確化したもの
<有効性の評価>
○ 原則として、発症予防効果を主要評価項目として臨床試験を実施する必要がある。
なお、副次評価項目として、重症度に関する項目等についても評価を行う。
○ 発症予防効果に関係する免疫原性の指標が確認された場合には、当該指標の確認によ
り、有効性を評価できる可能性がある。
<国内臨床試験における評価>
○ 国・地域による流行状況やウイルス株の違い、民族的要因の差等を踏まえると、国内
で臨床試験を実施し、日本人被験者における有効性及び安全性を検討する必要がある。
<海外開発型のワクチン候補、有効性の評価>
○ 海外で発症予防効果を主要評価項目とした大規模な検証的臨床試験が実施される場合
には、国内で日本人における免疫原性(抗体価等)及び安全性を確認することを目的とし
た国内臨床試験を実施することで十分な場合がある。
12
○ PMDAが、ICMRA(欧米日等各国の薬事規制当局国際連携)の議論や米国FDAのガイダ
ンスの内容も踏まえ、専門家と協議して策定したもの(2020年9月2日公表)
【ポイント抜粋】
* 基本的な考え方はICMRAと同じであり、指針として明確化したもの
<有効性の評価>
○ 原則として、発症予防効果を主要評価項目として臨床試験を実施する必要がある。
なお、副次評価項目として、重症度に関する項目等についても評価を行う。
○ 発症予防効果に関係する免疫原性の指標が確認された場合には、当該指標の確認によ
り、有効性を評価できる可能性がある。
<国内臨床試験における評価>
○ 国・地域による流行状況やウイルス株の違い、民族的要因の差等を踏まえると、国内
で臨床試験を実施し、日本人被験者における有効性及び安全性を検討する必要がある。
<海外開発型のワクチン候補、有効性の評価>
○ 海外で発症予防効果を主要評価項目とした大規模な検証的臨床試験が実施される場合
には、国内で日本人における免疫原性(抗体価等)及び安全性を確認することを目的とし
た国内臨床試験を実施することで十分な場合がある。
12