よむ、つかう、まなぶ。
参考資料14 定期の予防接種等による副反応疑いの報告等の取扱いについて(平成25年3月30日付け健発0330第3号・薬食発0330第1号厚生労働省健康局長及び医薬食品局長連名通知。最終改正:令和4年10月24日) (5 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000208910_00059.html |
| 出典情報 | 第92回厚生科学審議会予防接種・ワクチン分科会副反応検討部会、令和4年度第27回薬事・食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会(合同開催)(3/10)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
(7)過去にヒトパピローマウイルス感染症の定期の予防接種又は任意接種の接種後に
広範な慢性の疼痛又は運動障害を中心とする多様な症状が発生した患者であって、
既に当該症状については治療を受けていないものについても、(3)又は(4)と
同様に取り扱うこと。
5
新型コロナウイルス感染症の臨時の予防接種に係る対応
新型コロナワクチンについては、これまでワクチン接種との因果関係が示されてい
ない症状も含め、幅広く評価を行っていく必要があることから、当面の間、以下の症
状については当該規定による副反応疑い報告を積極的に行うよう検討するとともに、
これら以外の症状についても必要に応じて報告を検討すること。
けいれん(ただし、熱性けいれんを除く。)、ギラン・バレ症候群、急性散在性脳
脊髄炎(ADEM)、血小板減少性紫斑病、血管炎、無菌性髄膜炎、脳炎・脳症、関
節炎、脊髄炎、顔面神経麻痺、血管迷走神経反射(失神を伴うもの)
また、副反応疑い報告基準に基づき、
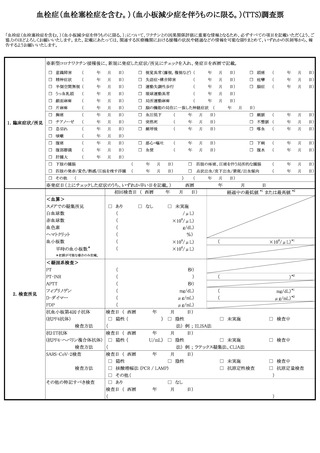
「血栓症(血栓塞栓症を含む。)
(血小板減少症
を伴うものに限る。)」、「心筋炎」又は「心膜炎」について報告する場合にあっては、
評価にあたり当該症例に係る症状の概要等を詳細に把握する必要があることから、別
紙様式1記入要領別表の記載も踏まえ、別紙様式1に加えて、TTS調査票、心筋炎
調査票又は心膜炎調査票をそれぞれ作成し、報告すること。ただし、心筋炎及び心膜
炎がともに疑われる場合にあっては、心筋炎調査票及び心膜炎調査票の両方を作成し
て報告すること。各調査票の作成にあたっては、全ての項目について遺漏なく記入す
ること。また、報告対象となる症例の経過において複数の医師等が関与した場合にあ
っては、接種の状況や経過等の情報を可能な限り集約して調査票に記入の上、一の医
師等が代表して報告することが望ましいこと。
広範な慢性の疼痛又は運動障害を中心とする多様な症状が発生した患者であって、
既に当該症状については治療を受けていないものについても、(3)又は(4)と
同様に取り扱うこと。
5
新型コロナウイルス感染症の臨時の予防接種に係る対応
新型コロナワクチンについては、これまでワクチン接種との因果関係が示されてい
ない症状も含め、幅広く評価を行っていく必要があることから、当面の間、以下の症
状については当該規定による副反応疑い報告を積極的に行うよう検討するとともに、
これら以外の症状についても必要に応じて報告を検討すること。
けいれん(ただし、熱性けいれんを除く。)、ギラン・バレ症候群、急性散在性脳
脊髄炎(ADEM)、血小板減少性紫斑病、血管炎、無菌性髄膜炎、脳炎・脳症、関
節炎、脊髄炎、顔面神経麻痺、血管迷走神経反射(失神を伴うもの)
また、副反応疑い報告基準に基づき、
「血栓症(血栓塞栓症を含む。)
(血小板減少症
を伴うものに限る。)」、「心筋炎」又は「心膜炎」について報告する場合にあっては、
評価にあたり当該症例に係る症状の概要等を詳細に把握する必要があることから、別
紙様式1記入要領別表の記載も踏まえ、別紙様式1に加えて、TTS調査票、心筋炎
調査票又は心膜炎調査票をそれぞれ作成し、報告すること。ただし、心筋炎及び心膜
炎がともに疑われる場合にあっては、心筋炎調査票及び心膜炎調査票の両方を作成し
て報告すること。各調査票の作成にあたっては、全ての項目について遺漏なく記入す
ること。また、報告対象となる症例の経過において複数の医師等が関与した場合にあ
っては、接種の状況や経過等の情報を可能な限り集約して調査票に記入の上、一の医
師等が代表して報告することが望ましいこと。