よむ、つかう、まなぶ。
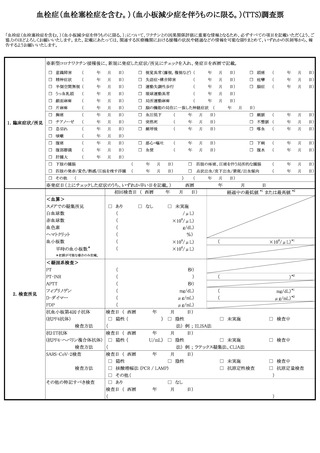
参考資料14 定期の予防接種等による副反応疑いの報告等の取扱いについて(平成25年3月30日付け健発0330第3号・薬食発0330第1号厚生労働省健康局長及び医薬食品局長連名通知。最終改正:令和4年10月24日) (6 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000208910_00059.html |
| 出典情報 | 第92回厚生科学審議会予防接種・ワクチン分科会副反応検討部会、令和4年度第27回薬事・食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会(合同開催)(3/10)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
(改正)
平成 26 年 10 月1日
一部改正
平成 26 年 11 月 25 日
一部改正
平成 28 年 10 月 1 日
一部改正
平成 29 年9月 25 日
一部改正
令和元年5月7日
一部改正
令和元年9月 27 日
一部改正
令和2年3月 26 日
一部改正
令和2年 10 月 1 日
一部改正
令和3年2月 16 日
一部改正
令和3年3月 25 日
一部改正
令和3年8月2日
一部改正
令和3年8月 16 日
一部改正
令和3年 12 月6日
一部改正
令和4年3月 18 日
一部改正
令和4年 10 月 24 日
一部改正
(別記)
任意接種における報告対象となる情報は、予防接種ワクチンの使用による副作用、感染
症の発生について、保健衛生上の危害の発生又は拡大を防止する観点から報告の必要があ
ると判断した情報(症例)であり、具体的には以下の事項(症例)を参考とすること。な
お、ワクチンとの因果関係が必ずしも明確でない場合であっても報告の対象となり得るこ
と。
① 死亡
② 障害
③ 死亡につながるおそれのある症例
④ 障害につながるおそれのある症例
⑤ 治療のために病院又は診療所への入院又は入院期間の延長が必要とされる症状(③
及④に掲げる症例を除く。)
⑥ ①から⑤までに掲げる症例に準じて重篤である症例
⑦ 後世代における先天性の疾病又は異常
⑧ 当該医薬品の使用によるものと疑われる感染症による症例等の発生
⑨ ①から⑧までに示す症例以外で、軽微ではなく、かつ、添付文書等から予測できない
未知の症例等の発生
平成 26 年 10 月1日
一部改正
平成 26 年 11 月 25 日
一部改正
平成 28 年 10 月 1 日
一部改正
平成 29 年9月 25 日
一部改正
令和元年5月7日
一部改正
令和元年9月 27 日
一部改正
令和2年3月 26 日
一部改正
令和2年 10 月 1 日
一部改正
令和3年2月 16 日
一部改正
令和3年3月 25 日
一部改正
令和3年8月2日
一部改正
令和3年8月 16 日
一部改正
令和3年 12 月6日
一部改正
令和4年3月 18 日
一部改正
令和4年 10 月 24 日
一部改正
(別記)
任意接種における報告対象となる情報は、予防接種ワクチンの使用による副作用、感染
症の発生について、保健衛生上の危害の発生又は拡大を防止する観点から報告の必要があ
ると判断した情報(症例)であり、具体的には以下の事項(症例)を参考とすること。な
お、ワクチンとの因果関係が必ずしも明確でない場合であっても報告の対象となり得るこ
と。
① 死亡
② 障害
③ 死亡につながるおそれのある症例
④ 障害につながるおそれのある症例
⑤ 治療のために病院又は診療所への入院又は入院期間の延長が必要とされる症状(③
及④に掲げる症例を除く。)
⑥ ①から⑤までに掲げる症例に準じて重篤である症例
⑦ 後世代における先天性の疾病又は異常
⑧ 当該医薬品の使用によるものと疑われる感染症による症例等の発生
⑨ ①から⑧までに示す症例以外で、軽微ではなく、かつ、添付文書等から予測できない
未知の症例等の発生