よむ、つかう、まなぶ。
材-1○ 保険医療材料制度の見直しに関する検討(その2)について (13 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000212455_00037.html |
| 出典情報 | 中央社会保険医療協議会 保険医療材料専門部会(第123回 10/27)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
(参考)希少疾病用医薬品等の指定制度について
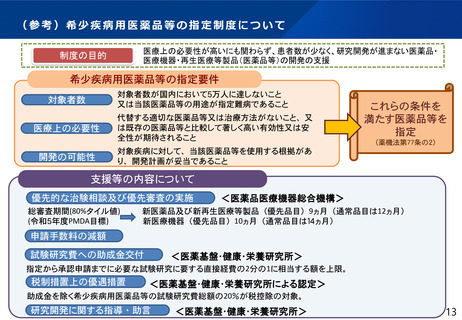
医療上の必要性が高いにも関わらず、患者数が少なく、研究開発が進まない医薬品・
医療機器・再生医療等製品(医薬品等)の開発の支援
制度の目的
希少疾病用医薬品等の指定要件
対象者数が国内において5万人に達しないこと
又は当該医薬品等の用途が指定難病であること
対象者数
医療上の必要性
開発の可能性
代替する適切な医薬品等又は治療方法がないこと、又
は既存の医薬品等と比較して著しく高い有効性又は安
全性が期待されること
これらの条件を
満たす医薬品等を
指定
(薬機法第77条の2)
対象疾病に対して、当該医薬品等を使用する根拠があ
り、開発計画が妥当であること
支援等の内容について
優先的な治験相談及び優先審査の実施
総審査期間(80%タイル値)
(令和5年度PMDA目標)
<医薬品医療機器総合機構>
新医薬品及び新再生医療等製品(優先品目)9ヵ月(通常品目は12ヵ月)
新医療機器(優先品目)10ヵ月(通常品目は14ヵ月)
申請手数料の減額
試験研究費への助成金交付
<医薬基盤・健康・栄養研究所>
指定から承認申請までに必要な試験研究に要する直接経費の2分の1に相当する額を上限。
税制措置上の優遇措置
<医薬基盤・健康・栄養研究所による認定>
助成金を除く希少疾病用医薬品等の試験研究費総額の20%が税控除の対象。
研究開発に関する指導・助言
<医薬基盤・健康・栄養研究所>
13
医療上の必要性が高いにも関わらず、患者数が少なく、研究開発が進まない医薬品・
医療機器・再生医療等製品(医薬品等)の開発の支援
制度の目的
希少疾病用医薬品等の指定要件
対象者数が国内において5万人に達しないこと
又は当該医薬品等の用途が指定難病であること
対象者数
医療上の必要性
開発の可能性
代替する適切な医薬品等又は治療方法がないこと、又
は既存の医薬品等と比較して著しく高い有効性又は安
全性が期待されること
これらの条件を
満たす医薬品等を
指定
(薬機法第77条の2)
対象疾病に対して、当該医薬品等を使用する根拠があ
り、開発計画が妥当であること
支援等の内容について
優先的な治験相談及び優先審査の実施
総審査期間(80%タイル値)
(令和5年度PMDA目標)
<医薬品医療機器総合機構>
新医薬品及び新再生医療等製品(優先品目)9ヵ月(通常品目は12ヵ月)
新医療機器(優先品目)10ヵ月(通常品目は14ヵ月)
申請手数料の減額
試験研究費への助成金交付
<医薬基盤・健康・栄養研究所>
指定から承認申請までに必要な試験研究に要する直接経費の2分の1に相当する額を上限。
税制措置上の優遇措置
<医薬基盤・健康・栄養研究所による認定>
助成金を除く希少疾病用医薬品等の試験研究費総額の20%が税控除の対象。
研究開発に関する指導・助言
<医薬基盤・健康・栄養研究所>
13