よむ、つかう、まなぶ。
資料1-2 精製ヒアルロン酸ナトリウムのリスク 区分について[5.0MB] (3 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_39892.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会安全対策調査会(令和6年度第2回 4/30)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
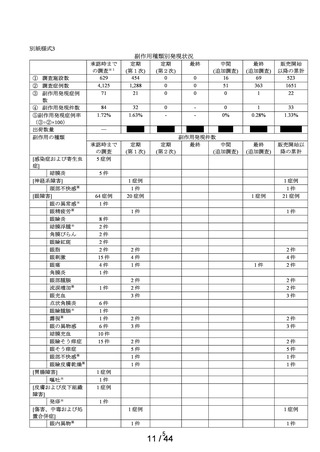
副作用等発現状況
本剤
(第1類医薬品)
販売名(成分名及び成
分量)
ヒアレイン S/サンテ ヒアルロン酸点
眼液
調査症例数
感染症及び寄
生虫症
免疫系障害
代謝及び栄養
障害
精神障害
神経系障害
【使用成績調査・特定使用成績調査・製造販売
後調査】
追加調査
2023/3/1~2023/5/30
1,288例
363例
※
ソフトサンティア
製造販売後調査
未実施
-
4,112例
1症例の中に複数の副作用を発現した場合は、副作用の領域毎にそれぞれ1例(%)として集計している。
78例84件
(1.90)
21例32件
(1.63)
1例1件
(0.28)
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
1例1件
(0.08)
-
-
-
-
-
-
-
-
眼瞼そう痒感(16)
眼刺激(15)
結膜充血(9)
眼瞼炎(9)
びまん性表層角膜炎
(6)
眼痛(5)
結膜炎(5)
眼の異物感(4)
角膜びらん(2)
眼脂(2)
霧視(2)
眼瞼発赤 (2)
眼瞼腫脹(2)
角膜炎(1)
眼の乾燥感(1)
20例29件
(1.55)
1例1件
(0.28)
75例81件
(1.82)
-
-
-
-
-
-
-
-
-
-
-
-
血管障害
-
-
-
-
-
-
呼吸器、胸郭
および縦隔障
害
-
-
-
-
-
-
胃腸障害
-
-
1例1件
(0.02)
-
-
肝胆道系障害
-
-
-
-
-
皮膚及び皮下
組織障害
-
-
2例2件
(0.05)
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
一般・全身障
害および投与
部位の状態
-
-
-
-
-
-
臨床検査
-
-
-
-
-
-
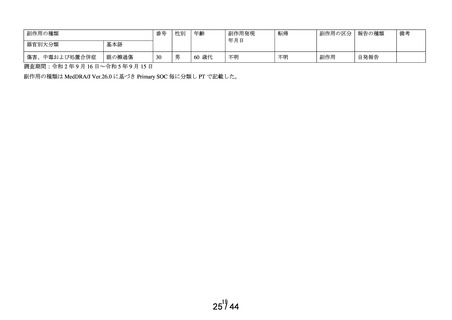
傷害、中毒お
よび処置合併
症
1例1件
(0.08)
-
-
-
-
-
製品の問題
1例1件
(0.08)
-
-
-
-
-
眼障害
耳および迷路
障害
心臓障害
筋骨格系およ
び結合組織障
害
腎および尿路
障害
生殖系および
乳房障害
一
般
調
査
ヒアレイン点眼液0.1%
(5mL中塩化ナトリウム 0.4%、塩化カリウム0.1%)
第一次・二次調査
2022/9/15まで
副作用発現件
数/件・例
(率:%)
合計件数
(第3類医薬品)
(5mL中精製ヒアル
ロン酸ナトリウム 0.1%)
2020/9/16~2023/9/15
販売開始~製造販売後
調査期間終了
類薬(参考)
医療用同一成分
嘔吐(1)
接触(性)皮膚炎(1)
発疹(1)
副作用報告数
59例80件
217例272件
主な副作用
眼の異常感10件、眼刺激10件、眼そう痒症6件、眼痛
6件 他
眼刺激36件、眼の異常感23件、眼痛21件、
霧視20件、流涙増加13件 他
注1) 本剤及び医療用同一成分に含有される添加物は同一である。
注2) 類薬の副作用報告件数は、医薬品医療機器法第68 条の 10 第1項に基づき、製造販売業者が報告した副作用報告の件数(集計対象期間:2020年9月16日~2023年9月15日)
3 / 44
本剤
(第1類医薬品)
販売名(成分名及び成
分量)
ヒアレイン S/サンテ ヒアルロン酸点
眼液
調査症例数
感染症及び寄
生虫症
免疫系障害
代謝及び栄養
障害
精神障害
神経系障害
【使用成績調査・特定使用成績調査・製造販売
後調査】
追加調査
2023/3/1~2023/5/30
1,288例
363例
※
ソフトサンティア
製造販売後調査
未実施
-
4,112例
1症例の中に複数の副作用を発現した場合は、副作用の領域毎にそれぞれ1例(%)として集計している。
78例84件
(1.90)
21例32件
(1.63)
1例1件
(0.28)
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
1例1件
(0.08)
-
-
-
-
-
-
-
-
眼瞼そう痒感(16)
眼刺激(15)
結膜充血(9)
眼瞼炎(9)
びまん性表層角膜炎
(6)
眼痛(5)
結膜炎(5)
眼の異物感(4)
角膜びらん(2)
眼脂(2)
霧視(2)
眼瞼発赤 (2)
眼瞼腫脹(2)
角膜炎(1)
眼の乾燥感(1)
20例29件
(1.55)
1例1件
(0.28)
75例81件
(1.82)
-
-
-
-
-
-
-
-
-
-
-
-
血管障害
-
-
-
-
-
-
呼吸器、胸郭
および縦隔障
害
-
-
-
-
-
-
胃腸障害
-
-
1例1件
(0.02)
-
-
肝胆道系障害
-
-
-
-
-
皮膚及び皮下
組織障害
-
-
2例2件
(0.05)
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
一般・全身障
害および投与
部位の状態
-
-
-
-
-
-
臨床検査
-
-
-
-
-
-
傷害、中毒お
よび処置合併
症
1例1件
(0.08)
-
-
-
-
-
製品の問題
1例1件
(0.08)
-
-
-
-
-
眼障害
耳および迷路
障害
心臓障害
筋骨格系およ
び結合組織障
害
腎および尿路
障害
生殖系および
乳房障害
一
般
調
査
ヒアレイン点眼液0.1%
(5mL中塩化ナトリウム 0.4%、塩化カリウム0.1%)
第一次・二次調査
2022/9/15まで
副作用発現件
数/件・例
(率:%)
合計件数
(第3類医薬品)
(5mL中精製ヒアル
ロン酸ナトリウム 0.1%)
2020/9/16~2023/9/15
販売開始~製造販売後
調査期間終了
類薬(参考)
医療用同一成分
嘔吐(1)
接触(性)皮膚炎(1)
発疹(1)
副作用報告数
59例80件
217例272件
主な副作用
眼の異常感10件、眼刺激10件、眼そう痒症6件、眼痛
6件 他
眼刺激36件、眼の異常感23件、眼痛21件、
霧視20件、流涙増加13件 他
注1) 本剤及び医療用同一成分に含有される添加物は同一である。
注2) 類薬の副作用報告件数は、医薬品医療機器法第68 条の 10 第1項に基づき、製造販売業者が報告した副作用報告の件数(集計対象期間:2020年9月16日~2023年9月15日)
3 / 44