よむ、つかう、まなぶ。
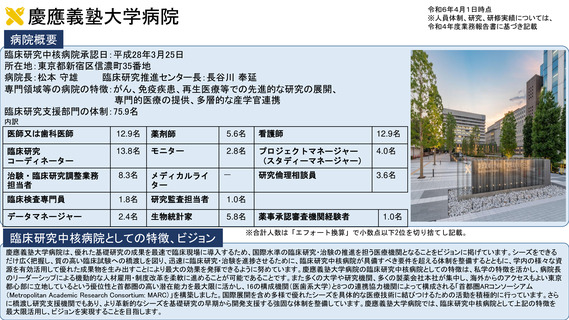
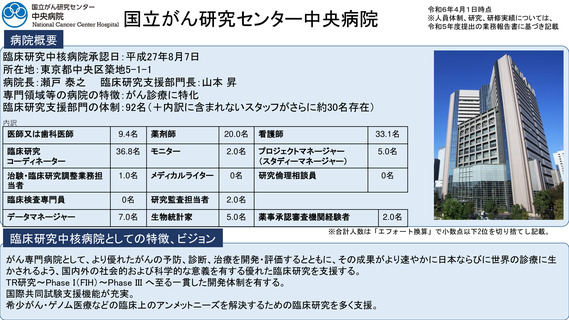
参考資料2:臨床研究中核病院概要 (11 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_42147.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第35回 8/8)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
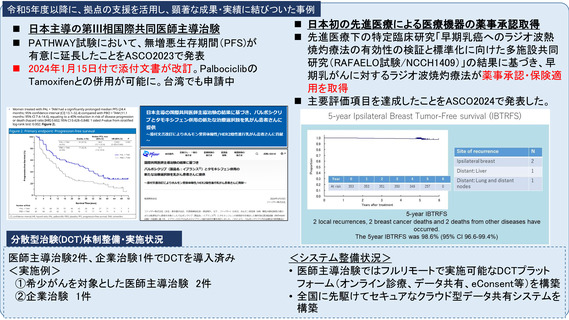
先進医療への対応
・先進医療に関しては、未承認医療機器を用いたFirst in Human の先進医療 B 試験を支援部門が支援し 3 試験実施
・現時点では先進医療B については、 CRC 業務などについては臨床研究コーディネーター室、データセンター機能などのセントラル機能については臨床研究支
援部門もしくは外部CRO などを活用して実施している
患者申出療養への対応
患者申し出療養の窓口を運営するとともに、本制度を活用した他施設主導研究に参加。
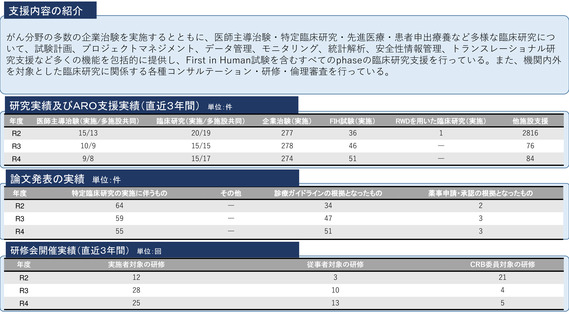
国際共同臨床研究・治験の実施状況
・SCRUM-Asiaでは、タイ・台 マレーシアの3か国に加えてベトナムが追加された。
・CICULATE Japanでは観察研究6,300名、 比較試験へ1,000名を超える登録を達成
・TITANIA studyでは目標を超える216名の登録を実施
・ARCAD-Asiaではデータベースが本格稼働し、ARCAR-globalとの5万例の統合データベースがARCARD-Asiaに統合された。
また、2023年度では、新規企業治験105件中、国際共同治験85件(実施地中では396/522件)であった。
ベンチャー企業への支援実施状況
・NCC発ベンチャー認定制度にて6社が認定ベンチャーとして認定済み
・M&Aで導出した1社の手術支援ロボットが承認取得、1社がIPOを達成、1社がFIHを実施中
・スタートアップ企業を育成するNCC Venture Incubation Program第III期を開始し6チームを支援
・先進医療に関しては、未承認医療機器を用いたFirst in Human の先進医療 B 試験を支援部門が支援し 3 試験実施
・現時点では先進医療B については、 CRC 業務などについては臨床研究コーディネーター室、データセンター機能などのセントラル機能については臨床研究支
援部門もしくは外部CRO などを活用して実施している
患者申出療養への対応
患者申し出療養の窓口を運営するとともに、本制度を活用した他施設主導研究に参加。
国際共同臨床研究・治験の実施状況
・SCRUM-Asiaでは、タイ・台 マレーシアの3か国に加えてベトナムが追加された。
・CICULATE Japanでは観察研究6,300名、 比較試験へ1,000名を超える登録を達成
・TITANIA studyでは目標を超える216名の登録を実施
・ARCAD-Asiaではデータベースが本格稼働し、ARCAR-globalとの5万例の統合データベースがARCARD-Asiaに統合された。
また、2023年度では、新規企業治験105件中、国際共同治験85件(実施地中では396/522件)であった。
ベンチャー企業への支援実施状況
・NCC発ベンチャー認定制度にて6社が認定ベンチャーとして認定済み
・M&Aで導出した1社の手術支援ロボットが承認取得、1社がIPOを達成、1社がFIHを実施中
・スタートアップ企業を育成するNCC Venture Incubation Program第III期を開始し6チームを支援